Clear Sky Science · nl
De novo covalente geneesmiddelontwikkeling met verbeterde drug‑likeness en veiligheid
Waarom slimmer covalente geneesmiddelen ertoe doen
Antikankermedicijnen en antivirale middelen werken vaak doordat ze zich vasthechten aan eiwitten in onze cellen. Een krachtige klasse geneesmiddelen, covalente middelen, gaat een stap verder: ze vormen sterke, langdurige bindingen met hun doelen, wat ze zeer effectief kan maken. Diezelfde kleefkracht kan echter ook ernstige bijwerkingen veroorzaken als de middelen zich aan de verkeerde eiwitten binden. Deze studie introduceert CovaGEN, een nieuw kunstmatig‑intelligentiesysteem dat covalente geneesmiddelkandidaten van de grond af kan ontwerpen, met nadruk op zowel werkzaamheid als veiligheid.
Van proberen en fouten naar slim ontwerp
Traditionele ontdekking van covalente geneesmiddelen is traag en duur. Scheikundigen beginnen vaak met een bestaand medicijn en zetten daar een reactieve "hendel" op, of ze starten met een reactief fragment en moeten vervolgens het restant van het molecuul zorgvuldig afstemmen. Computerondersteunde methoden helpen door grote bibliotheken bekende verbindingen te screenen, maar ze zijn beperkt tot wat al bestaat. Recente doorbraken in deep learning kunnen volledig nieuwe moleculen genereren, maar deze tools richten zich meestal op conventionele, niet‑covalente medicijnen en negeren vaak essentiële eigenschappen zoals hoe makkelijk een verbinding te synthetiseren is, of ze zich als een echt medicijn gedraagt, of hoe toxisch ze kunnen zijn. CovaGEN pakt al deze vragen tegelijk aan.
Een verborgen kaart van medicijnachtige chemie
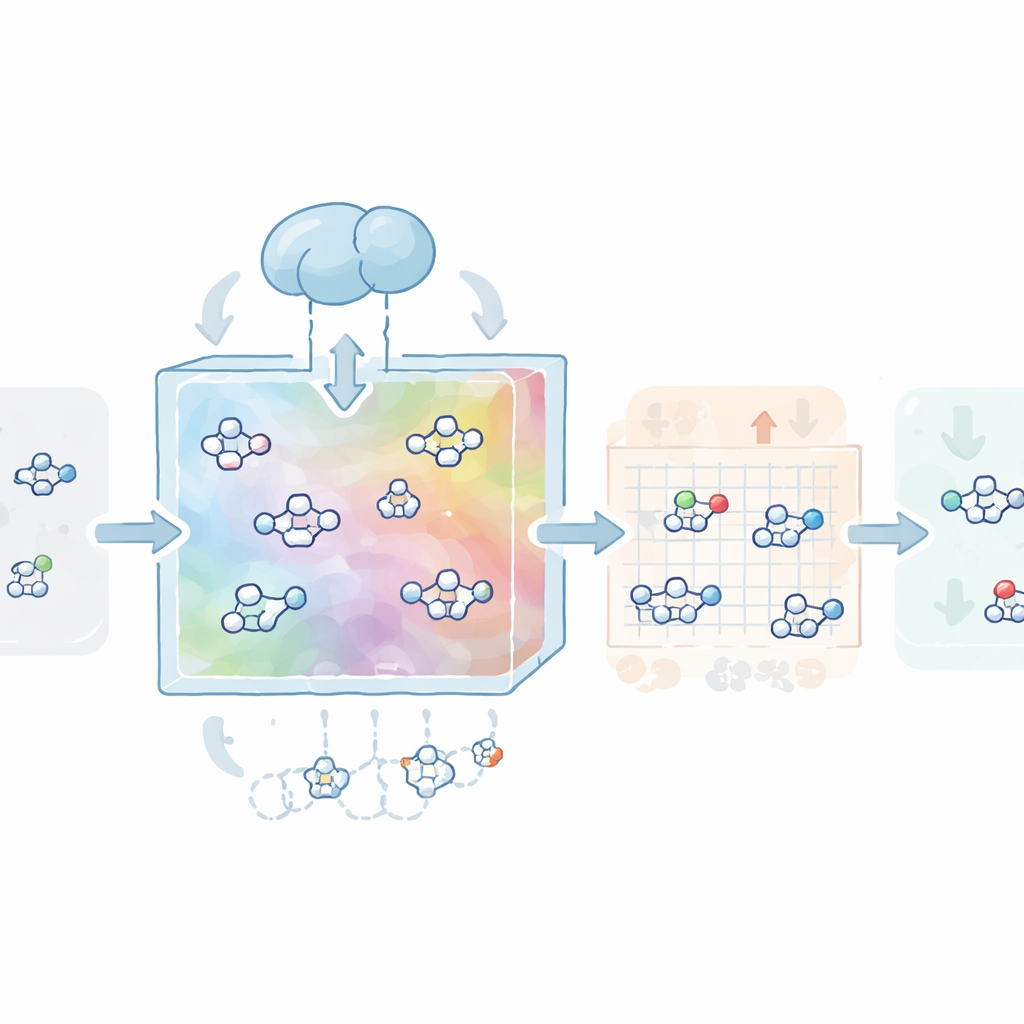
De auteurs bouwden eerst een "kaart" van de chemische ruimte met meer dan een miljoen medicijnachtige moleculen uit de openbare ZINC‑database. Ze trainden een type neuraal netwerk, een variational autoencoder, om elk molecuul samen te persen tot een compact numeriek coderingselement, of latente vector, en het vervolgens te reconstrueren. Deze stap leert het model de basale grammatica van medicinale chemie: wat er realistisch uitziet, wat voldoet aan gebruikelijke regels voor orale geneesmiddelen, en wat synthetisch haalbaar lijkt. Op deze aangeleerde kaart werd een tweede model, gebaseerd op diffusie — een proces dat structuur geleidelijk in ruis verandert en vervolgens leert dat proces om te keren — getraind om te dwalen en nieuwe latente vectoren te genereren die decoderen naar geldige, diverse en realistische moleculen.
Moleculen afstemmen op eiwitten en kleverige haakjes
Vervolgens leert CovaGEN moleculen te ontwerpen voor specifieke eiwitdoelen. Het systeem neemt de aminozuurvolgorde van een eiwit en codeert die met een krachtig taalmodel voor eiwitten, dat patronen met betrekking tot structuur en functie vastlegt. Tijdens diffusie besteedt het model cross‑attention aan deze eiwitreprepresentatie zodat de gegenereerde moleculen geneigd zijn te passen in de bindingsplaats van het target. In tests op een grote benchmarkset scoorden deze op maat gemaakte moleculen niet alleen goed voor voorspelde bindingssterkte, maar toonden ze ook betere drug‑likeness en synthetische toegankelijkheid dan ontwerpen van verschillende geavanceerde 3D‑ontwerptools. Om van deze niet‑covalente binders covalente kandidaten te maken, voegde het team een classifier toe die het diffusieproces richting moleculen met bepaalde reactieve groepen — zogenoemde covalente warheads — stuurt, zonder in te boeten aan algemene kwaliteit.
Veiligheid vanaf het begin inbouwen
Aangezien covalente geneesmiddelen blijvende schade kunnen veroorzaken als ze de verkeerde targets raken, staat veiligheid centraal. De onderzoekers behandelden toxiciteit daarom als een optimaliseerbare grootheid, niet als een bijzaak. Ze trainden voorspellende modellen voor acute toxiciteit en orgaanspecifieke risico's en pasten vervolgens reinforcement learning toe om het diffusiemodel fijn af te stemmen zodat het de voorkeur geeft aan moleculen met lagere voorspelde toxiciteit. Na deze training genereerde CovaGEN verbindingen die goede bindings‑ en medicijnachtige eigenschappen behielden, maar minder geneigd waren structurele "rode vlaggen" te bevatten die met schadelijke effecten geassocieerd worden. Belangrijk is dat de methode dit bereikte zonder te vervallen tot een smalle set soortgelijke moleculen, waardoor chemische diversiteit behouden bleef.
De methode op de proef stellen
Om het reële potentieel te demonstreren vroeg het team CovaGEN covalente remmers te ontwerpen voor twee waardevolle doelen: een gemuteerde vorm van het EGFR‑eiwit dat betrokken is bij geneesmiddelresistente longkanker, en de hoofdprotease van SARS‑CoV‑2, het virus achter COVID‑19. Voor elk eiwit genereerde het systeem vele kandidaatmoleculen uitgerust met de geschikte warheads. Computerdockingsuggesties wezen erop dat CovaGEN’s ontwerpen waarschijnlijker posities innamen die covalente bindingen konden vormen dan verbindingen waarbij warheads eenvoudig op niet‑covalente ontwerpen waren bevestigd. Verschillende topkandidaten matchten of overtroffen referentiegeneesmiddelen op gecombineerde maatstaven van voorspelde binding, drug‑likeness en synthetische eenvoud.
Wat dit betekent voor toekomstige medicijnen
CovaGEN laat zien dat moderne generatieve AI meer kan dan alleen moleculen bedenken die strak aan eiwitten kleven. Door te werken in een ruimte van van nature medicijnachtige structuren, het sturen van de toevoeging van reactieve groepen en het expliciet wegleiden van toxiciteit, brengt het systeem de ontdekking van covalente geneesmiddelen naar een meer holistisch en geautomatiseerd proces. Hoewel verder laboratoriumonderzoek nodig is om te bevestigen hoe deze virtuele moleculen zich in levende systemen gedragen, opent de aanpak een pad naar snellere, bredere verkenning van covalente middelen die niet alleen potent zijn maar ook veiliger voor patiënten.
Bronvermelding: Zhang, W., Liu, T., Dong, X. et al. De novo covalent drug generation with enhanced drug-likeness and safety. Commun Biol 9, 446 (2026). https://doi.org/10.1038/s42003-026-09725-5
Trefwoorden: covalente geneesmiddelen, generatieve AI, geneesmiddelontdekking, diffusiemodellen, toxicity prediction