Clear Sky Science · pl
De novo kowalencyjne projektowanie leków z ulepszoną zgodnością z kryteriami lekopodobności i bezpieczeństwem
Dlaczego mądrzejsze leki kowalencyjne mają znaczenie
Terapie przeciwnowotworowe i leki przeciwwirusowe często działają przez przyłączanie się do białek wewnątrz komórek. Potężna klasa leków, określana jako leki kowalencyjne, idzie krok dalej: tworzą silne, długotrwałe wiązania ze swoimi celami, co może czynić je bardzo skutecznymi. Jednak ta sama „przyczepność" może powodować poważne skutki uboczne, jeśli związki wiążą się z niewłaściwymi białkami. W tym badaniu przedstawiono CovaGEN, nowy system sztucznej inteligencji zaprojektowany do tworzenia kandydatów na leki kowalencyjne od podstaw, przy jednoczesnym uwzględnieniu użyteczności i bezpieczeństwa.
Od prób i błędów do inteligentnego projektowania
Tradycyjne odkrywanie leków kowalencyjnych jest powolne i kosztowne. Chemicy albo zaczynają od istniejącego leku i doklejają reaktywną „rączkę”, albo startują od reaktywnego fragmentu i mozolnie dopracowują resztę cząsteczki. Metody wspomagane komputerowo ułatwiają pracę przez przeszukiwanie dużych bibliotek znanych związków, ale są ograniczone do tego, co już istnieje. Ostatnie postępy w uczeniu głębokim potrafią generować całkowicie nowe cząsteczki, jednak narzędzia te zwykle koncentrują się na konwencjonalnych, niekowalencyjnych lekach i często pomijają kluczowe cechy, takie jak łatwość syntezy, zgodność z właściwościami lekopodobnymi czy potencjalna toksyczność. CovaGEN ma na celu jednoczesne rozwiązanie wszystkich tych problemów.
Ukryta mapa chemii lekopodobnej
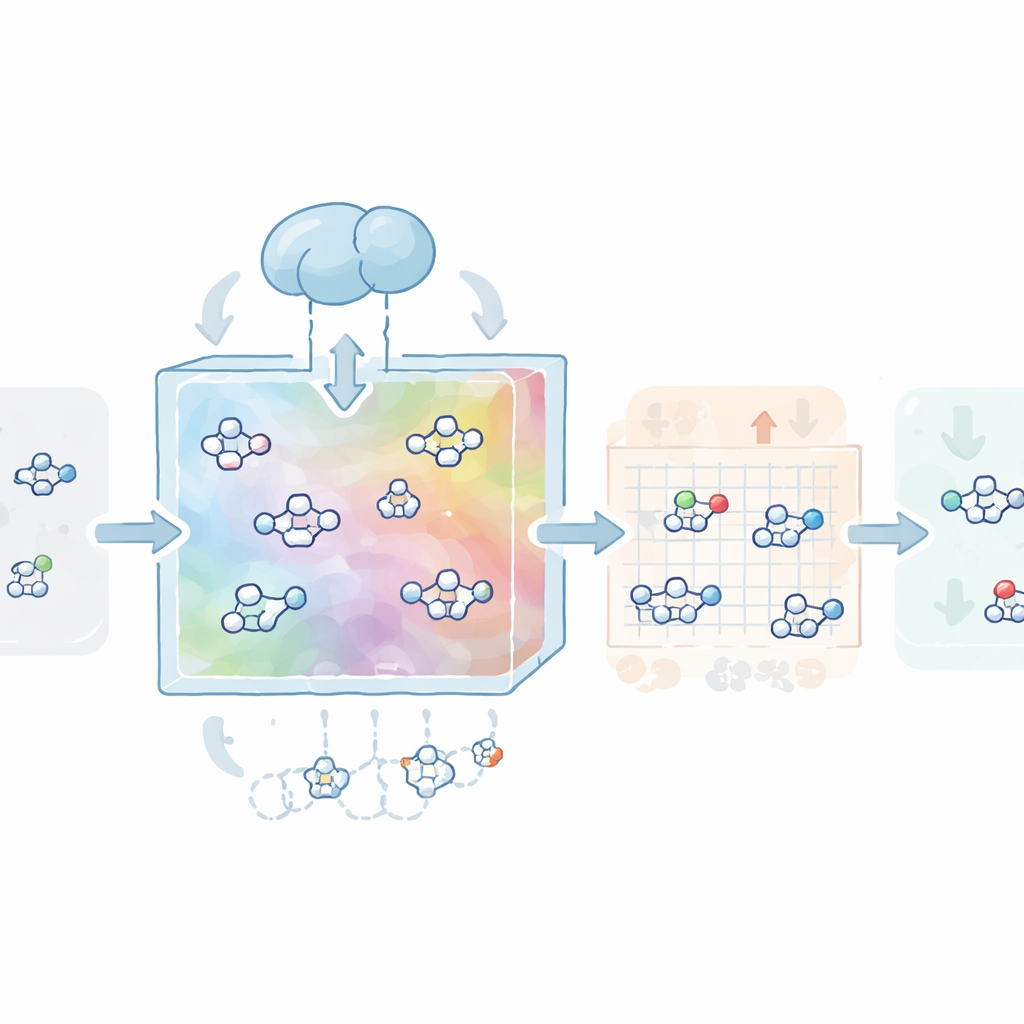
Autorzy najpierw zbudowali „mapę” przestrzeni chemicznej, wykorzystując ponad milion związków lekopodobnych z publicznej bazy ZINC. Wytrenowali sieć neuronową typu wariacyjnego autoenkodera, aby skompresować każdą cząsteczkę do zwartego kodu numerycznego, zwanego wektorem latentnym, a następnie ją odtworzyć. Ten krok uczy model podstawowej gramatyki chemii leków: co wygląda realistycznie, co respektuje powszechne reguły dla leków doustnych i co ma tendencję do bycia syntetycznie wykonalnym. Na tej wyuczonej mapie drugi model oparty na dyfuzji — procesie, który stopniowo zamienia strukturę w szum, a następnie uczy się odwracać ten proces — został przeszkolony do eksploracji i generowania nowych wektorów latentnych, które dekodują się w prawidłowe, zróżnicowane i realistyczne cząsteczki.
Dopasowywanie cząsteczek do białek i reaktywnych „haczyków”
Następnie CovaGEN uczy się projektować cząsteczki pod konkretne cele białkowe. System przyjmuje sekwencję aminokwasową białka i koduje ją za pomocą potężnego modelu językowego dla białek, który wychwytuje wzorce związane ze strukturą i funkcją. Podczas procesu dyfuzji model zwraca krzyżową uwagę na tę reprezentację białka, tak aby generowane cząsteczki miały predyspozycje do dopasowania się do miejsca wiążącego celu. W testach na dużym zbiorze benchmarkowym te ukierunkowane cząsteczki nie tylko uzyskiwały wysokie prognozy siły wiązania, lecz także wykazywały lepszą lekopodobność i dostępność syntetyczną niż związki pochodzące z kilku zaawansowanych narzędzi projektowania 3D. Aby przekształcić te niekowalencyjne wiążące się związki w kandydatów kowalencyjnych, zespół dodał klasyfikator, który delikatnie kieruje proces dyfuzji w stronę cząsteczek zawierających określone grupy reaktywne, znane jako „kowalencyjne narzędzia” (warheads), bez poświęcania ogólnej jakości.
Wbudowane bezpieczeństwo od samego początku
Ponieważ leki kowalencyjne mogą powodować trwałe szkody, jeśli trafią w niewłaściwe cele, bezpieczeństwo jest kluczowe. Badacze potraktowali więc toksyczność jako wielkość do optymalizacji, a nie dodatek. Wytrenowali modele predykcyjne ostrej toksyczności i ryzyk związanych z określonymi narządami, a następnie zastosowali uczenie ze wzmocnieniem, aby dopracować model dyfuzji tak, by preferował cząsteczki o niższej przewidywanej toksyczności. Po tym treningu CovaGEN generował związki, które zachowywały dobre właściwości wiążące i lekopodobne, lecz miały mniejsze prawdopodobieństwo zawierania strukturalnych „czerwonych flag” związanych ze szkodliwymi efektami. Co istotne, metoda osiągnęła to bez kurczenia się do wąskiego zestawu podobnych cząsteczek, zachowując różnorodność chemiczną.
Próba metody w praktyce
Aby wykazać potencjał w świecie rzeczywistym, zespół poprosił CovaGEN o zaprojektowanie inhibitorów kowalencyjnych dla dwóch istotnych celów: mutantowej formy białka EGFR związanej z opornością na leki w raku płuca oraz głównej proteazy SARS‑CoV‑2, wirusa wywołującego COVID‑19. Dla każdego białka system wygenerował wiele kandydatów wyposażonych w odpowiednie warheads. Badania dokowania komputerowego sugerowały, że projekty CovaGEN częściej przyjmowały pozy umożliwiające tworzenie wiązań kowalencyjnych niż związki, którym warheady były jedynie doklejone do niekowalencyjnych projektów. Kilka czołowych kandydatów dorównywało lub przewyższało leki referencyjne pod względem łączonych miar przewidywanego wiązania, lekopodobności i łatwości syntezy.
Co to oznacza dla przyszłych leków
CovaGEN pokazuje, że nowoczesna generatywna SI potrafi zrobić więcej niż wyobrazić sobie cząsteczki mocno wiążące się z białkami. Pracując w przestrzeni z natury lekopodobnych struktur, prowadząc dodawanie grup reaktywnych i jawnie odchodząc od toksyczności, system przesuwa odkrywanie leków kowalencyjnych w stronę procesu bardziej holistycznego i zautomatyzowanego. Chociaż konieczne są dalsze testy laboratoryjne, by potwierdzić, jak te wirtualne cząsteczki zachowują się w układach biologicznych, podejście otwiera drogę do szybszego i szerszego badania leków kowalencyjnych, które są nie tylko silne, ale też bezpieczniejsze dla pacjentów.
Cytowanie: Zhang, W., Liu, T., Dong, X. et al. De novo covalent drug generation with enhanced drug-likeness and safety. Commun Biol 9, 446 (2026). https://doi.org/10.1038/s42003-026-09725-5
Słowa kluczowe: leki kowalencyjne, generatywna SI, poszukiwanie leków, modele dyfuzji, predykcja toksyczności