Clear Sky Science · ar
توليد أدوية تساهمية جديدة مع تحسين خصائص الشبيه بالدواء والسلامة
لماذا تهم الأدوية التساهمية الأذكى
تعتمد علاجات السرطان والأدوية المضادة للفيروسات غالبًا على الارتباط بالبروتينات داخل خلايانا. فئة قوية من الأدوية، تُسمى الأدوية التساهمية، تتجاوز ذلك: فهي تُشكّل روابط قوية وطويلة الأمد مع أهدافها، ما قد يجعلها فعّالة للغاية. لكن تلك القابلية للالتصاق قد تسبب أيضًا آثارًا جانبية خطيرة إذا ارتبطت الأدوية ببروتينات خاطئة. تُقدّم هذه الدراسة CovaGEN، نظامًا جديدًا للذكاء الاصطناعي مصممًا لاختراع مرشحين للأدوية التساهمية من الصفر مع مراعاة كل من الفعالية والسلامة.
من التجربة والخطأ إلى التصميم الذكي
إن اكتشاف الأدوية التساهمية التقليدي بطيء ومكلف. يبدأ الكيميائيون إما بدواء موجود ويضيفون إليه «مقبضًا» تفاعليًا، أو يبدأون بجزء تفاعلي ويعدّلون بقيّة الجزيء بدقة. تساعد الطرق المحوسبة من خلال فحص مكتبات كبيرة من المركبات المعروفة، لكنها محدودة بما هو موجود مسبقًا. يمكن للتقدّم في التعلم العميق أن يولّد جزيئات جديدة بالكامل، إلا أن هذه الأدوات عادةً ما تركز على الأدوية غير التساهمية وتتجاهل سمات حاسمة مثل سهولة التصنيع، والسلوك كدواء حقيقي، أو مدى السمية المحتملة. يهدف CovaGEN إلى معالجة كل هذه القضايا معًا.
خريطة خفيّة للكيمياء الشبيهة بالدواء
بنى المؤلفون أولًا «خريطة» للمساحة الكيميائية باستخدام أكثر من مليون جزيء شبيه بالدواء من قاعدة بيانات ZINC العامة. درّبوا نوعًا من الشبكات العصبية يُعرف بالمشفر التبايني التلقائي (variational autoencoder) لضغط كل جزيء إلى رمز عددي مُدمج أو متجه كامن، ثم إعادة بنائه. تعلم النموذج من خلال هذه الخطوة قواعد اللغة الأساسية للكيمياء الدوائية: ما يبدو واقعيًا، وما يحترم قواعد الأدوية الفموية الشائعة، وما يميل لأن يكون قابلًا للتصنيع. على هذه الخريطة المتعلمة، دُرّب نموذج ثانٍ قائم على الانتشار—عملية تحول البنية تدريجيًا إلى ضوضاء ثم يتعلم عكس تلك العملية—للتجوّل وتوليد متجهات كامنة جديدة تُفكّ شيفرتها إلى جزيئات صالحة، متنوعة، وواقعية.
ضبط الجزيئات لتلائم البروتينات والخطافات التفاعلية
بعد ذلك، يتعلّم CovaGEN تصميم جزيئات لأهداف بروتينية محددة. يأخذ النظام تسلسل الأحماض الأمينية للبروتين ويشفّره بنموذج لغوي قوي للبروتينات، ما يلتقط أنماطًا متعلقة بالبنية والوظيفة. خلال عملية الانتشار، يولي النموذج اهتمامًا متقاطعًا لهذا التمثيل البروتيني بحيث تميل الجزيئات التي يولّدها إلى التناسب مع موقع الارتباط في الهدف. في اختبارات على مجموعة مرجعية كبيرة، لم تكن هذه الجزيئات المصمّمة مناسبة فقط من حيث قوة الارتباط المتوقعة، بل أظهرت أيضًا شبهاً بالدواء وسهولة تصنيع أفضل من تلك الناتجة عن عدة أدوات تصميم ثلاثية الأبعاد متقدمة. لتحويل هؤلاء الرابِطين غير التساهميين إلى مرشحين تساهميين، أضاف الفريق مصنّفًا يوجّه عملية الانتشار نحو جزيئات تحمل مجموعات تفاعلية معينة، تُعرف بالرؤوس الحربية التساهمية، دون التضحية بالجودة العامة.
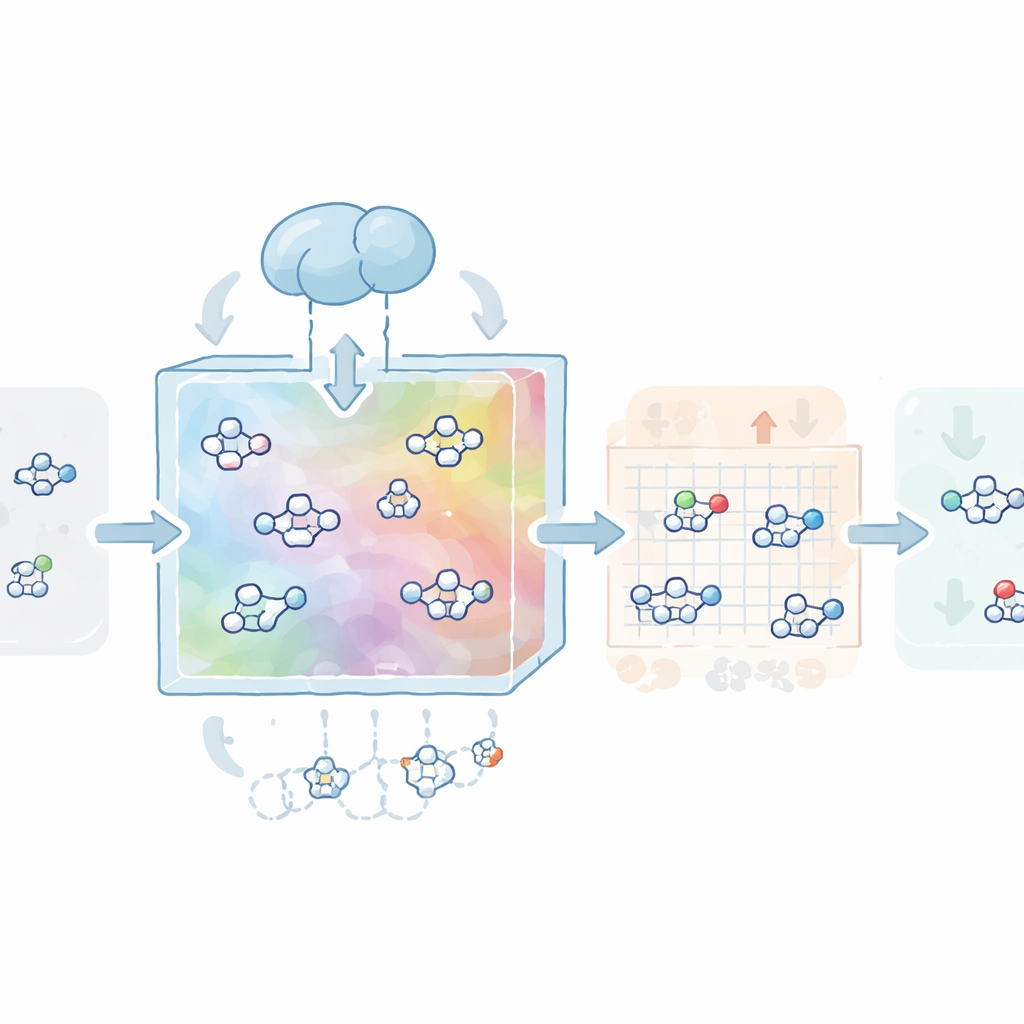
بناء السلامة منذ البداية
بما أن الأدوية التساهمية قد تسبب ضررًا دائمًا إن أصابت أهدافًا خاطئة، تكون السلامة مسألة مركزية. لذلك تعامل الباحثون مع السمية ككمية يجب تحسينها، لا كملاحظة لاحقة. درّبوا نماذج تنبؤية للسمية الحادة ومخاطر متعلقة بأعضاء معينة، ثم طبقوا التعلم المعزز لضبط نموذج الانتشار بحيث يُفضّل الجزيئات ذات السمية المتوقعة الأدنى. بعد هذا التدريب، ولّد CovaGEN مركبات حافظت على ارتباط جيد وخصائص شبيهة بالدواء لكنها كانت أقل احتمالًا لاحتواء «أعلام حمراء» تركيبية مرتبطة بتأثيرات ضارة. ومن المهم أن الطريقة حققت ذلك من دون الانهيار إلى مجموعة ضيقة من الجزيئات المتشابهة، محافظةً على التنوع الكيميائي.
وضع الطريقة قيد الاختبار
لإظهار الإمكانات الواقعية، طلب الفريق من CovaGEN تصميم مثبطات تساهمية لهدفين ذوي قيمة عالية: شكل طفري من بروتين EGFR المتورط في سرطان الرئة المقاوم للأدوية، والبروتياز الرئيسي لـ SARS‑CoV‑2، الفيروس المسبب لكوفيد‑19. لكل بروتين، ولّد النظام العديد من المرشحين المجهزين بالرؤوس الحربية المناسبة. أشارت دراسات التأثير الحاسوبي إلى أن تصاميم CovaGEN كانت أكثر احتمالًا لتبني أوضاع قادرة على تشكيل روابط تساهمية مقارنةً بالمركبات التي أُضيفت إليها الرؤوس الحربية ببساطة على تصميمات غير تساهمية. كما أن عددًا من أفضل المرشحين طابق أو تفوّق على الأدوية المرجعية في مقاييس مشتركة لتنبؤ الارتباط، والشبيه بالدواء، وسهولة التصنيع.
ماذا يعني هذا لأدوية المستقبل
يُظهر CovaGEN أن الذكاء الاصطناعي التوليدي الحديث يمكنه أن يفعل أكثر من تخيل جزيئات تلتصق بقوة بالبروتينات. من خلال العمل في فضاء يتسم جوهريًا بالشبه بالدواء، وتوجيه إضافة المجموعات التفاعلية، والمضي صراحةً بعيدًا عن السمية، يتقدّم النظام باكتشاف الأدوية التساهمية نحو عملية أكثر شمولية وتلقائية. وبينما يلزم مزيد من الاختبارات المخبرية لتأكيد سلوك هذه الجزيئات الافتراضية في النظم الحية، يفتح النهج طريقًا لاستكشاف أسرع وأوسع للأدوية التساهمية التي ليست قوية فحسب بل أكثر أمانًا للمرضى.
الاستشهاد: Zhang, W., Liu, T., Dong, X. et al. De novo covalent drug generation with enhanced drug-likeness and safety. Commun Biol 9, 446 (2026). https://doi.org/10.1038/s42003-026-09725-5
الكلمات المفتاحية: الأدوية التساهمية, الذكاء الاصطناعي التوليدي, اكتشاف الأدوية, نماذج الانتشار, تنبؤ السمية