Clear Sky Science · pt
Purificação, caracterização e propriedades de despelamento de queratinase alcalina e termoestável produzida por Penicillium citrinum AUMC 14742
Transformando penas residuais em produtos úteis
As granjas modernas geram montanhas de penas e outros resíduos coriáceos semelhantes a pelos, que são difíceis de degradar e frequentemente acabam incinerados ou descartados. Este estudo mostra como um fungo naturalmente existente pode produzir uma enzima poderosa que converte esse resíduo persistente em algo valioso, ao mesmo tempo que oferece uma maneira mais limpa de remover pelos de peles animais na indústria do couro.
Por que as penas são tão difíceis de tratar
Penas, lã e pelos animais são formados por queratina, uma proteína organizada como cordas fortemente trançadas reforçadas por muitas “pontes” químicas. Esse arranjo torna as penas leves, resistentes e quase indestrutíveis, mas também faz com que resistam à decomposição comum e à maioria das enzimas proteolíticas usuais. Como resultado, resíduos ricos em queratina se acumulam em fazendas e curtumes, gerando poluição e desperdiçando uma fonte potencialmente valiosa de nutrientes e matérias‑primas que poderiam ser usadas para ração animal, fertilizantes ou produtos especializados.
Um fungo útil entra em cena
Os pesquisadores focaram em uma linhagem do fungo Penicillium citrinum, coletada e identificada com precisão. Essa linhagem produz queratinase, uma enzima especialmente capaz de atacar a estrutura resistente da queratina. Usando uma abordagem estatística de otimização chamada delineamento Box–Behnken, a equipe ajustou sistematicamente a temperatura de crescimento, a acidez (pH) e a quantidade de peptona adicionada, um nutriente rico em nitrogênio. Descobriram que uma temperatura relativamente baixa de 26 °C, condições levemente alcalinas (pH 8) e uma baixa concentração de peptona proporcionavam a maior produção enzimática. Nessas condições, o fungo produziu uma queratinase com atividade impressionante, que foi então cuidadosamente purificada e demonstrada como uma única proteína bem definida.
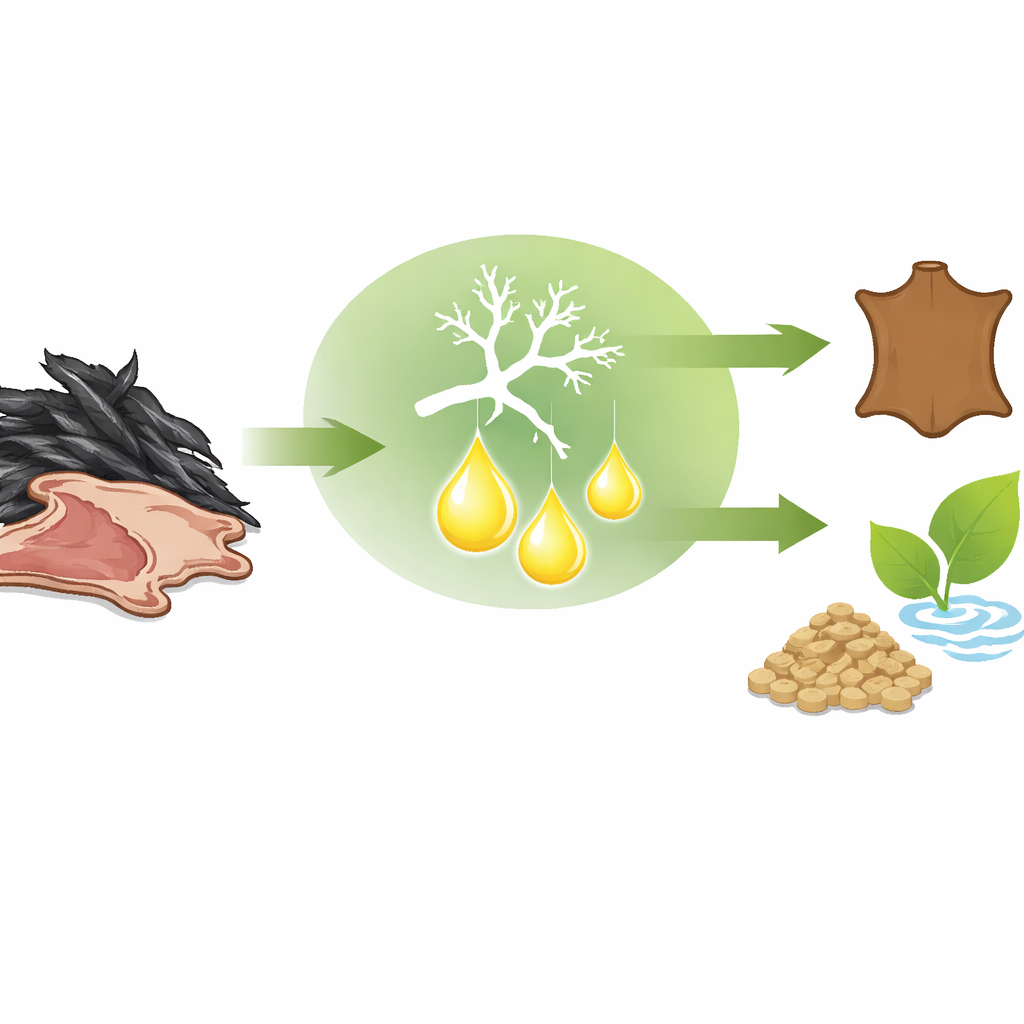
Uma enzima feita para trabalhos severos
Uma vez purificada, a queratinase revelou um conjunto de características que a tornam especialmente promissora para uso industrial. Ela é mais ativa em pH fortemente alcalino (pH 10) e em temperatura moderadamente elevada (55 °C), mostrando que pode permanecer ativa onde muitas outras proteínas se desnaturariam. Testes com vários sais, detergentes e solventes mostraram que a enzima é notavelmente resistente a condições semelhantes às encontradas em produtos de limpeza e em banhos de processamento. Certos íons metálicos e aditivos, e especialmente um agente redutor que ajuda a abrir as pontes internas da queratina, aumentaram sua atividade de forma dramática. A enzima também apresentou alta eficiência catalítica, o que significa que pode processar queratina rapidamente uma vez que a encontra.
Do banco de laboratório à sapataria de couro
Para verificar se essas propriedades favoráveis se traduzem em desempenho no mundo real, a equipe testou a mistura enzimática bruta em peles de cabra. Em vez de usar produtos químicos agressivos e odoríferos normalmente empregados para remoção de pelos, eles simplesmente imergiram as peles na solução de queratinase a 30 °C. Em até 15 horas, os pelos se soltaram completamente, deixando a pele lisa e flexível sem danos visíveis. Esse despelamento suave, porém eficaz, demonstra que a enzima pode realizar o mesmo trabalho que os produtos químicos tradicionais, mas em condições mais brandas e com muito menos impactos ambientais.
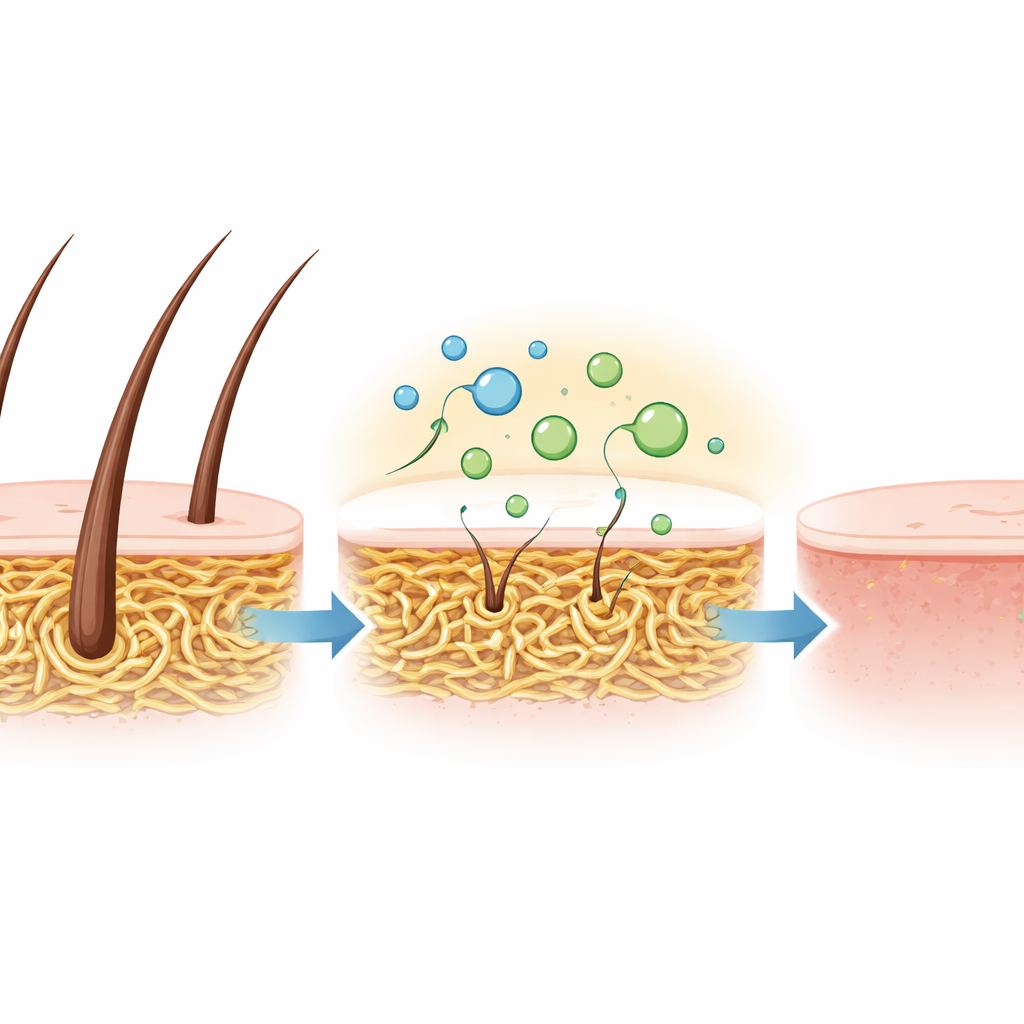
Um caminho mais verde para resíduos proteicos resistentes
Em termos simples, este trabalho revela uma enzima produzida por fungo que é incomumente resistente em ambientes alcalinos e quentes, tolera detergentes e solventes, e pode degradar queratina de forma eficiente. Essa combinação a torna uma ferramenta potente para transformar resíduos teimosos de penas e pelos em produtos úteis e para substituir produtos químicos tóxicos no processamento do couro. Para o leitor, a conclusão é que aquilo que hoje tratamos como um fluxo de resíduos problemático poderia se tornar um recurso valioso, graças a um parceiro microscópico e suas tesouras moleculares bem ajustadas.
Citação: Al-Bedak, O.A.M., Abdel-Latif, A.M.A., Abo-Dahab, N.F. et al. Purification, characterization, and dehairing properties of alkaline and thermo-stable keratinase by Penicillium citrinum AUMC 14742. Sci Rep 16, 13025 (2026). https://doi.org/10.1038/s41598-026-48471-w
Palavras-chave: queratinase, resíduo de penas de aves, enzimas fúngicas, processamento de couro ecologicamente correto, bioconversão