Clear Sky Science · de
Reinigung, Charakterisierung und Enthaarungseigenschaften einer alkalischen und thermo-stabilen Keratinase von Penicillium citrinum AUMC 14742
Aus Abfallfedern nützliche Produkte machen
Moderne Geflügelfarmen produzieren Berge von Federn und anderen zähen, haarähnlichen Resten, die schwer abzubauen sind und oft verbrannt oder deponiert werden. Diese Studie zeigt, wie ein natürlich vorkommender Pilz ein wirkungsvolles Enzym herstellen kann, das diesen hartnäckigen Abfall in etwas Wertvolles verwandelt und zugleich eine sauberere Methode bietet, Haare bei Tierhäuten in der Lederindustrie zu entfernen.
Warum Federn so schwer zu behandeln sind
Federn, Wolle und Tierhaare bestehen aus Keratin, einem Protein, das wie fest verknotete Seile aufgebaut ist und durch zahlreiche chemische „Brücken“ verstärkt wird. Diese Konstruktion macht Federn leicht, stabil und nahezu unzerstörbar, sorgt aber auch dafür, dass sie der normalen Verwesung und den meisten üblichen proteinhaltigen Abbauenzymen widerstehen. Infolgedessen häufen sich keratinreiche Abfälle auf Farmen und in Gerbereien, was zu Umweltproblemen führt und eine potenziell wertvolle Quelle für Nährstoffe und Rohstoffe verschwendet, die etwa in Tierfutter, Dünger oder Spezialprodukten genutzt werden könnten.
Ein hilfreicher Pilz kommt ins Spiel
Die Forschenden konzentrierten sich auf einen Stamm des Pilzes Penicillium citrinum, der ursprünglich isoliert und detailliert charakterisiert wurde, um seine Identität zu bestätigen. Dieser Stamm produziert Keratinase, ein Enzym, das speziell darauf zugeschnitten ist, die robuste Struktur des Keratins anzugreifen. Mithilfe eines statistischen Optimierungsansatzes, des Box–Behnken-Designs, passte das Team systematisch Wachstumstemperatur, Säuregrad (pH) und die Menge an zugegebenem Pepton, einem stickstoffreichen Nährstoff, an. Sie fanden heraus, dass eine relativ niedrige Temperatur von 26 °C, mild alkalische Bedingungen (pH 8) und eine geringe Peptonkonzentration die höchste Enzymausbeute lieferten. Unter diesen Bedingungen produzierte der Pilz eine beeindruckend aktive Keratinase, die anschließend sorgfältig gereinigt und als ein einzelnes, klar definiertes Protein nachgewiesen wurde.
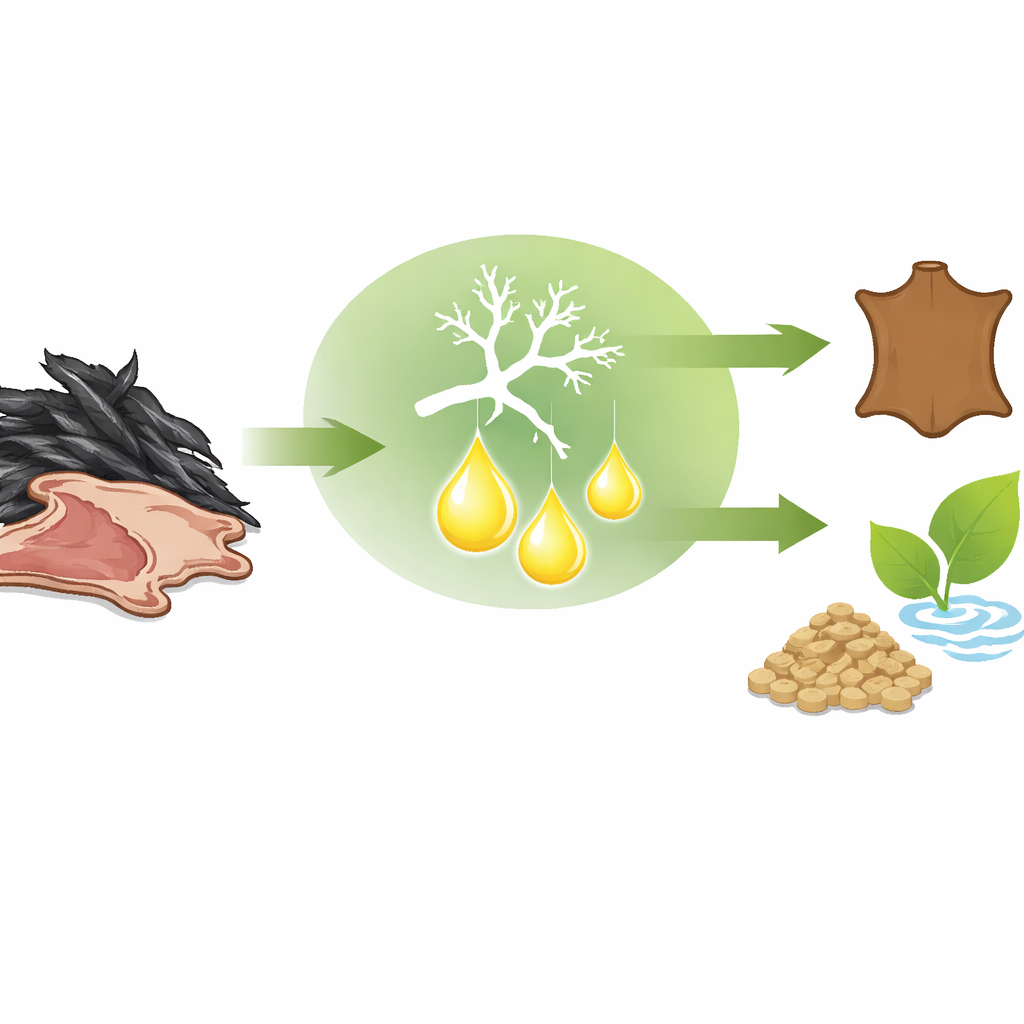
Ein Enzym für harte Einsätze
Nach der Reinigung zeigte die Keratinase Eigenschaften, die sie besonders vielversprechend für den industriellen Einsatz machen. Sie arbeitet am besten bei stark alkalischem pH 10 und einer moderat hohen Temperatur von 55 °C, was zeigt, dass sie unter Bedingungen aktiv bleibt, bei denen viele andere Proteine denaturieren würden. Tests mit verschiedenen Salzen, Tensiden und Lösungsmitteln ergaben, dass das Enzym bemerkenswert tolerant gegenüber Bedingungen ist, wie sie in Reinigungsprodukten und Verarbeitungsbädern vorkommen. Bestimmte Metallionen und Zusatzstoffe und besonders ein reduzierendes Mittel, das hilft, die inneren Brücken des Keratins zu öffnen, steigerten die Aktivität deutlich. Das Enzym zeigte außerdem eine hohe katalytische Effizienz, was bedeutet, dass es Keratin schnell verarbeiten kann, sobald es auf dieses trifft.
Vom Labortisch in die Gerberei
Um zu prüfen, ob sich diese vorteilhaften Eigenschaften in der Praxis bewähren, testete das Team das rohe Enzymgemisch an Ziegenhäuten. Anstatt der üblichen aggressiven, geruchsintensiven Chemikalien zur Haarentfernung wurden die Häute einfach bei 30 °C in die Keratinase-Lösung eingelegt. Innerhalb von 15 Stunden löste sich das Haar vollständig, und es blieb eine glatte, flexible Haut ohne sichtbare Schäden zurück. Diese schonende, aber effektive Enthaarung zeigt, dass das Enzym die gleiche Aufgabe wie traditionelle Chemikalien erfüllen kann, jedoch unter milderen Bedingungen und mit deutlich geringeren Umweltauswirkungen.
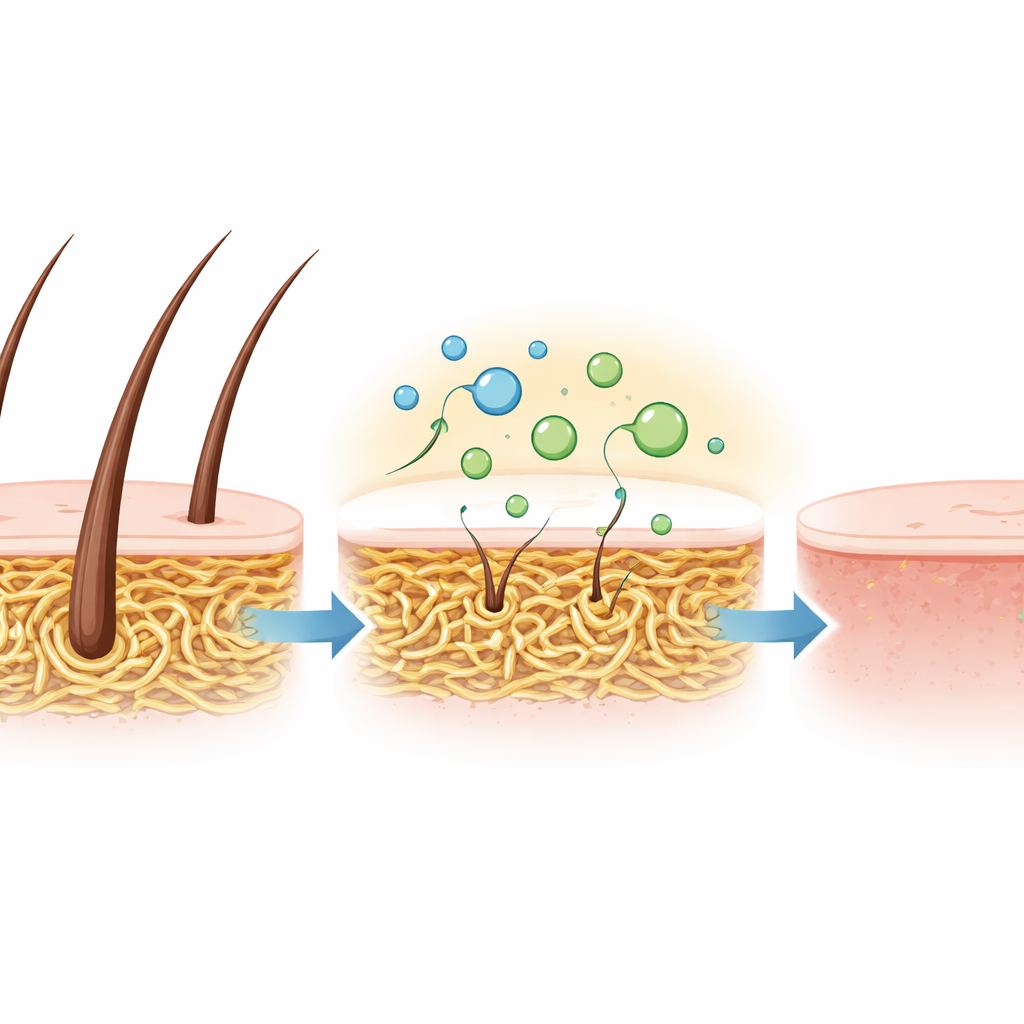
Ein grünerer Weg für zähe Proteinabfälle
Kurz gesagt, diese Arbeit stellt ein vom Pilz produziertes Enzym vor, das ungewöhnlich stabil in alkalischen und warmen Umgebungen ist, Tenside und Lösungsmittel verträgt und Keratin effizient aufspalten kann. Diese Kombination macht es zu einem wirksamen Werkzeug, um hartnäckige Feder- und Haarabfälle in nützliche Produkte zu verwandeln und giftige Chemikalien in der Lederverarbeitung zu ersetzen. Für die Leserschaft lautet die Quintessenz, dass das, was wir heute als lästigen Abfallstrom betrachten, dank eines mikroskopischen Partners und seiner fein abgestimmten molekularen Schere zu einer wertvollen Ressource werden könnte.
Zitation: Al-Bedak, O.A.M., Abdel-Latif, A.M.A., Abo-Dahab, N.F. et al. Purification, characterization, and dehairing properties of alkaline and thermo-stable keratinase by Penicillium citrinum AUMC 14742. Sci Rep 16, 13025 (2026). https://doi.org/10.1038/s41598-026-48471-w
Schlüsselwörter: Keratinase, Geflügelfederabfälle, pilzliche Enzyme, umweltfreundliche Lederverarbeitung, Biokonversion