Clear Sky Science · pl
Oczyszczanie, charakterystyka i właściwości odkrzewiające alkalicznej i termostabilnej keratynazy z Penicillium citrinum AUMC 14742
Przekształcanie odpadów piór w użyteczne produkty
Nowoczesne fermy drobiu wytwarzają góry piór i innych odpornych, włóknistych resztek, które trudno rozłożyć i często są spalane lub składowane. W badaniu pokazano, jak naturalnie występujący grzyb może wytwarzać silny enzym, który zamienia ten uporczywy odpad w coś wartościowego, a jednocześnie oferuje czystszy sposób usuwania włosów z wyprawianych skór w przemyśle garbarskim.
Dlaczego pióra są tak trudne do obróbki
Pióra, wełna i włosie zwierząt zbudowane są z keratyny — białka ułożonego jak mocno związane liny, wzmocnione wieloma chemicznymi „mostkami”. Ta konstrukcja czyni pióra lekkimi, wytrzymałymi i niemal niezniszczalnymi, ale też sprawia, że opierają się zwykłemu rozkładowi i większości powszechnych enzymów rozcinających białka. W efekcie odpady bogate w keratynę nagromadzają się wokół ferm i garbarni, powodując zanieczyszczenia i marnując potencjalnie wartościowe źródło składników odżywczych i surowców, które mogłyby trafić do pasz, nawozów lub produktów specjalistycznych.
Pomocny grzyb wkracza do akcji
Naukowcy skoncentrowali się na szczepie grzyba Penicillium citrinum, który został najpierw zebrany i dokładnie scharakteryzowany w celu potwierdzenia tożsamości. Szczep ten wytwarza keratynazę — enzym zaprojektowany do atakowania odpornej struktury keratyny. Wykorzystując statystyczne podejście optymalizacyjne zwane projektem Box–Behnken, zespół systematycznie dostosowywał temperaturę wzrostu, kwasowość (pH) i ilość dodanego peptonu, bogatego w azot składnika odżywczego. Odkryto, że stosunkowo niska temperatura 26 °C, łagodnie alkaliczne warunki (pH 8) oraz niskie stężenie peptonu dają najwyższy uzysk enzymu. W tych warunkach grzyb wytworzył imponująco aktywną keratynazę, którą następnie starannie oczyszczono i wykazano, że jest to pojedynczy, dobrze zdefiniowany białkowy enzym.
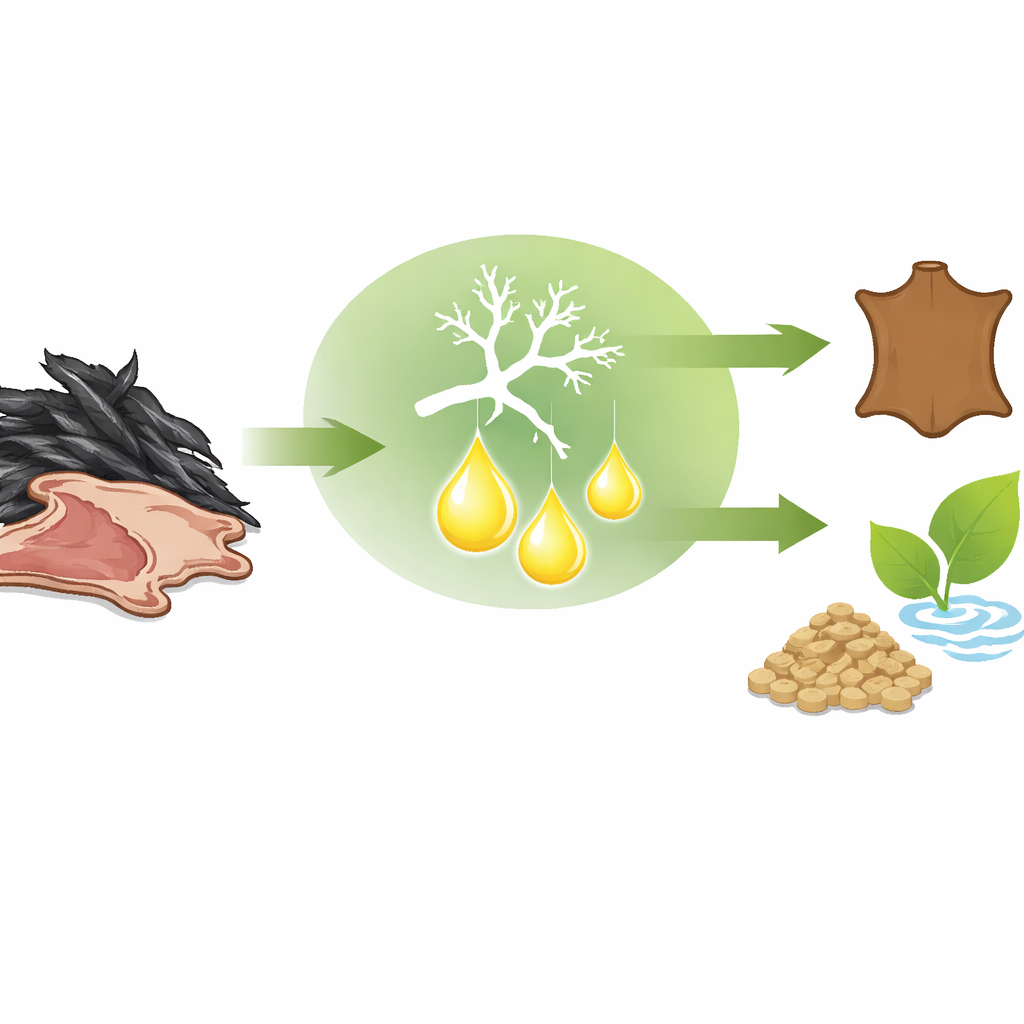
Enzym stworzony do trudnych zadań
Po oczyszczeniu keratynaza ujawniła zestaw cech czyniących ją szczególnie obiecującą do zastosowań przemysłowych. Najlepiej działa w silnie alkalicznym pH 10 i w umiarkowanie wysokiej temperaturze 55 °C, co pokazuje, że potrafi zachować aktywność tam, gdzie wiele innych białek ulega denaturacji. Badania z różnymi solami, detergentami i rozpuszczalnikami wykazały, że enzym wykazuje niezwykłą tolerancję na warunki podobne do tych występujących w środkach czyszczących i kąpielach procesowych. Niektóre jony metali i dodatki, a zwłaszcza związek redukujący, który pomaga rozrywać wewnętrzne mostki keratyny, znacząco zwiększały jego aktywność. Enzym wykazał też wysoką wydajność katalityczną, co oznacza, że potrafi szybko przetwarzać keratynę po jej napotkaniu.
Od stolika laboratoryjnego do garbarni
Aby sprawdzić, czy korzystne właściwości przekładają się na rzeczywiste zastosowania, zespół przetestował surową mieszaninę enzymatyczną na skórkach koziach. Zamiast używać ostrych, nieprzyjemnych chemikaliów zwykle stosowanych do usuwania włosów, po prostu zanurzono skóry w roztworze keratynazy w 30 °C. W ciągu 15 godzin włos zszedł całkowicie, pozostawiając gładką, elastyczną skórę bez widocznych uszkodzeń. To delikatne, a jednocześnie skuteczne odskarżanie dowodzi, że enzym może wykonać tę samą pracę co tradycyjne chemikalia, ale w łagodniejszych warunkach i z dużo mniejszym wpływem na środowisko.
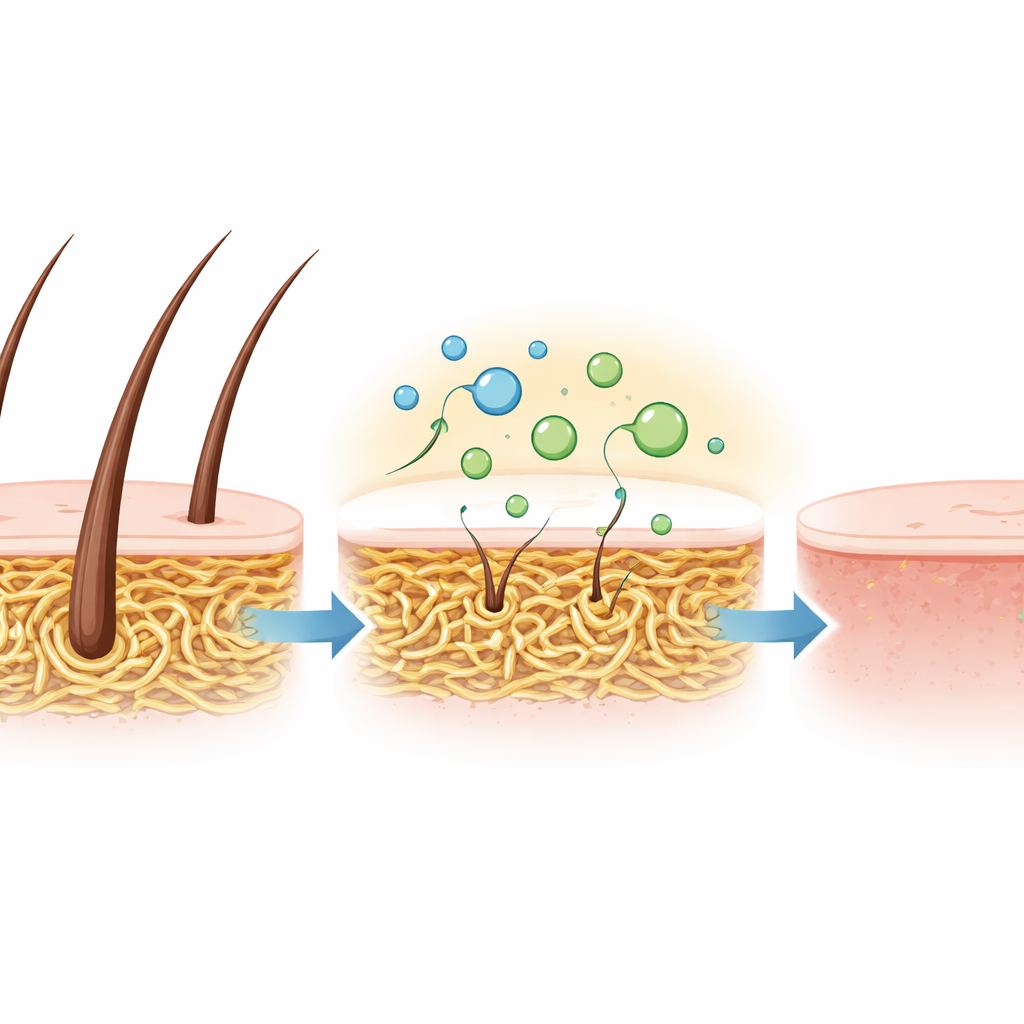
Bardziej ekologiczna ścieżka dla trudnych odpadów białkowych
Mówiąc prosto — praca ta ujawnia enzym wytwarzany przez grzyba, który jest wyjątkowo odporny w warunkach alkalicznych i podwyższonej temperaturze, znosi detergenty i rozpuszczalniki oraz skutecznie rozkłada keratynę. Taka kombinacja czyni go potężnym narzędziem do przekształcania uporczywych odpadów piór i włosów w użyteczne produkty oraz do zastępowania toksycznych chemikaliów w przetwarzaniu skór. Wniosek dla czytelników jest taki, że to, co obecnie traktujemy jako kłopotliwy strumień odpadów, dzięki mikroskopijnemu partnerowi i jego precyzyjnym molekularnym nożyczkom, może stać się cennym surowcem.
Cytowanie: Al-Bedak, O.A.M., Abdel-Latif, A.M.A., Abo-Dahab, N.F. et al. Purification, characterization, and dehairing properties of alkaline and thermo-stable keratinase by Penicillium citrinum AUMC 14742. Sci Rep 16, 13025 (2026). https://doi.org/10.1038/s41598-026-48471-w
Słowa kluczowe: keratynaza, odpady piór drobiowych, enzymy grzybowe, przyjazne dla środowiska przetwarzanie skór, biokonwersja