Clear Sky Science · it
Purificazione, caratterizzazione e proprietà di disoleamento della cheratinasi alcalina e termo-stabile prodotta da Penicillium citrinum AUMC 14742
Trasformare le piume di scarto in prodotti utili
Le moderne aziende avicole generano montagne di piume e altri residui coriacei simili a peli, difficili da degradare e spesso bruciati o scaricati. Questo studio mostra come un fungo naturalmente presente possa produrre un enzima potente che trasforma questo rifiuto ostinato in qualcosa di prezioso, offrendo al contempo un metodo più pulito per rimuovere il pelo dalle pelli animali nell’industria conciaria.
Perché le piume sono così difficili da trattare
Piume, lana e peli animali sono costituiti da cheratina, una proteina organizzata come corde strettamente annodate rinforzate da numerosi “ponti” chimici. Questa struttura rende le piume leggere, resistenti e quasi indistruttibili, ma significa anche che resistono alla degradazione ordinaria e alla maggior parte degli enzimi proteolitici comuni. Di conseguenza, i rifiuti ricchi di cheratina si accumulano attorno a allevamenti e concerie, creando inquinamento e sprecando una potenziale risorsa nutritiva e di materie prime che potrebbe essere impiegata per mangimi, fertilizzanti o prodotti speciali.
Un fungo utile entra in gioco
I ricercatori si sono concentrati su un ceppo del fungo Penicillium citrinum, raccolto e caratterizzato in dettaglio per confermarne l’identità. Questo ceppo produce cheratinasi, un enzima specificamente adatto ad attaccare la struttura tenace della cheratina. Utilizzando un approccio di ottimizzazione statistica noto come disegno di Box–Behnken, il gruppo ha regolato in modo sistematico la temperatura di crescita, l’acidità (pH) e la quantità di peptone aggiunta, un nutriente ricco di azoto. Hanno scoperto che una temperatura relativamente bassa di 26 °C, condizioni lievemente alcaline (pH 8) e una bassa concentrazione di peptone fornivano la massima produzione enzimatica. In tali condizioni il fungo ha prodotto una cheratinasi notevolmente attiva, che è stata poi purificata con cura e dimostrata essere una singola proteina ben definita.
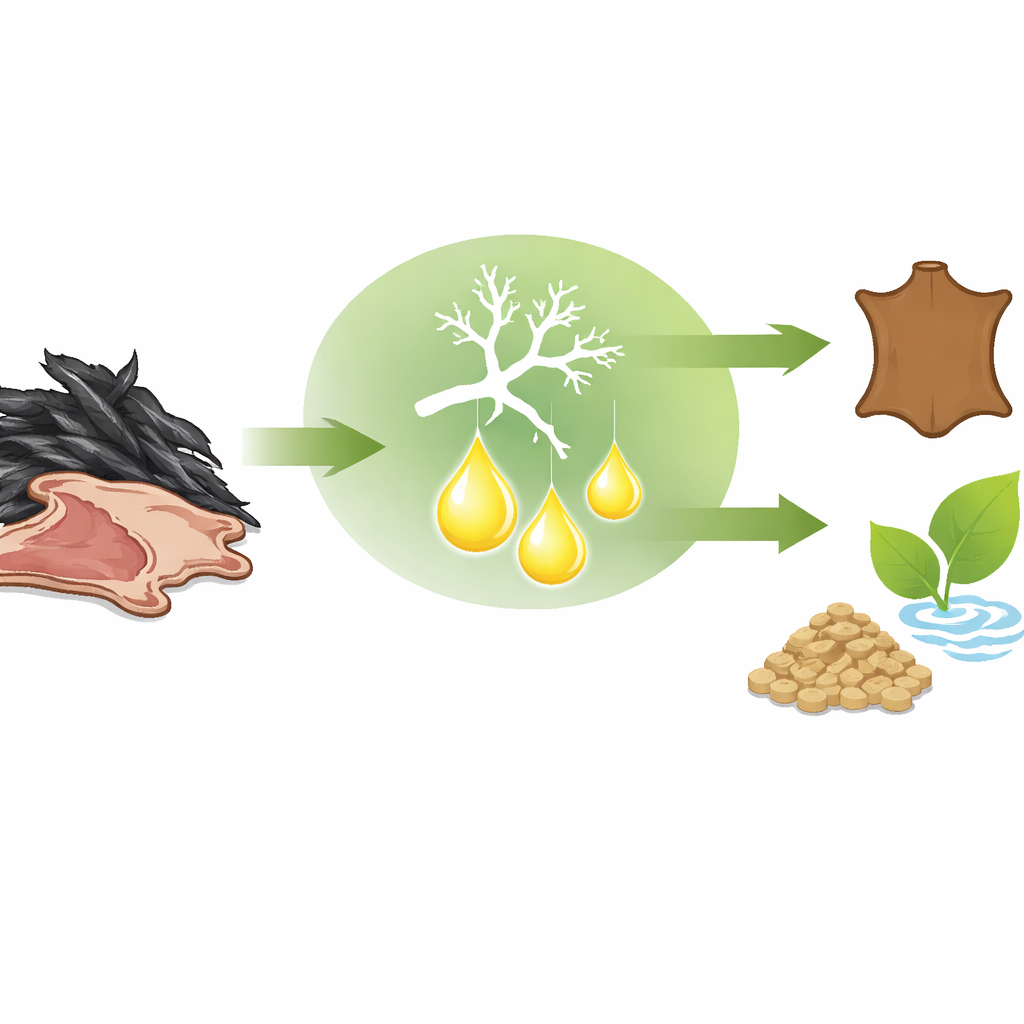
Un enzima progettato per lavori difficili
Una volta purificata, la cheratinasi ha mostrato un insieme di caratteristiche che la rendono particolarmente promettente per impieghi industriali. Funziona al meglio a un pH fortemente alcalino di 10 e a una temperatura moderatamente alta di 55 °C, dimostrando di restare attiva dove molte altre proteine si disattiverebbero. Test con vari sali, detergenti e solventi hanno mostrato che l’enzima è notevolmente tollerante a condizioni simili a quelle presenti in prodotti per la pulizia e bagni di lavorazione. Alcuni ioni metallici e additivi, e in particolare un agente riducente che aiuta ad aprire i ponti interni della cheratina, ne hanno aumentato drasticamente l’attività. L’enzima ha inoltre evidenziato un’elevata efficienza catalitica, il che significa che può processare la cheratina rapidamente quando la incontra.
Dal banco di laboratorio alla conceria
Per verificare se queste proprietà favorevoli si traducono in prestazioni reali, il team ha testato la miscela enzimatica grezza su pelli di capra. Invece di usare i prodotti chimici aggressivi e maleodoranti normalmente impiegati per rimuovere il pelo, hanno semplicemente immerso le pelli nella soluzione di cheratinasi a 30 °C. Nel giro di 15 ore il pelo si è staccato completamente, lasciando la pelle liscia e flessibile senza danni visibili. Questo disoleamento delicato ma efficace dimostra che l’enzima può svolgere lo stesso compito dei prodotti chimici tradizionali, ma in condizioni più miti e con molti meno impatti ambientali.
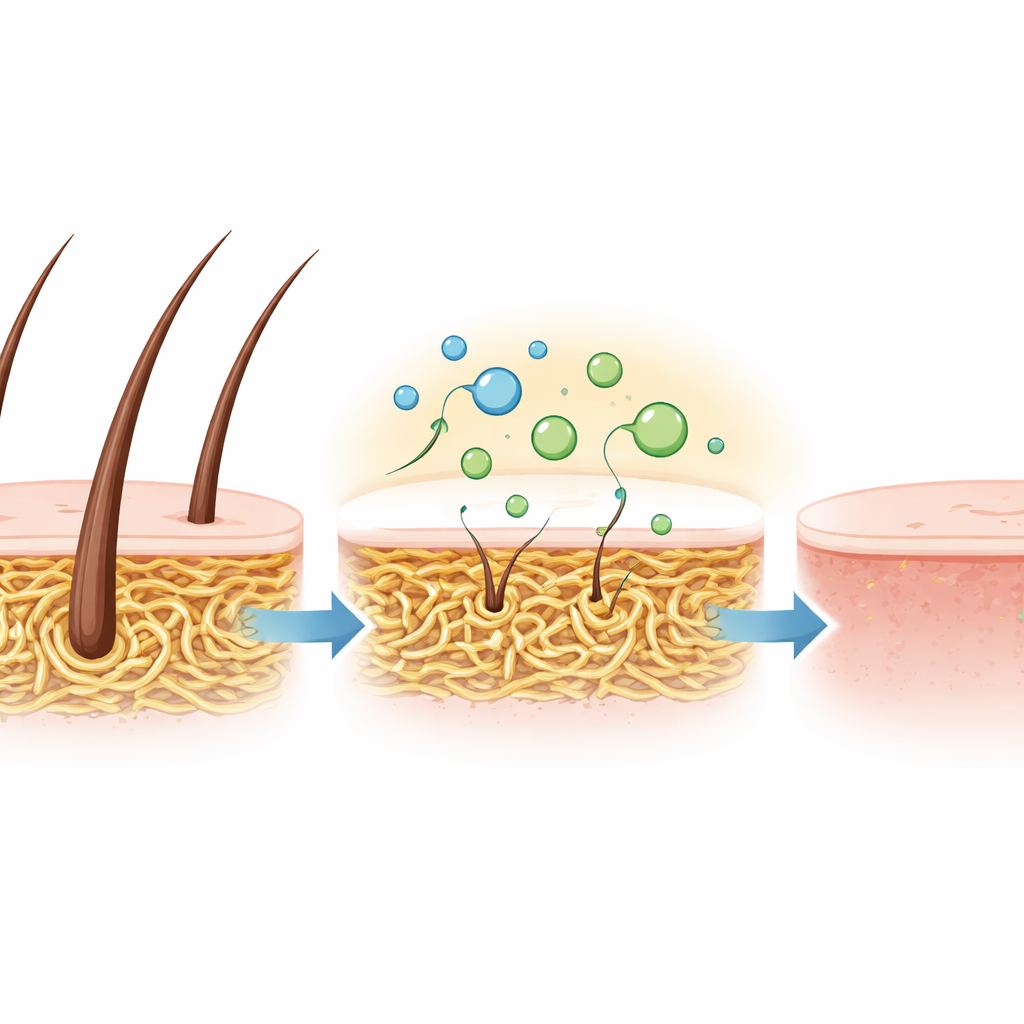
Un percorso più verde per i rifiuti proteici resistenti
In termini semplici, questo lavoro mette in luce un enzima prodotto da un fungo che è straordinariamente stabile in ambienti alcalini e caldi, resiste a detergenti e solventi e può demolire la cheratina in modo efficiente. Questa combinazione lo rende uno strumento potente per trasformare piume e peli resistenti in prodotti utili e per sostituire sostanze chimiche tossiche nella lavorazione delle pelli. Per il lettore, la conclusione è che ciò che oggi consideriamo un flusso di rifiuti problematico potrebbe diventare una risorsa preziosa, grazie a un alleato microscopico e alle sue forbici molecolari finemente tarate.
Citazione: Al-Bedak, O.A.M., Abdel-Latif, A.M.A., Abo-Dahab, N.F. et al. Purification, characterization, and dehairing properties of alkaline and thermo-stable keratinase by Penicillium citrinum AUMC 14742. Sci Rep 16, 13025 (2026). https://doi.org/10.1038/s41598-026-48471-w
Parole chiave: cheratinasi, scarti di piume avicole, enzimi fungini, lavorazione della pelle ecocompatibile, bioconversione