Clear Sky Science · fr
Purification, caractérisation et propriétés d’éclaircissement de poils d’une kératinase alcaline et thermo-stable produite par Penicillium citrinum AUMC 14742
Transformer les plumes de déchet en produits utiles
Les élevages de volaille modernes génèrent des montagnes de plumes et d’autres résidus fibreux difficiles à décomposer qui sont souvent brûlés ou mis en décharge. Cette étude montre comment un champignon naturellement présent peut produire une enzyme puissante qui transforme ces déchets tenaces en matière utile, tout en offrant une méthode plus propre pour enlever les poils des peaux animales dans l’industrie du cuir.
Pourquoi les plumes sont si difficiles à traiter
Les plumes, la laine et les poils d’animaux sont constitués de kératine, une protéine organisée comme des cordages fortement noués renforcés par de nombreux « ponts » chimiques. Cette architecture rend les plumes légères, résistantes et presque indestructibles, mais elle les rend aussi imperméables à la décomposition ordinaire et à la plupart des enzymes protéolytiques communes. En conséquence, les déchets riches en kératine s’accumulent autour des fermes et des tanneries, générant de la pollution et gaspillant une source potentiellement riche de nutriments et de matières premières pouvant servir pour l’alimentation animale, les engrais ou des produits de spécialité.
Un champignon utile entre en jeu
Les chercheurs se sont intéressés à une souche du champignon Penicillium citrinum, collectée et identifiée précisément. Cette souche produit une kératinase, une enzyme spécialement adaptée pour attaquer la structure robuste de la kératine. En utilisant une méthode d’optimisation statistique appelée plan Box–Behnken, l’équipe a ajusté systématiquement la température de croissance, l’acidité (pH) et la quantité de peptone ajoutée, une source d’azote riche. Ils ont découvert qu’une température relativement fraîche de 26 °C, des conditions légèrement alcalines (pH 8) et une faible concentration en peptone donnaient la production enzymatique la plus élevée. Dans ces conditions, le champignon a produit une kératinase d’activité impressionnante, qui a ensuite été purifiée et révélée comme une protéine unique et bien définie.
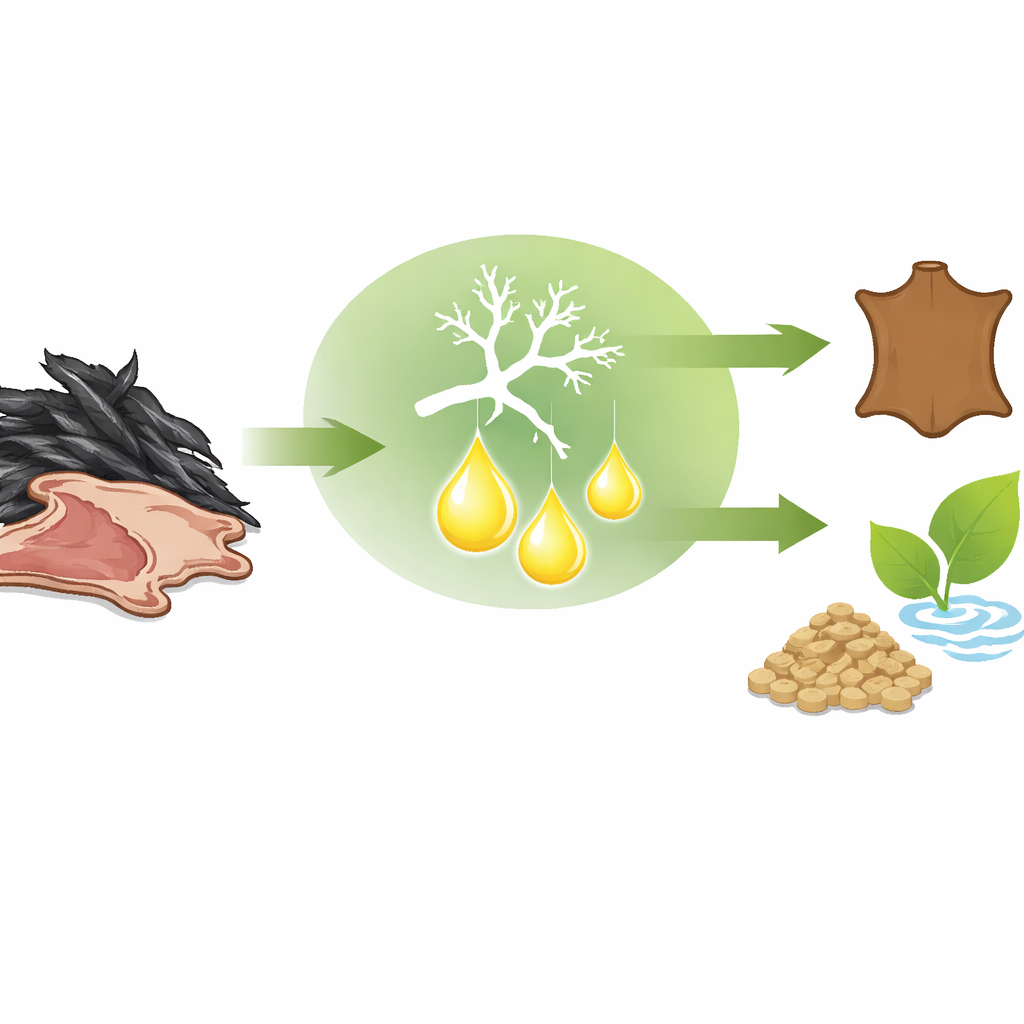
Une enzyme conçue pour les tâches difficiles
Une fois purifiée, la kératinase a présenté un ensemble de caractéristiques qui la rendent particulièrement prometteuse pour un usage industriel. Elle fonctionne de façon optimale en milieu fortement alcalin à pH 10 et à une température relativement élevée de 55 °C, ce qui montre qu’elle reste active là où beaucoup d’autres protéines se dégradent. Des tests avec divers sels, détergents et solvants ont montré que l’enzyme est remarquablement tolérante à des conditions similaires à celles rencontrées dans les produits de nettoyage et les bains de traitement. Certains ions métalliques et additifs, et en particulier un agent réducteur qui aide à ouvrir les ponts internes de la kératine, ont considérablement renforcé son activité. L’enzyme a également montré une grande efficacité catalytique, ce qui signifie qu’elle peut transformer la kératine rapidement une fois en présence du substrat.
Du banc de laboratoire à l’atelier de tannage
Pour vérifier si ces propriétés favorables se traduisent en performance réelle, l’équipe a testé le mélange enzymatique brut sur des peaux de chèvre. Au lieu d’utiliser des produits chimiques agressifs et odorants traditionnellement employés pour l’épilation, ils ont simplement trempé les peaux dans la solution de kératinase à 30 °C. En l’espace de 15 heures, les poils se sont détachés complètement, laissant une peau lisse et souple sans dommage visible. Cet épilation douce mais efficace montre que l’enzyme peut accomplir la même tâche que les produits chimiques traditionnels, mais dans des conditions plus douces et avec bien moins d’impacts environnementaux.
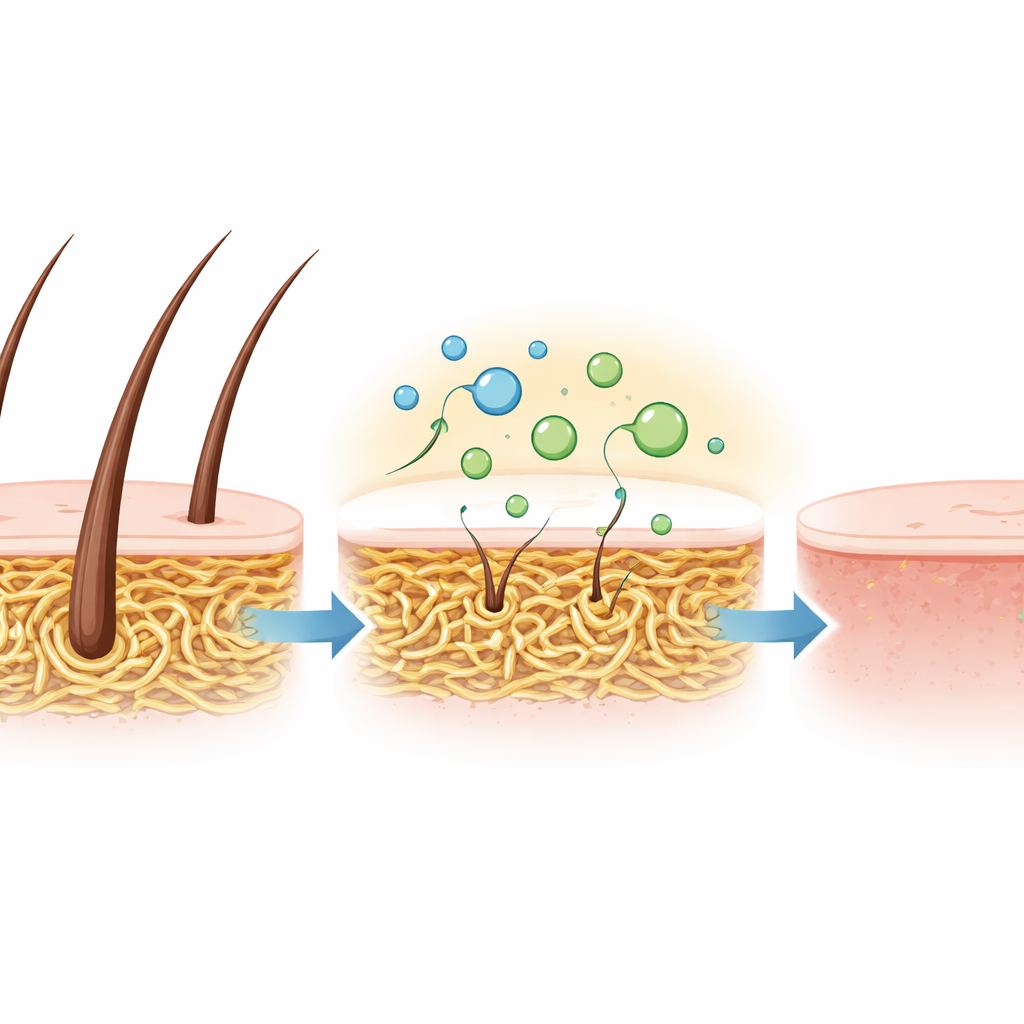
Une voie plus verte pour les déchets protéiques résistants
En termes simples, ce travail met en lumière une enzyme produite par un champignon qui est exceptionnellement robuste en milieu alcalin et chaud, résiste aux détergents et aux solvants, et peut dégrader efficacement la kératine. Cette combinaison en fait un outil puissant pour transformer les déchets tenaces de plumes et de poils en produits utiles et pour remplacer des produits chimiques toxiques dans le traitement du cuir. Pour le lecteur, la conclusion est que ce que nous considérons aujourd’hui comme un flux de déchets problématique pourrait devenir une ressource précieuse, grâce à un partenaire microscopique et ses ciseaux moléculaires finement ajustés.
Citation: Al-Bedak, O.A.M., Abdel-Latif, A.M.A., Abo-Dahab, N.F. et al. Purification, characterization, and dehairing properties of alkaline and thermo-stable keratinase by Penicillium citrinum AUMC 14742. Sci Rep 16, 13025 (2026). https://doi.org/10.1038/s41598-026-48471-w
Mots-clés: kératinase, déchets de plumes de volaille, enzymes fongiques, traitement du cuir respectueux de l’environnement, bioconversion