Clear Sky Science · pt
Uma força transversal de picoNewton revelada no escoamento anisotrópico de Womersley
Por que pequenos empurrões laterais no fluxo sanguíneo importam
As nossas artérias são revestidas por uma fina camada de células que sentem constantemente o empurrão e o puxão do sangue em movimento. Por décadas, os pesquisadores concentraram-se no arraste do sangue ao longo da parede do vaso, chamado tensão de cisalhamento, como o principal sinal mecânico percebido por essas células. No entanto, essa medida tem dificuldade em prever de forma confiável onde surgirão condições perigosas como aterosclerose ou aneurismas. Este estudo propõe uma maneira diferente de pensar sobre como o sangue pressiona a parede do vaso: não apenas como um atrito suave ao longo da superfície, mas como pequenos empurrões laterais — na ordem de um trilionésimo de newton — que surgem da forma como o movimento interno do sangue torce e curva-se perto da parede.
Olhando além de uma simples força de atrito
Tradicionalmente, os cientistas tentaram ligar a saúde dos vasos sanguíneos à tensão de cisalhamento na parede, um único número que descreve quão fortemente o sangue arrasta ao longo da superfície. Mas o fluxo sanguíneo real está longe de ser simples. Pulsando a cada batida do coração, ele forma estruturas turbulentas e padrões complexos que mudam no tempo e no espaço. Experimentos e simulações computacionais mostraram que dois escoamentos com a mesma tensão de cisalhamento na parede ainda podem produzir respostas celulares muito diferentes, sugerindo que informações importantes se perdem quando tudo é comprimido em uma única grandeza escalar.
O sangue como um fluido sensível à direção
Parte do enigma reside na própria natureza do sangue. O sangue não é um líquido uniforme; quase metade do seu volume é composto por glóbulos vermelhos que se deformam, alinham-se e migram sob o efeito do escoamento. Próximo à parede do vaso, essas células tendem a se afastar, deixando uma camada delgada com propriedades diferentes do núcleo do fluxo. Como resultado, as tensões internas no sangue dependem da direção — não podem ser totalmente descritas por um único valor de viscosidade. Neste trabalho, o autor incorpora essa sensibilidade direcional diretamente nas equações governantes, substituindo a viscosidade escalar usual por uma pequena matriz que pode acoplar o movimento ao longo do vaso ao movimento ao redor dele. Essa mudança matematicamente simples libera comportamentos que são impossíveis no modelo clássico.
Descobrindo forças laterais ocultas
Usando um tubo reto e rígido idealizado como bancada limpa de testes, o estudo revisita uma descrição clássica do escoamento pulsátil conhecida como fluxo de Womersley. Na imagem padrão, o fluido move-se apenas ao longo do tubo, sem giro e sem impulso inercial lateral além de um leve efeito centrípeto. Quando a nova viscosidade dependente da direção é introduzida, a solução muda qualitativamente: o escoamento desenvolve um leve redemoinho azimutal, a vorticidade ganha novos componentes e sua interação cria um termo inercial radial — o vetor de Lamb — que aponta para dentro ou para fora da parede. Ao resolver numericamente essas equações com alta precisão, o autor mostra que essa força inercial transversal se concentra fortemente em uma fina camada próxima à parede e que, quando integrada sobre a área ocupada por uma única célula endotelial, atinge níveis de picoNewton comparáveis às forças conhecidas por abrir canais iônicos mecanossensíveis.
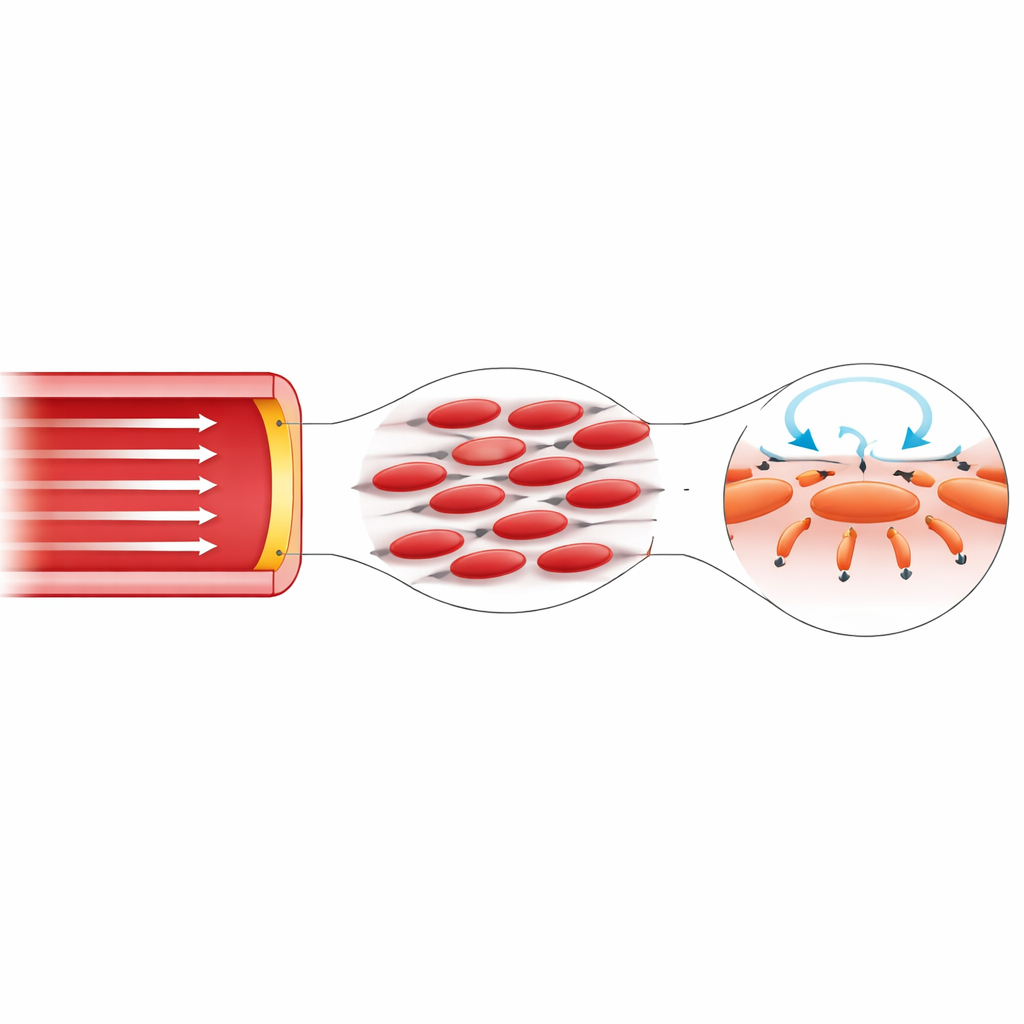
Como essas forças variam pela árvore arterial
A análise é então estendida de um batimento cardíaco ideal para formas de onda de pressão realistas medidas em seis artérias humanas diferentes, variando desde a grande raiz aórtica até vasos periféricos menores. Um parâmetro de controle chave é o número de Womersley, que compara a inércia não estacionária à viscosidade e cresce com o tamanho do vaso. Em grandes artérias dominadas pela inércia, o redemoinho induzido fica confinado a uma camada limite muito fina perto da parede, e a força lateral resultante muda de sinal e direção várias vezes ao longo de um único batimento, produzindo um padrão rico e de alta frequência. Em artérias menores, o perfil de força é mais suave, penetra mais profundamente em direção ao núcleo do vaso e tende a manter uma direção interna mais consistente. Análises estatísticas confirmam que o padrão e a intensidade dessas forças de picoNewton diferem sistematicamente de um tipo de artéria para outro.
Competindo com curvatura e moldando sinais rápidos
Artérias reais não são retilíneas, e a curvatura do vaso também gera forças transversais por efeitos centrífugos e movimentos secundários de rotação. O estudo compara esse carregamento gerado pela geometria com o novo mecanismo impulsionado pela anisotropia no domínio da frequência. Na frequência fundamental do batimento, forças induzidas pela curvatura são tipicamente mais fortes — muitas vezes por cerca de uma ordem de magnitude. No entanto, ao examinar harmônicos mais altos do pulso, a contribuição geométrica em grande escala é fortemente filtrada pela inércia, enquanto as forças anisotrópicas próximas à parede mantêm potência substancial. Isso significa que, em frequências mais altas, a forçagem lateral sentida pelas células endoteliais é dominada não pela forma do vaso, mas pela natureza direcional do próprio sangue.
O que isso significa para a saúde dos vasos
Ao mostrar que níveis realistas de anisotropia do sangue produzem de forma natural forças laterais na escala de picoNewtons concentradas na parede do vaso, este trabalho introduz uma nova linha de base independente da geometria para como o fluxo sanguíneo pulsátil pode estimular mecanicamente as células endoteliais. Em vez de depender apenas da tensão de cisalhamento na parede, aponta para uma grandeza volumétrica — o vetor de Lamb, que captura como velocidade e vorticidade interagem — como um descritor mais completo do ambiente mecânico. O estudo sugere que a forçagem multidirecional e de alta frequência originada na estrutura interna do sangue pode ajudar a explicar por que células em diferentes artérias respondem de maneira tão diferente, mesmo sob níveis médios de cisalhamento semelhantes, e oferece uma base teórica para futuros experimentos que investiguem a mecanobiologia endotelial nos domínios espectral e direcional.
Citação: Saqr, K.M. A transverse picoNewton force revealed in anisotropic Womersley flow. Sci Rep 16, 12584 (2026). https://doi.org/10.1038/s41598-026-47474-x
Palavras-chave: mecânica do fluxo sanguíneo, mecanotransdução endotelial, hemodinâmica pulsátil, viscosidade anisotrópica, forças na parede arterial