Clear Sky Science · fr
Une force transverse de l’ordre du picoNewton révélée dans l’écoulement anisotrope de Womersley
Pourquoi de petites poussées latérales dans l’écoulement sanguin comptent
Nos artères sont tapissées d’une fine couche de cellules qui ressent en permanence les poussées et tractions du sang en mouvement. Pendant des décennies, les chercheurs se sont concentrés sur la traînée du sang qui frotte la paroi, appelée contrainte de cisaillement, considérée comme le signal mécanique principal perçu par ces cellules. Pourtant, cette grandeur a eu du mal à prédire de façon fiable où des conditions dangereuses comme l’athérosclérose ou les anévrismes apparaîtront. Cette étude propose une autre manière de penser la façon dont le sang sollicite la paroi : pas seulement comme un frottement lisse le long de la paroi, mais comme de minuscules coups latéraux — de l’ordre du billionième de newton — qui émergent de la manière dont le mouvement interne du sang se tord et tourne près de la paroi.
Au-delà d’une simple force de frottement
Traditionnellement, les scientifiques ont tenté de relier la santé des vaisseaux sanguins à la contrainte de cisaillement à la paroi, un nombre unique décrivant la force avec laquelle le sang glisse le long de la surface. Mais l’écoulement sanguin réel est loin d’être simple. Pulsatile à chaque battement cardiaque, il forme des structures tourbillonnaires et des motifs complexes qui évoluent dans le temps et l’espace. Des expériences et des simulations numériques ont montré que deux écoulements affichant la même contrainte de cisaillement à la paroi peuvent néanmoins induire des réponses cellulaires très différentes, ce qui suggère qu’une information importante est perdue lorsque tout est compressé en une seule grandeur scalaire.
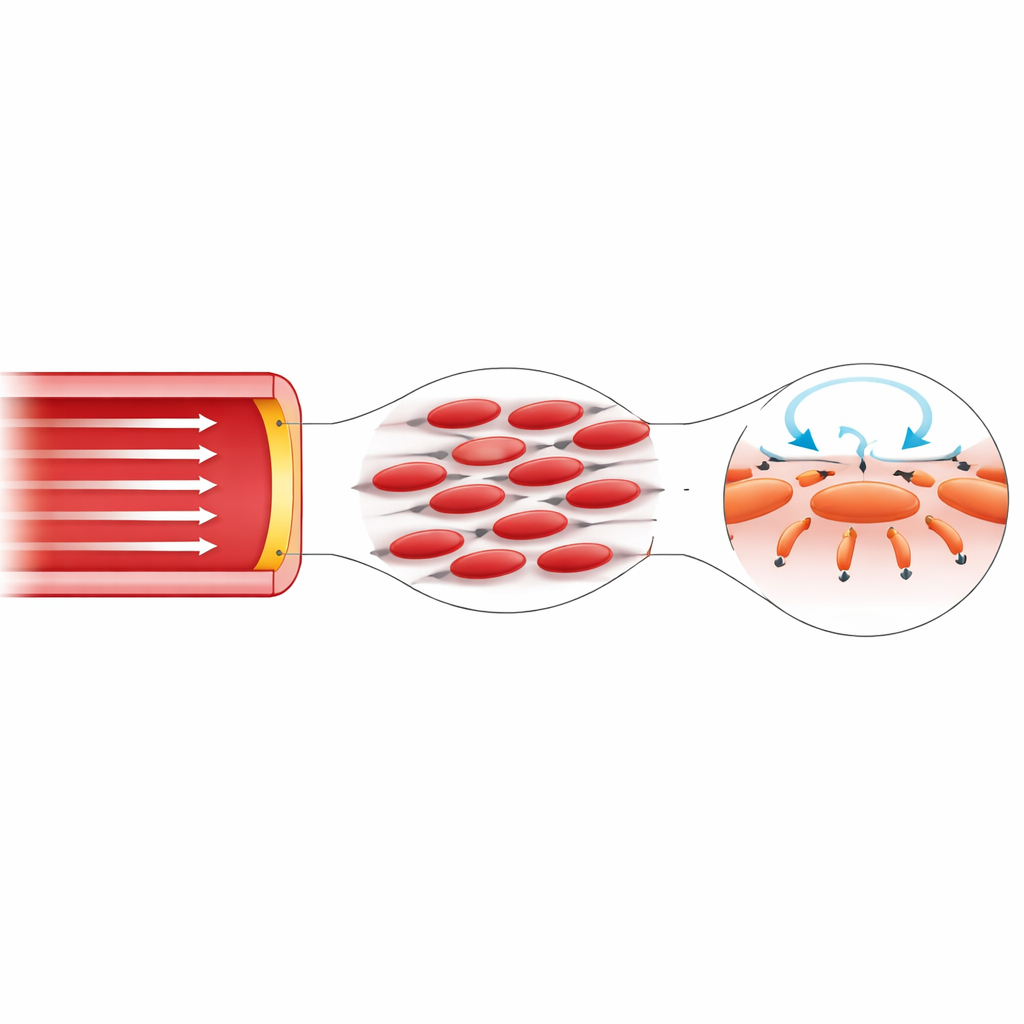
Le sang, un fluide sensible à la direction
Une partie du puzzle tient à la nature même du sang. Le sang n’est pas un liquide uniforme ; près de la moitié de son volume est occupée par des globules rouges qui se déforment, s’alignent et migrent sous l’effet de l’écoulement. Près de la paroi, ces cellules ont tendance à s’éloigner, laissant une couche mince aux propriétés distinctes du cœur d’écoulement. En conséquence, les contraintes internes dans le sang dépendent de la direction — elles ne peuvent être entièrement décrites par une seule valeur de viscosité. Dans ce travail, l’auteur intègre cette sensibilité directionnelle directement dans les équations gouvernantes en remplaçant la viscosité scalaire habituelle par une petite matrice capable de coupler le mouvement le long du vaisseau au mouvement autour de celui-ci. Ce changement mathématiquement simple libère des comportements impossibles dans le modèle classique.
Mettre au jour des forces latérales cachées
En utilisant un tube droit et rigide idéalisé comme banc d’essai, l’étude revisite une description classique de l’écoulement pulsatile connue sous le nom d’écoulement de Womersley. Dans le tableau standard, le fluide se déplace uniquement le long du tube, sans tourbillon et sans poussée inertielle latérale autre qu’un léger effet centripète. Lorsque la nouvelle viscosité dépendante de la direction est introduite, la solution change qualitativement : l’écoulement développe un léger mouvement tourbillonnaire azimutal, la vorticité acquiert de nouvelles composantes, et leur interaction crée un terme inertiel radial — le vecteur de Lamb — qui pointe vers ou depuis la paroi. En résolvant numériquement ces équations avec une grande précision, l’auteur montre que cette force inertielle transverse est fortement concentrée dans une fine couche proche de la paroi et, intégrée sur l’empreinte d’une cellule endothéliale unique, atteint des niveaux de picoNewton comparables aux forces connues pour ouvrir des canaux ioniques mécanosensibles.
Comment ces forces varient dans l’arbre artériel
L’analyse est ensuite étendue d’un battement cardiaque idéal à des formes d’onde de pression réalistes mesurées dans six artères humaines différentes, allant de la grande racine aortique à des vaisseaux périphériques plus petits. Un paramètre de contrôle clé est le nombre de Womersley, qui compare l’inertie non stationnaire à la viscosité et augmente avec la taille du vaisseau. Dans les grandes artères dominées par l’inertie, le tourbillon induit se confine à une couche limite très mince près de la paroi, et la force latérale résultante change de signe et de direction plusieurs fois au cours d’un même battement, produisant un motif riche à haute fréquence. Dans les artères plus petites, le profil de force est plus doux, pénètre plus profondément vers le cœur de l’écoulement et tend à conserver une direction intérieure plus constante. L’analyse statistique confirme que le motif et l’intensité de ces forces de l’ordre du picoNewton diffèrent systématiquement d’un type d’artère à l’autre.
En concurrence avec la courbure et modelant les signaux rapides
Les artères réelles ne sont pas droites, et la courbure des vaisseaux génère aussi des forces transverses par des effets centrifuges et des mouvements tourbillonnaires secondaires. L’étude compare ce chargement induit par la géométrie avec le nouveau mécanisme lié à l’anisotropie dans le domaine fréquentiel. À la fréquence cardiaque fondamentale, les forces induites par la courbure sont généralement plus fortes — souvent d’environ un ordre de grandeur. Cependant, lorsque l’on considère les harmoniques supérieurs du pouls, la contribution géométrique à grande échelle est fortement filtrée par l’inertie, tandis que les forces anisotropes proches de la paroi conservent une puissance substantielle. Cela signifie qu’aux fréquences élevées, la sollicitation latérale ressentie par les cellules endothéliales est dominée non pas par la forme du vaisseau, mais par la nature direction-dépendante du sang lui-même.
Ce que cela implique pour la santé des vaisseaux
En montrant que des niveaux réalistes d’anisotropie sanguine produisent naturellement des forces latérales de l’ordre du picoNewton concentrées à la paroi, ce travail introduit une nouvelle référence indépendante de la géométrie pour la façon dont l’écoulement sanguin pulsatile peut stimuler mécaniquement les cellules endothéliales. Plutôt que de s’appuyer uniquement sur la contrainte de cisaillement à la paroi, il met en avant une quantité volumique — le vecteur de Lamb, capturant l’interaction entre vitesse et vorticité — comme descripteur plus complet de l’environnement mécanique. L’étude suggère que la sollicitation multidirectionnelle et à haute fréquence résultant de la structure interne du sang pourrait aider à expliquer pourquoi les cellules dans différentes artères répondent si différemment, même sous des niveaux moyens de cisaillement similaires, et offre une base théorique pour de futures expériences explorant la mécanobiologie endothéliale dans les domaines spectral et directionnel.
Citation: Saqr, K.M. A transverse picoNewton force revealed in anisotropic Womersley flow. Sci Rep 16, 12584 (2026). https://doi.org/10.1038/s41598-026-47474-x
Mots-clés: mécanique de l’écoulement sanguin, mécanotransduction endothéliale, hémodynamique pulsatile, viscosité anisotrope, forces sur la paroi artérielle