Clear Sky Science · it
Una forza trasversale di picoNewton rivelata nel flusso anisotropo di Womersley
Perché contano quei minuscoli spintoni laterali nel flusso sanguigno
Le nostre arterie sono rivestite da uno strato sottile di cellule che avvertono costantemente le spinte e i tiraggi del sangue in movimento. Per decenni i ricercatori si sono concentrati sull’attrito del sangue lungo la parete, chiamato sforzo tangenziale (shear stress), come principale segnale meccanico percepito da queste cellule. Tuttavia questa grandezza ha faticato a prevedere in modo affidabile dove si manifestano condizioni pericolose come aterosclerosi o aneurismi. Questo studio propone un modo diverso di pensare a come il sangue solleciti la parete: non solo come un levigante scorrimento lungo la superficie, ma come piccoli colpetti laterali—dell’ordine del trilionesimo di newton—che emergono dal modo in cui il moto interno del sangue si attorciglia e si piega vicino alla parete.
Oltre la semplice forza di scorrimento
Tradizionalmente gli scienziati hanno cercato di collegare la salute dei vasi allo sforzo tangenziale sulla parete, un singolo numero che descrive quanto intensamente il sangue trascina la superficie. Ma il flusso sanguigno reale è ben lungi dall’essere semplice. Pulsando a ogni battito cardiaco, forma strutture vorticali e schemi complessi che cambiano nel tempo e nello spazio. Esperimenti e simulazioni al computer hanno mostrato che due flussi con lo stesso shear stress alla parete possono comunque produrre risposte cellulari molto diverse, suggerendo che informazioni importanti vanno perse quando tutto viene compress o in una sola grandezza scalare.
Il sangue come fluido sensibile alla direzione
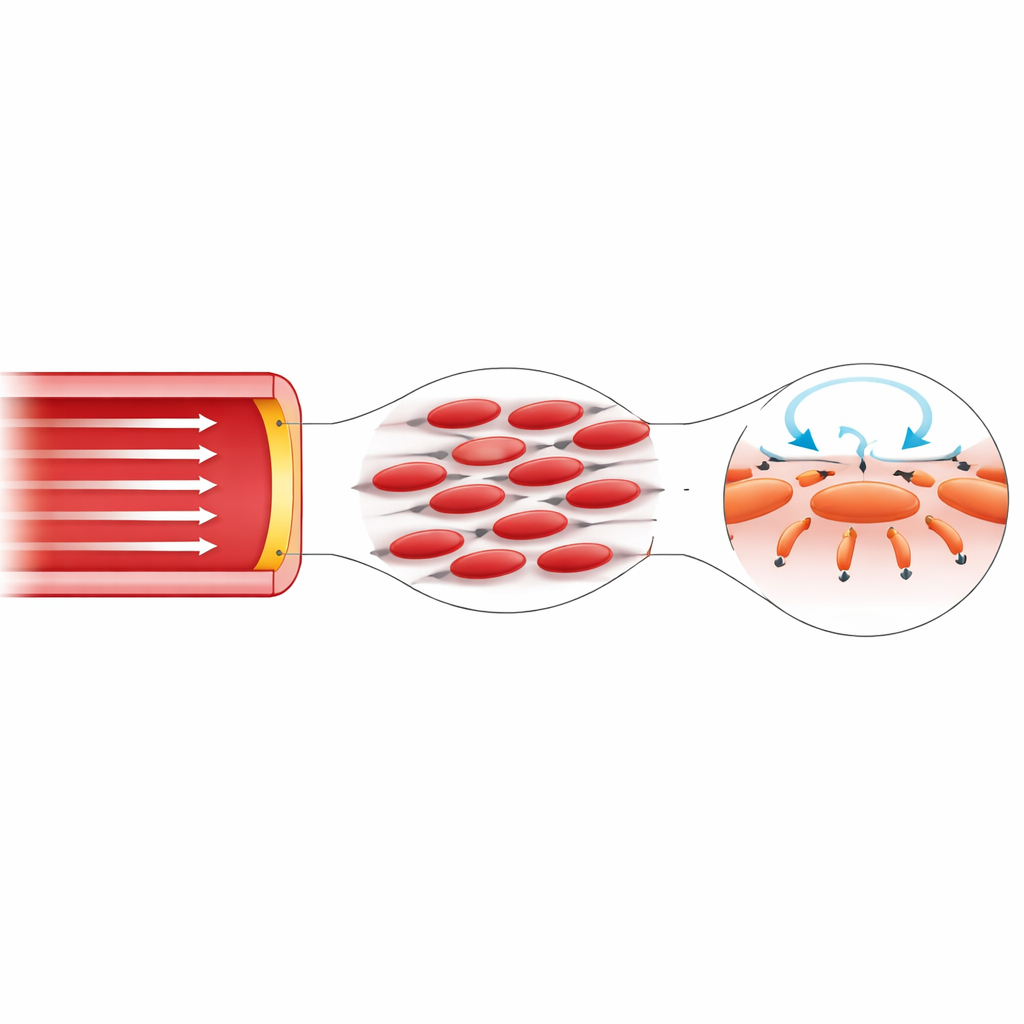
Parte del problema risiede nella natura stessa del sangue. Il sangue non è un liquido uniforme; quasi la metà del suo volume è costituita da globuli rossi che si deformano, si allineano e migrano sotto flusso. Vicino alla parete vascolare queste cellule tendono ad allontanarsi, lasciando uno strato sottile con proprietà diverse rispetto al nucleo centrale. Di conseguenza, le sollecitazioni interne nel sangue dipendono dalla direzione—non possono essere descritte pienamente con un’unica viscosità scalare. In questo lavoro l’autore incorpora questa sensibilità direzionale direttamente nelle equazioni che governano il moto, sostituendo la consueta viscosità scalare con una piccola matrice in grado di accoppiare il moto lungo il vaso al moto intorno ad esso. Questo cambiamento matematicamente semplice sblocca comportamenti impossibili nel modello classico.
Scoprire forze laterali nascoste
Usando un tubo diritto e rigido idealizzato come banco di prova, lo studio rivisita una descrizione classica del flusso pulsatile nota come flusso di Womersley. Nella rappresentazione standard, il fluido si muove solo lungo il tubo, senza avvitamenti e senza spinte inerziali laterali ad eccezione di un lieve effetto centripeto. Quando si introduce la nuova viscosità dipendente dalla direzione, la soluzione cambia qualitativamente: il flusso sviluppa un lieve moto azimutale, la vorticità acquista nuove componenti e la loro interazione crea un termine inerziale radiale—il vettore di Lamb—that punta verso o lontano dalla parete. Risolvendo numericamente queste equazioni con elevata accuratezza, l’autore mostra che questa forza inerziale trasversale è fortemente concentrata in uno strato sottile vicino alla parete e, integrata sull’impronta di una singola cellula endoteliale, raggiunge livelli di picoNewton paragonabili alle forze note per aprire canali ionici meccanosensibili.
Come queste forze variano nell’albero arterioso
L’analisi viene poi estesa da un singolo battito ideale a forme d’onda di pressione realistiche misurate in sei diverse arterie umane, che vanno dalla grande radice aortica a vasi periferici più piccoli. Un parametro di controllo chiave è il numero di Womersley, che confronta l’inerzia non stazionaria con la viscosità e cresce con le dimensioni del vaso. Nelle grandi arterie dominate dall’inerzia, il vortice indotto è confinato in uno strato limite molto sottile vicino alla parete, e la conseguente forza laterale cambia segno e direzione più volte nel corso di un singolo battito, producendo un pattern ricco e ad alta frequenza. In arterie più piccole, il profilo della forza è più liscio, penetra più in profondità verso il nucleo del flusso e tende a mantenere una direzione interna più coerente. L’analisi statistica conferma che il modello e l’intensità di queste forze di picoNewton differiscono sistematicamente tra i vari tipi di arteria.
Competizione con la curvatura e modulazione dei segnali rapidi
Le arterie reali non sono dritte, e la curvatura del vaso genera anch’essa forze trasversali attraverso effetti centrifughi e moti secondari vorticosi. Lo studio confronta questo carico dovuto alla geometria con il nuovo meccanismo guidato dall’anisotropia nel dominio delle frequenze. Alla frequenza fondamentale del battito, le forze indotte dalla curvatura sono tipicamente più intense—spesso di circa un ordine di grandezza. Tuttavia, analizzando gli armonici più alti del polso, il contributo geometrico su larga scala viene fortemente filtrato dall’inerzia, mentre le forze anisotrope vicino alla parete conservano potenza sostanziale. Ciò significa che ad alte frequenze la sollecitazione laterale avvertita dalle cellule endoteliali è dominata non dalla forma del vaso, ma dalla natura direzionale del sangue stesso.
Cosa significa per la salute dei vasi
Dimostrando che livelli realistici di anisotropia del sangue producono naturalmente forze laterali concentrate sulla parete dell’ordine dei picoNewton, questo lavoro introduce una nuova baseline indipendente dalla geometria per come il flusso pulsatile può stimolare meccanicamente le cellule endoteliali. Piuttosto che basarsi esclusivamente sullo shear stress alla parete, suggerisce una quantità volumetrica—il vettore di Lamb, che cattura l’interazione tra velocità e vorticità—come descrittore più completo dell’ambiente meccanico. Lo studio propone che forzamenti ad alta frequenza e multidirezionali, derivanti dalla struttura interna del sangue, possano contribuire a spiegare perché le cellule in arterie diverse rispondono in modo così differente, anche con livelli medi di shear simili, e offre una base teorica per esperimenti futuri che indaghino la meccanobiologia endoteliale nei domini spettrale e direzionale.
Citazione: Saqr, K.M. A transverse picoNewton force revealed in anisotropic Womersley flow. Sci Rep 16, 12584 (2026). https://doi.org/10.1038/s41598-026-47474-x
Parole chiave: meccanica del flusso sanguigno, meccano-trasduzione endoteliale, emodinamica pulsatile, viscosità anisotropa, forze sulla parete arteriosa