Clear Sky Science · es
Una fuerza transversal de picoNewton revelada en el flujo anisótropo de Womersley
Por qué importan los pequeños empujes laterales en el flujo sanguíneo
Nuestras arterias están revestidas por una delgada capa de células que sienten constantemente los empujes y tirones de la sangre en movimiento. Durante décadas, los investigadores se han centrado en la fricción de la sangre a lo largo de la pared del vaso, denominada tensión cortante, como la principal señal mecánica que perciben estas células. Sin embargo, esta magnitud ha tenido dificultades para predecir de forma fiable dónde aparecerán condiciones peligrosas como la aterosclerosis o los aneurismas. Este estudio propone una forma distinta de pensar cómo la sangre incide en la pared del vaso: no solo como un rozamiento suave a lo largo de la superficie, sino como pequeñas nudges laterales—del orden de una billonésima de newton—que surgen de la manera en que el movimiento interno de la sangre gira y se enrosca cerca de la pared.
Más allá de una simple fuerza de rozamiento
Tradicionalmente, los científicos han intentado vincular la salud de los vasos sanguíneos con la tensión cortante en la pared, un número único que describe con qué fuerza la sangre se arrastra a lo largo de la superficie. Pero el flujo sanguíneo real está lejos de ser simple. Pulsando con cada latido, forma estructuras arremolinadas y patrones complejos que cambian en el espacio y el tiempo. Experimentos y simulaciones por ordenador han mostrado que dos flujos con la misma tensión cortante en la pared pueden aún producir respuestas celulares muy diferentes, lo que sugiere que se pierde información importante cuando todo se comprime en una única magnitud escalar.
La sangre como un fluido sensible a la dirección
Parte del enigma reside en la propia naturaleza de la sangre. La sangre no es un líquido homogéneo; casi la mitad de su volumen está compuesto por glóbulos rojos que se deforman, se alinean y migran bajo el flujo. Cerca de la pared del vaso, estas células tienden a alejarse, dejando una capa delgada con propiedades distintas respecto al núcleo. Como resultado, las tensiones internas en la sangre dependen de la dirección—no pueden describirse completamente mediante un único valor de viscosidad. En este trabajo, el autor incorpora esta sensibilidad direccional directamente en las ecuaciones gobernantes reemplazando la viscosidad escalar habitual por una pequeña matriz que puede acoplar el movimiento a lo largo del vaso con el movimiento alrededor del mismo. Este cambio matemáticamente sencillo desbloquea comportamientos que son imposibles en el modelo clásico.
Descubriendo fuerzas laterales ocultas
Usando un tubo recto y rígido idealizado como bancada de pruebas limpia, el estudio revisita una descripción clásica del flujo pulsátil conocida como flujo de Womersley. En el cuadro estándar, el fluido se mueve solo a lo largo del tubo, sin vórtice y sin empuje inercial lateral más allá de un suave efecto centrípeto. Cuando se introduce la nueva viscosidad dependiente de la dirección, la solución cambia cualitativamente: el flujo desarrolla un ligero remolino azimutal, la vorticidad gana nuevos componentes y su interacción crea un término inercial radial—el vector de Lamb—que apunta hacia o desde la pared. Al resolver numéricamente estas ecuaciones con alta precisión, el autor muestra que esta fuerza inercial transversal se concentra intensamente en una delgada capa próxima a la pared y, al integrarse sobre la huella de una sola célula endotelial, alcanza niveles de picoNewton comparables a las fuerzas conocidas por activar canales iónicos mecanosensibles.
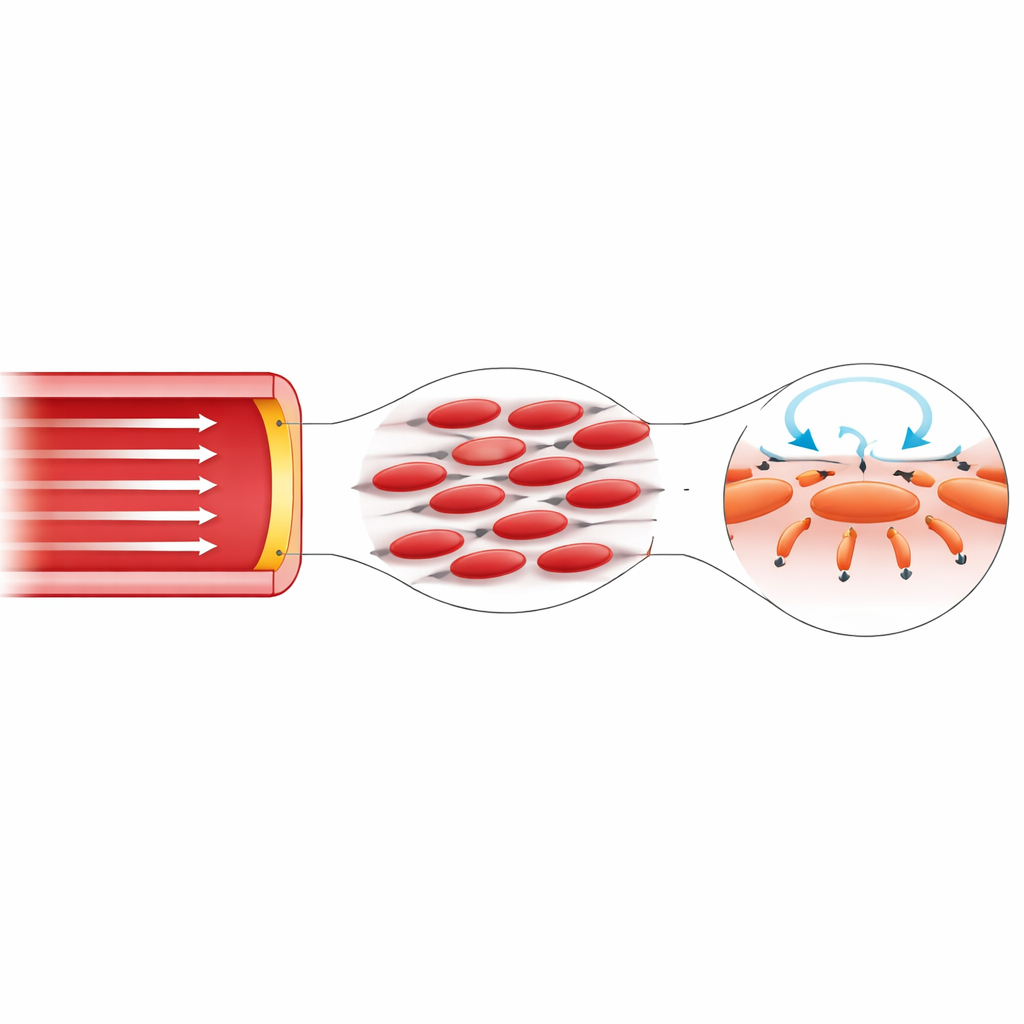
Cómo varían estas fuerzas a lo largo del árbol arterial
El análisis se extiende luego desde un latido ideal a formas de onda de presión realistas medidas en seis arterias humanas diferentes, que van desde la gran raíz aórtica hasta vasos periféricos más pequeños. Un parámetro de control clave es el número de Womersley, que compara la inercia no estacionaria con la viscosidad y crece con el tamaño del vaso. En arterias grandes dominadas por la inercia, el remolino inducido se confina a una capa límite muy delgada cerca de la pared, y la fuerza lateral resultante cambia de signo y dirección varias veces durante un solo latido, produciendo un patrón rico y de alta frecuencia. En arterias más pequeñas, el perfil de la fuerza es más suave, penetra más hacia el núcleo del vaso y tiende a mantener una dirección hacia el interior más consistente. El análisis estadístico confirma que el patrón y la intensidad de estas fuerzas de picoNewton difieren sistemáticamente según el tipo de arteria.
Compitiendo con la curvatura y moldeando señales rápidas
Las arterias reales no son rectas, y la curvatura del vaso también genera fuerzas transversales mediante efectos centrífugos y movimientos secundarios en remolino. El estudio compara esta carga impulsada por la geometría con el nuevo mecanismo impulsado por la anisotropía en el dominio de la frecuencia. En la frecuencia fundamental del latido, las fuerzas inducidas por la curvatura suelen ser más fuertes—con frecuencia por cerca de un orden de magnitud. Sin embargo, al observar armónicos más altos del pulso, la contribución geométrica a gran escala es fuertemente filtrada por la inercia, mientras que las fuerzas anisótropas próximas a la pared conservan una potencia sustancial. Esto significa que a frecuencias más altas, la forzamiento lateral sentido por las células endoteliales está dominado no por la forma del vaso, sino por la naturaleza direccional de la propia sangre.
Qué implica esto para la salud vascular
Al mostrar que niveles realistas de anisotropía sanguínea producen de forma natural fuerzas laterales de escala picoNewton concentradas en la pared vascular, este trabajo introduce una nueva línea base independiente de la geometría sobre cómo el flujo sanguíneo pulsátil puede estimular mecánicamente a las células endoteliales. En lugar de apoyarse únicamente en la tensión cortante en la pared, apunta a una cantidad volumétrica—el vector de Lamb, que captura cómo interactúan velocidad y vorticidad—como un descriptor más completo del entorno mecánico. El estudio sugiere que el forzamiento multidireccional y de alta frecuencia que surge de la estructura interna de la sangre puede ayudar a explicar por qué las células en distintas arterias responden de forma tan diferente, incluso bajo niveles promedio de cizallamiento similares, y ofrece una base teórica para futuros experimentos que exploren la mecanobiología endotelial en los dominios espectral y direccional.
Cita: Saqr, K.M. A transverse picoNewton force revealed in anisotropic Womersley flow. Sci Rep 16, 12584 (2026). https://doi.org/10.1038/s41598-026-47474-x
Palabras clave: mecánica del flujo sanguíneo, mecanotransducción endotelial, hemodinámica pulsátil, viscosidad anisótropa, fuerzas sobre la pared arterial