Clear Sky Science · de
Eine transversale picoNewton-Kraft im anisotropen Womersley-Fluss aufgedeckt
Warum winzige seitliche Stöße im Blutfluss wichtig sind
Unsere Arterien sind mit einer dünnen Zellschicht ausgekleidet, die ständig den Druck und Zug des strömenden Blutes spürt. Jahrzehntelang konzentrierten sich Forschende auf die Reibung des Bluts an der Gefäßwand, die sogenannte Schubspannung, als das wichtigste mechanische Signal, das diese Zellen wahrnehmen. Diese Größe konnte jedoch nur eingeschränkt zuverlässig vorhersagen, wo gefährliche Erkrankungen wie Atherosklerose oder Aneurysmen entstehen. Diese Studie schlägt eine andere Betrachtungsweise dafür vor, wie Blut an die Gefäßwand stößt: nicht nur als gleichmäßiges Reiben entlang der Wand, sondern als winzige seitliche Stupser—im Bereich von Billionsteln eines Newton—die aus der Art entstehen, wie sich das innere Fließen des Bluts in Wandnähe verdreht und dreht.
Über das einfache Reibungskraftbild hinausblicken
Traditionell versuchten Wissenschaftler, die Gesundheit von Blutgefäßen mit der Wand-Schubspannung zu verknüpfen, einer einzelnen Zahl, die beschreibt, wie stark Blut an der Oberfläche zieht. Echter Blutfluss ist jedoch alles andere als einfach. Im Takt jedes Herzschlags pulsiert er, bildet Wirbelstrukturen und komplexe Muster, die sich in Zeit und Raum verändern. Experimente und Computersimulationen haben gezeigt, dass zwei Strömungen mit gleicher Schubspannung an der Wand sehr unterschiedliche Reaktionen in den Zellen hervorrufen können, was nahelegt, dass wichtige Informationen verloren gehen, wenn alles auf eine skalare Größe komprimiert wird.
Blut als richtungssensitives Fluid
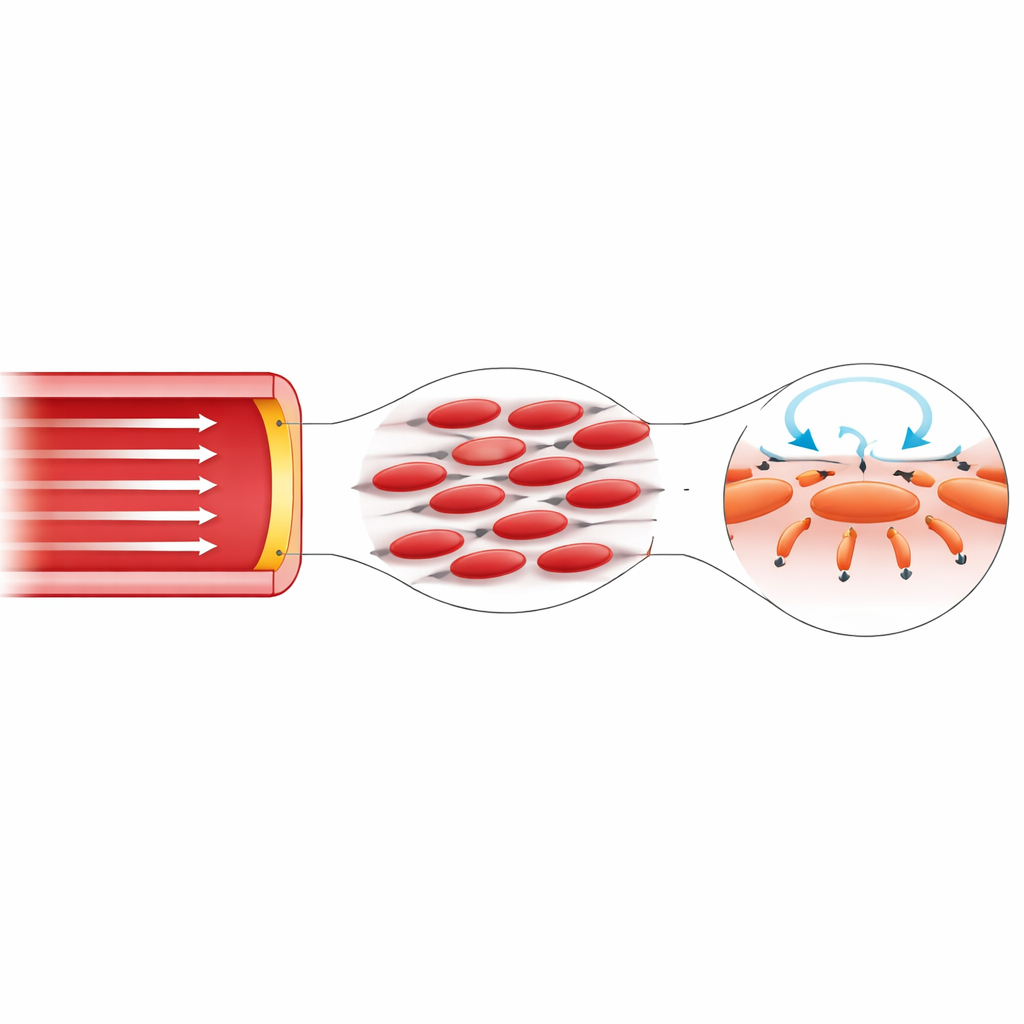
Ein Teil des Rätsels liegt in der Natur des Bluts selbst. Blut ist keine einheitliche Flüssigkeit; nahezu die Hälfte seines Volumens besteht aus roten Blutkörperchen, die sich unter Strömung verformen, ausrichten und migrieren. In Wandnähe neigen diese Zellen dazu, wegzuwandern und hinterlassen eine dünne Schicht mit anderen Eigenschaften als der Kernströmung. Dadurch hängen die inneren Spannungen im Blut von der Richtung ab—sie lassen sich nicht vollständig durch einen einzigen Viskositätswert beschreiben. In dieser Arbeit wird diese Richtungsabhängigkeit direkt in die herrschenden Gleichungen eingebaut, indem die übliche skalare Viskosität durch eine kleine Matrix ersetzt wird, die Bewegungen längs des Gefäßes mit Bewegungen darum koppeln kann. Diese mathematisch einfache Änderung erschließt Verhaltensweisen, die im klassischen Modell unmöglich sind.
Verborgene seitliche Kräfte aufspüren
Unter Verwendung eines idealisierten geraden, starren Rohrs als sauberes Testfeld untersucht die Studie die klassische Beschreibung pulsierender Strömung, bekannt als Womersley-Strömung, neu. Im Standardbild bewegt sich die Flüssigkeit nur entlang des Rohrs, ohne Wirbel und ohne seitliche träge Schubkraft außer einem sanften Zentripetaleffekt. Bei Einführung der neuen richtungsabhängigen Viskosität verändert sich die Lösung qualitativ: Die Strömung entwickelt ein geringes azimutales Aufwirbeln, die Wirbelstärke gewinnt neue Komponenten, und deren Wechselwirkung erzeugt einen radialen Trägheitsterm—den Lamb-Vektor—der zur Wand hin oder von ihr wegzeigt. Durch hochgenaues numerisches Lösen dieser Gleichungen zeigt der Autor, dass diese transversale Trägheitskraft scharf in einer dünnen nahe der Wand liegenden Schicht konzentriert ist und, integriert über die Aufstandsfläche einer einzelnen Endothelzelle, picoNewton-Niveaus erreicht, die mit Kräften vergleichbar sind, die mechanosensitive Ionenkanäle öffnen können.
Wie diese Kräfte im arteriellen Baum variieren
Die Analyse wird dann von einem idealen Herzschlag auf realistische Druckwellenformen ausgeweitet, die in sechs verschiedenen menschlichen Arterien gemessen wurden, von der großen Aortenwurzel bis zu kleineren peripheren Gefäßen. Ein zentraler Steuerparameter ist die Womersley-Zahl, die die unsteady Trägheit mit der Viskosität vergleicht und mit der Gefäßgröße zunimmt. In großen, trägheitsdominierten Arterien ist das induzierte Aufwirbeln auf eine sehr dünne Randzonenschicht nahe der Wand beschränkt, und die resultierende seitliche Kraft ändert während eines Herzschlags mehrmals ihr Vorzeichen und ihre Richtung und erzeugt ein reiches, hochfrequentes Muster. In kleineren Arterien ist das Kraftprofil glatter, dringt tiefer in den Gefäßkern ein und behält tendenziell eine beständigere nach innen gerichtete Richtung bei. Statistische Analysen bestätigen, dass Muster und Stärke dieser picoNewton-Kräfte systematisch zwischen den Arterientypen variieren.
Mit Krümmung konkurrieren und schnelle Signale formen
Echte Arterien sind nicht gerade, und Gefäßkrümmung erzeugt ebenfalls transversale Kräfte durch Fliehkrafteffekte und sekundäre Wirbelbewegungen. Die Studie vergleicht diese geometriegetriebene Belastung mit dem neuen anisotropiegetriebenen Mechanismus im Frequenzbereich. Bei der Grundfrequenz des Herzschlags sind krümmungsinduzierte Kräfte typischerweise stärker—oft um etwa eine Größenordnung. Blickt man jedoch auf höhere Harmonische der Pulse, so wird der großskalige geometrische Beitrag durch die Trägheit stark herausgefiltert, während die nahe der Wand wirkenden anisotropen Kräfte beträchtliche Leistung behalten. Das bedeutet, dass bei höheren Frequenzen die seitliche Belastung, die Endothelzellen spüren, eher von der richtungsabhängigen Natur des Bluts als von der Gefäßform dominiert wird.
Was das für die Gefäßgesundheit bedeutet
Indem gezeigt wird, dass realistische Level von Blutanisotropie natürlicherweise picoNewton-skaliere seitliche Kräfte erzeugen, die an der Gefäßwand konzentriert sind, führt diese Arbeit eine neue, von der Geometrie weitgehend unabhängige Basis ein, wie pulsierender Blutfluss Endothelzellen mechanisch stimulieren kann. Anstelle sich allein auf die Wand-Schubspannung zu stützen, weist sie auf eine volumetrische Größe—den Lamb-Vektor, der einfängt, wie Geschwindigkeit und Wirbelstärke interagieren—als vollständigere Beschreibung der mechanischen Umgebung hin. Die Studie legt nahe, dass hochfrequente, multidirektionale Belastungen, die aus der inneren Struktur des Bluts entstehen, helfen könnten zu erklären, warum Zellen in verschiedenen Arterien so unterschiedlich reagieren, selbst bei ähnlichen mittleren Schubspannungen, und bietet eine theoretische Grundlage für zukünftige Experimente, die endotheliale Mechanobiologie im spektralen und richtungsbezogenen Bereich untersuchen.
Zitation: Saqr, K.M. A transverse picoNewton force revealed in anisotropic Womersley flow. Sci Rep 16, 12584 (2026). https://doi.org/10.1038/s41598-026-47474-x
Schlüsselwörter: Mechanik des Blutflusses, endotheliale Mechanotransduktion, pulsatile Hämodynamik, anisotrope Viskosität, Kräfte an der Arterienwand