Clear Sky Science · pt
Um modelo híbrido melhorado ICEEMDAN–deep integrando dados multimodais para a triagem da neuropatia periférica diabética
Por que o dano nervoso no diabetes precisa de um teste mais suave
Para muitas pessoas com diabetes, o dano aos nervos dos pés e das pernas progride silenciosamente, tornando‑se óbvio apenas quando surgem dor, dormência ou até úlceras e amputações. Os testes atuais para essa condição, chamada neuropatia periférica diabética, podem ser invasivos, caros ou difíceis de repetir em clínicas de rotina. Este estudo explora uma nova forma de rastrear danos nervosos iniciais usando apenas sensores ópticos e elétricos inofensivos na pele, combinados com processamento inteligente de sinais e um modelo de aprendizado profundo adaptado.
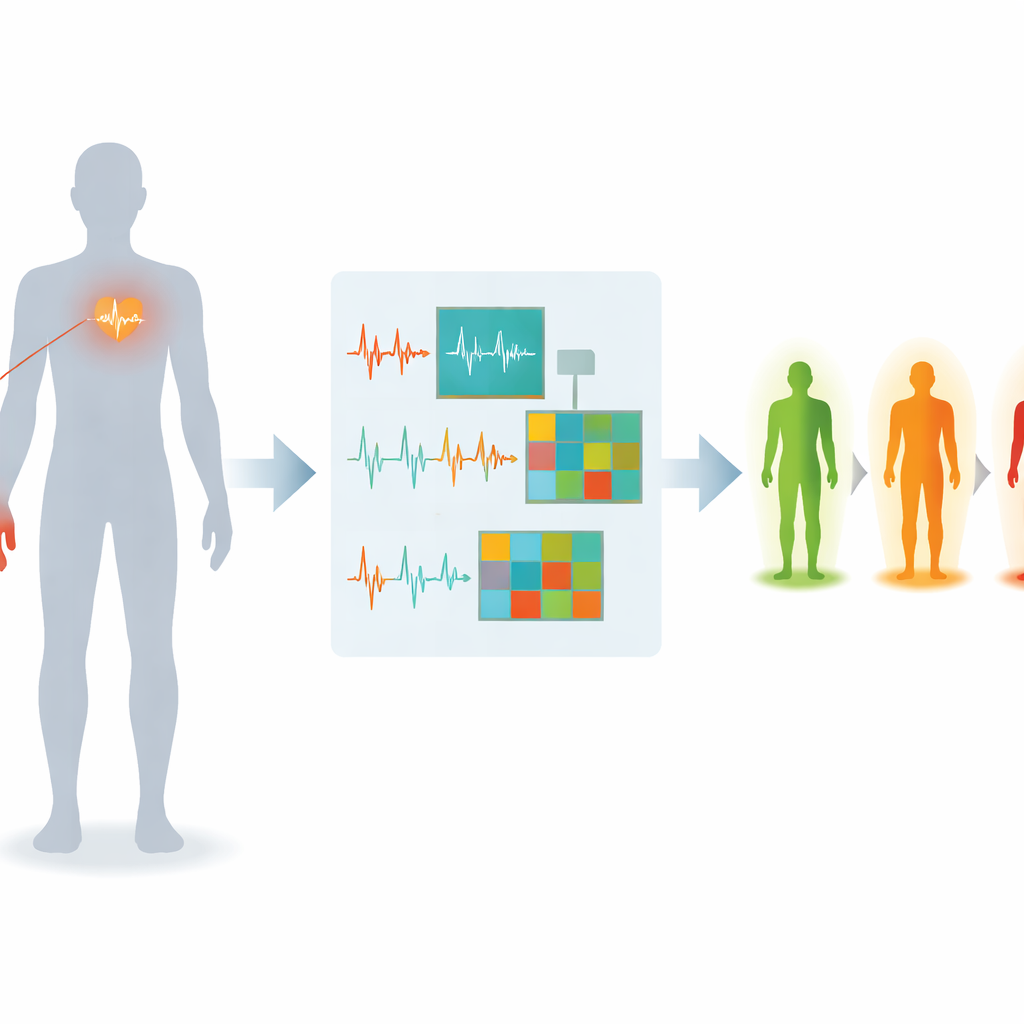
Uma nova maneira de ouvir o coração e o fluxo sanguíneo
Os pesquisadores focam em dois sinais já comuns em hospitais e dispositivos vestíveis. Um é o eletrocardiograma, ou ECG, que registra a atividade elétrica do coração. O outro é o fotopletismograma, ou PPG, um sinal óptico de um sensor de ponta do dedo que acompanha o fluxo sanguíneo a cada batida. Cada sinal conta uma parte da história de como o diabetes afeta vasos e nervos; juntos, eles podem oferecer um retrato mais completo dos danos nervosos iniciais do que qualquer um isolado. A equipe recrutou 120 pessoas, incluindo voluntários saudáveis, pessoas com diabetes sem diagnóstico de dano nervoso e pessoas com neuropatia confirmada. Para cada participante, ECG e PPG foram registrados em repouso sob condições controladas para reduzir fontes de ruído cotidiano, como movimento e variações de temperatura.
Limpeza de sinais biológicos bagunçados
Registros reais de batimento cardíaco e pulso estão cheios de oscilações indesejadas vindas de atividade muscular, respiração e interferência elétrica. Se essas distorções não forem removidas com cuidado, podem ocultar as mudanças sutis que apontam para problemas nervosos iniciais. O estudo apresenta um método de redução de ruído aprimorado que decompõe cada sinal em muitos “blocos de construção” mais simples, decide quais partes são principalmente ruído e quais carregam fisiologia genuína, e então reconstrói uma versão mais limpa. Para isso, os autores combinam uma técnica flexível de decomposição com uma estratégia de busca inspirada em enxames que sintoniza automaticamente parâmetros-chave, aplicando em seguida filtragem por wavelet apenas onde ela é mais útil. Testes contra vários métodos estabelecidos mostram que essa abordagem melhora a parte útil dos sinais de ECG e PPG enquanto mantém a distorção ao mínimo.
Transformando ondas em imagens que o computador pode ver
Em vez de alimentar ondas unidimensionais brutas em uma rede neural, os pesquisadores convertem segmentos curtos de ECG e PPG em pequenas imagens coloridas. Cada canal de cor codifica um aspecto diferente de como o sinal evolui no tempo: relações de posição entre pontos do ciclo cardíaco, mudanças de fase e ritmo, e padrões que se repetem de forma complexa e não linear. Quando essas três visões são empilhadas, formam um “retrato” compacto de cada janela com múltiplos ciclos que enfatiza características dinâmicas ligadas à saúde dos nervos e vasos. Ao combinar vários ciclos consecutivos em vez de um único batimento, o método captura padrões mais estáveis e interações de longo alcance entre a atividade elétrica do coração e a onda de pulso que percorre os vasos.
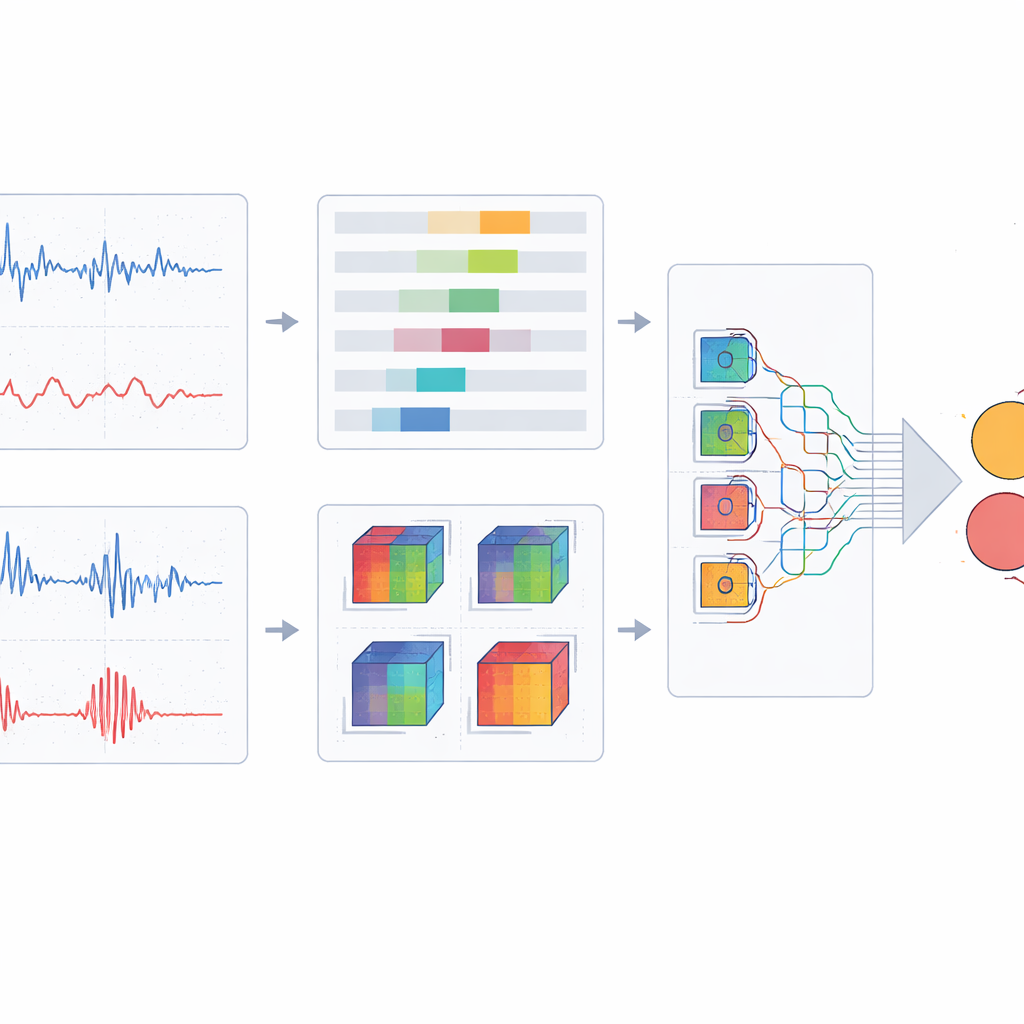
Uma rede leve que foca no que importa
Para classificar essas imagens fundidas em casos saudáveis, em risco ou com neuropatia, a equipe projetou uma arquitetura de aprendizado profundo personalizada baseada em uma espinha dorsal moderna e eficiente. Eles substituem blocos convolucionais padrão por um desenho de múltiplos ramos que examina cada patch de imagem com núcleos de formas e tamanhos diferentes, capturando tanto detalhes finos quanto tendências mais amplas sem grande aumento no custo computacional. Sobre isso, adicionam um mecanismo de atenção espacial que permite à rede enfatizar regiões e padrões informativos ao mesmo tempo em que atenua o fundo redundante. O modelo é treinado e ajustado usando validação cruzada criteriosa, e seu desempenho é comparado com uma gama de redes de classificação de imagem bem conhecidas, incluindo vários projetos populares baseados em convolução e em transformadores.
O que os resultados significam para pessoas com diabetes
Em dados construídos a partir de múltiplos ciclos cardíacos, o sistema proposto classifica corretamente o status de neuropatia em quase 94% dos casos, com sensibilidade e precisão igualmente altas. Ele supera claramente tanto configurações tradicionais de processamento de sinais quanto fortes linhas de base modernas de aprendizado profundo, indicando que a combinação de redução de ruído mais inteligente, codificação sinal‑para‑imagem mais rica e desenho de rede sob medida agrega valor real. Embora o estudo seja baseado em dados de um único centro e precise de testes mais amplos, aponta para um futuro em que medições rotineiras e indolores feitas com simples clipes e eletrodos — possivelmente até em atenção primária ou em casa — poderiam sinalizar danos nervosos iniciais em pessoas com diabetes muito antes de surgirem complicações graves.
Citação: Xiao, M., Wang, F., Fang, S. et al. An improved ICEEMDAN–depth hybrid network model integrating multimodal data for the screening of diabetic peripheral neuropathy. Sci Rep 16, 10954 (2026). https://doi.org/10.1038/s41598-026-45862-x
Palavras-chave: neuropatia periférica diabética, triagem não invasiva, ECG, PPG, aprendizado profundo