Clear Sky Science · nl
Een verbeterd ICEEMDAN–diepte hybride netwerkmodel dat multimodale gegevens integreert voor de screening van diabetische perifere neuropathie
Waarom zenuwbeschadiging bij diabetes een zachtere test verdient
Bij veel mensen met diabetes sluipt beschadiging van de zenuwen in de voeten en benen ongemerkt binnen en wordt pas duidelijk wanneer pijn, gevoelloosheid of zelfs zweren en amputaties optreden. De huidige tests voor deze aandoening, diabetes perifere neuropathie genoemd, kunnen invasief, duur of moeilijk herhaalbaar zijn in de dagelijkse klinische praktijk. Deze studie onderzoekt een nieuwe manier om vroege zenuwbeschadiging te screenen met alleen onschadelijke licht- en elektrische sensoren op de huid, gecombineerd met slimme signaalverwerking en een op maat gemaakt deep‑learningmodel.
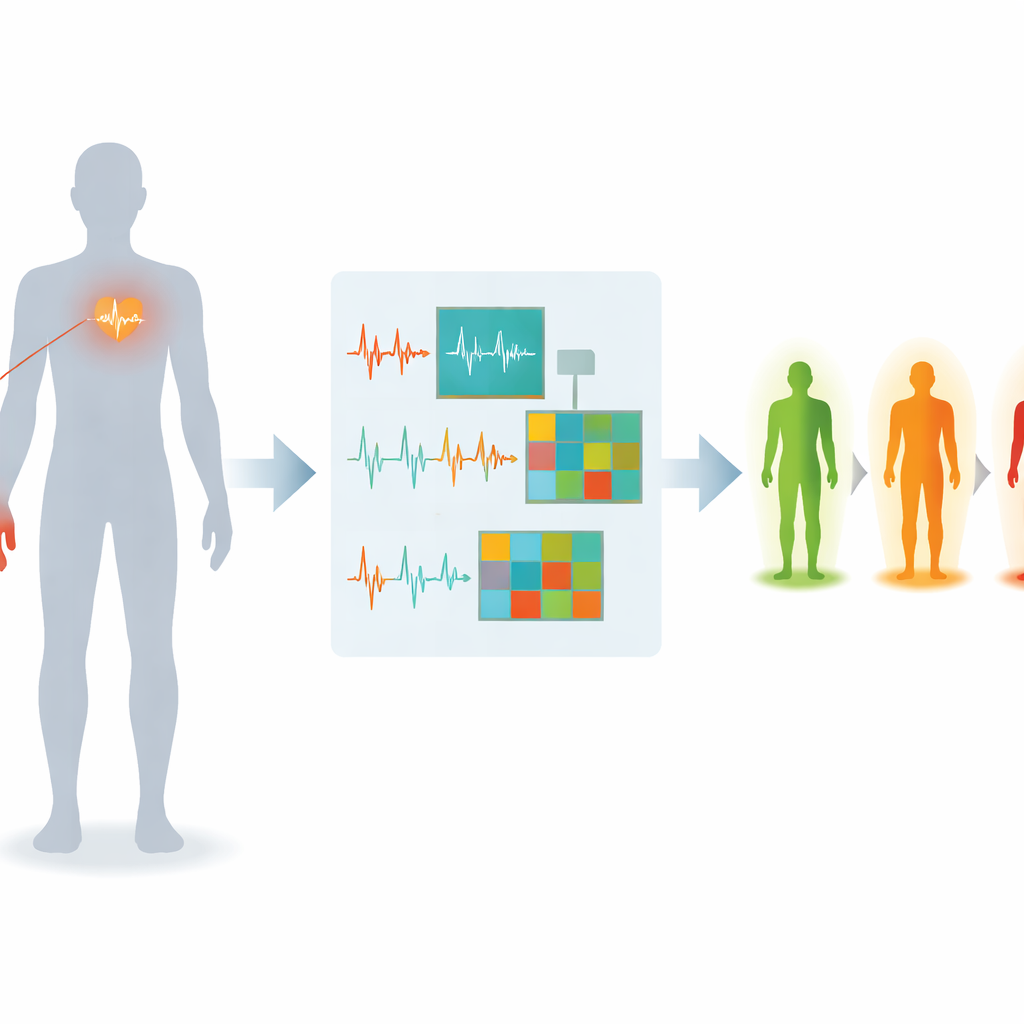
Een nieuwe manier om naar hart en bloedstroom te luisteren
De onderzoekers richten zich op twee signalen die al veel voorkomen in ziekenhuizen en draagbare apparaten. De ene is het elektrocardiogram, of ECG, dat de elektrische activiteit van het hart vastlegt. De andere is het photoplethysmogram, of PPG, een optisch signaal van een vingertopsensor dat de bloedstroom bij elke hartslag volgt. Elk signaal vertelt een deel van het verhaal over hoe diabetes bloedvaten en zenuwen beïnvloedt; samen kunnen ze een rijker beeld geven van vroege zenuwbeschadiging dan elk signaal afzonderlijk. Het team rekruteerde 120 mensen, waaronder gezonde vrijwilligers, mensen met diabetes maar zonder gediagnosticeerde zenuwbeschadiging, en mensen met bevestigde neuropathie. Voor elke deelnemer werden ECG en PPG in rust onder gecontroleerde omstandigheden geregistreerd om alledaagse storingsbronnen zoals beweging en temperatuurschommelingen te verminderen.
Rommelige biologische signalen opschonen
Opnamen van hart en pols uit de praktijk zitten vol ongewenste ruis van spieractiviteit, ademhaling en elektrische interferentie. Als deze vervormingen niet zorgvuldig worden verwijderd, kunnen ze de subtiele veranderingen verbergen die wijzen op vroege zenuwproblemen. De studie introduceert een verbeterde denoising‑methode die elk signaal opdeelt in veel eenvoudigere “bouwstenen”, bepaalt welke delen grotendeels ruis zijn en welke echte fysiologie bevatten, en vervolgens een schonere versie reconstrueert. Hiervoor combineren de auteurs een flexibele decompositietechniek met een zwermgebaseerde zoekstrategie die automatische sleutelparameters afstemt, en passen daarna wavelet‑gebaseerde filtering alleen toe waar het het meest helpt. Vergelijkende tests met diverse gevestigde methoden laten zien dat deze aanpak het nuttige deel van zowel ECG‑ als PPG‑signalen beter versterkt terwijl vervorming tot een minimum beperkt blijft.
Golven omzetten in beelden die de computer kan zien
In plaats van ruwe eendimensionale golven in een neuraal netwerk te voeren, zetten de onderzoekers korte segmenten van ECG en PPG om in kleine kleurafbeeldingen. Elk kleurkanaal codeert een ander aspect van hoe het signaal in de tijd evolueert: algemene relatieve posities tussen punten in de hartcyclus, veranderingen in fase en ritme, en patronen die op complexe, niet‑lineaire manieren terugkeren. Wanneer deze drie gezichten worden gestapeld, vormen ze een compact “portret” van elk venster met meerdere slagen dat dynamische kenmerken benadrukt die samenhangen met zenuw- en vaatgezondheid. Door meerdere opeenvolgende cycli te combineren in plaats van een enkele hartslag, legt de methode stabielere patronen vast en langeafstandsinvloed tussen de elektrische activiteit van het hart en de polsgolf die door de vaten reist.
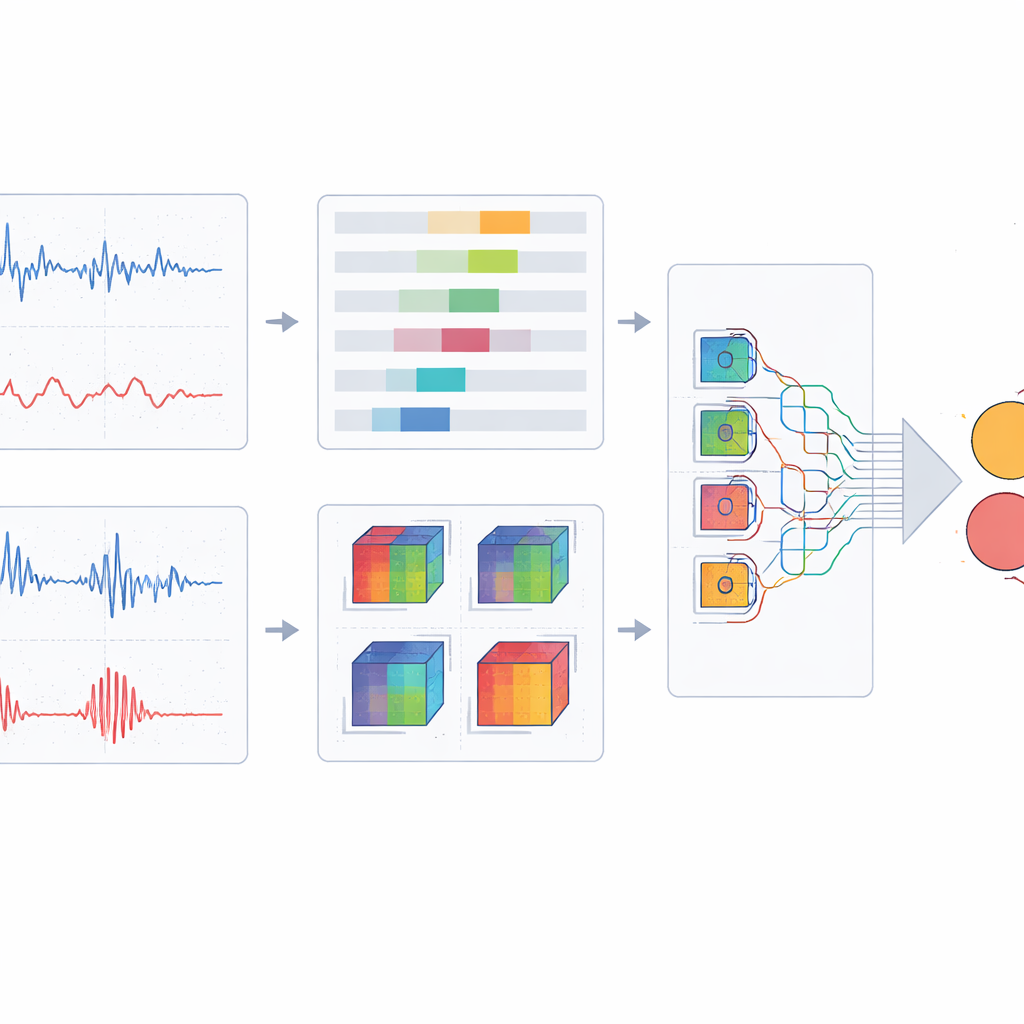
Een lichtgewicht netwerk dat zich richt op wat belangrijk is
Om deze gefuseerde afbeeldingen te classificeren als gezond, risicovol of neuropathie, ontwerpt het team een aangepast deep‑learning‑architectuur gebouwd op een moderne, efficiënte backbone. Ze vervangen standaard convolutieblokken door een meergrensontwerp dat elk afbeeldingspatch bekijkt met kernels van verschillende vormen en afmetingen, waardoor zowel fijne details als bredere trends worden vastgelegd zonder een grote toename in rekenkosten. Daarbovenop voegen ze een ruimtelijk aandachtmechanisme toe dat het netwerk in staat stelt informatieve regio’s en patronen te benadrukken terwijl redundante achtergrond minder belangrijk wordt. Het model wordt getraind en afgestemd met zorgvuldige cross‑validatie, en de prestaties worden vergeleken met een reeks bekende beeldclassificatienetwerken, waaronder verschillende populaire convolutionele en transformer‑gebaseerde ontwerpen.
Wat de resultaten betekenen voor mensen met diabetes
Op gegevens samengesteld uit meerdere hartcycli classificeert het voorgestelde systeem de neuropathiestatus correct in bijna 94% van de gevallen, met vergelijkbaar hoge gevoeligheid en precisie. Het overtreft duidelijk zowel traditionele signaalverwerkingsopstellingen als sterke moderne deep‑learning‑baselines, wat aangeeft dat de combinatie van slimmer denoising, rijkere signaal‑naar‑beeldcodering en een op maat gemaakt netwerkontwerp echte meerwaarde biedt. Hoewel de studie is gebaseerd op gegevens uit één centrum en bredere testen nodig heeft, wijst ze op een toekomst waarin routinematige, pijnloze metingen met eenvoudige clips en elektroden — mogelijk zelfs in de eerstelijnszorg of thuis — vroege zenuwbeschadiging bij mensen met diabetes kunnen signaleren lang voordat ernstige complicaties optreden.
Bronvermelding: Xiao, M., Wang, F., Fang, S. et al. An improved ICEEMDAN–depth hybrid network model integrating multimodal data for the screening of diabetic peripheral neuropathy. Sci Rep 16, 10954 (2026). https://doi.org/10.1038/s41598-026-45862-x
Trefwoorden: diabetische perifere neuropathie, niet-invasieve screening, ECG, PPG, deep learning