Clear Sky Science · it
Un migliorato modello ibrido ICEEMDAN–deep che integra dati multimodali per lo screening della neuropatia periferica diabetica
Perché il danno nervoso nel diabete richiede un esame meno invasivo
Per molte persone con diabete, il danno ai nervi di piedi e gambe avanza silenzioso, diventando evidente solo quando compaiono dolore, intorpidimento o persino ulcere e amputazioni. I test odierni per questa condizione, chiamata neuropatia periferica diabetica, possono essere invasivi, costosi o difficili da ripetere nelle cliniche di routine. Questo studio esplora un nuovo modo di schermare i primi segni di danno nervoso usando soltanto sensori ottici ed elettrici non invasivi sulla pelle, combinati con avanzate tecniche di elaborazione del segnale e un modello di deep learning su misura.
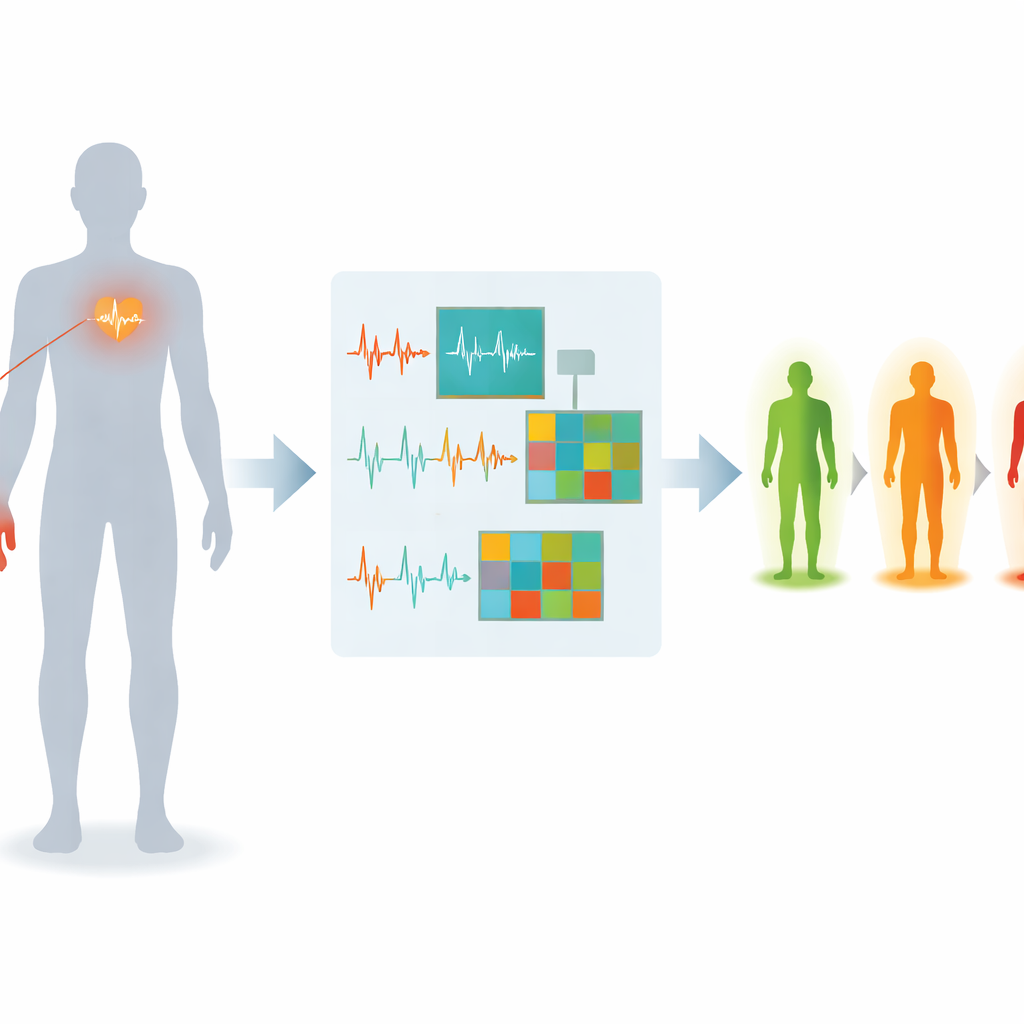
Un nuovo modo di ascoltare cuore e flusso sanguigno
I ricercatori si concentrano su due segnali già comuni negli ospedali e nei dispositivi indossabili. Uno è l’elettrocardiogramma, o ECG, che registra l’attività elettrica del cuore. L’altro è il fotopletismogramma, o PPG, un segnale ottico da un sensore al dito che traccia il flusso sanguigno a ogni battito. Ogni segnale racconta una parte dell’effetto del diabete su vasi e nervi; messi insieme possono dipingere un quadro più ricco dei primi danni nervosi rispetto a ciascun segnale preso singolarmente. Il gruppo ha reclutato 120 persone, inclusi volontari sani, pazienti diabetici senza neuropatia diagnosticata e soggetti con neuropatia confermata. Per ciascun partecipante sono stati registrati ECG e PPG a riposo in condizioni controllate per ridurre fonti di rumore quotidiane come il movimento e le variazioni di temperatura.
Ripulire i segnali biologici rumorosi
Le registrazioni reali di cuore e polso sono piene di oscillazioni indesiderate dovute all’attività muscolare, alla respirazione e alle interferenze elettriche. Se queste distorsioni non vengono rimosse con cura, possono nascondere i cambiamenti sottili che indicano problemi nervosi precoci. Lo studio introduce un metodo di denoising migliorato che scompone ciascun segnale in molti “mattoni” più semplici, decide quali parti sono per lo più rumore e quali trasmettono fisiologia reale, e quindi ricostruisce una versione più pulita. Per farlo, gli autori combinano una tecnica di decomposizione flessibile con una strategia di ricerca ispirata agli sciami che ottimizza automaticamente parametri chiave, applicando poi il filtraggio basato su wavelet soltanto dove è più utile. Test confrontati con vari metodi consolidati mostrano che questo approccio aumenta meglio la componente utile di ECG e PPG mantenendo la distorsione al minimo.
Trasformare le onde in immagini che il computer può interpretare
Invece di fornire onde unidimensionali grezze a una rete neurale, i ricercatori convertono brevi segmenti di ECG e PPG in piccole immagini a colori. Ogni canale colore codifica un aspetto diverso dell’evoluzione temporale del segnale: relazioni di posizione complessiva tra i punti del ciclo cardiaco, variazioni di fase e ritmo, e pattern che si ripetono in modi complessi e non lineari. Quando queste tre viste sono impilate insieme formano un “ritratto” compatto di ciascuna finestra multi‑battito che enfatizza caratteristiche dinamiche legate alla salute di nervi e vasi. Combinando diversi cicli consecutivi anziché un singolo battito, il metodo cattura pattern più stabili e interazioni a lungo raggio tra l’attività elettrica del cuore e l’onda di polso che viaggia nei vasi.
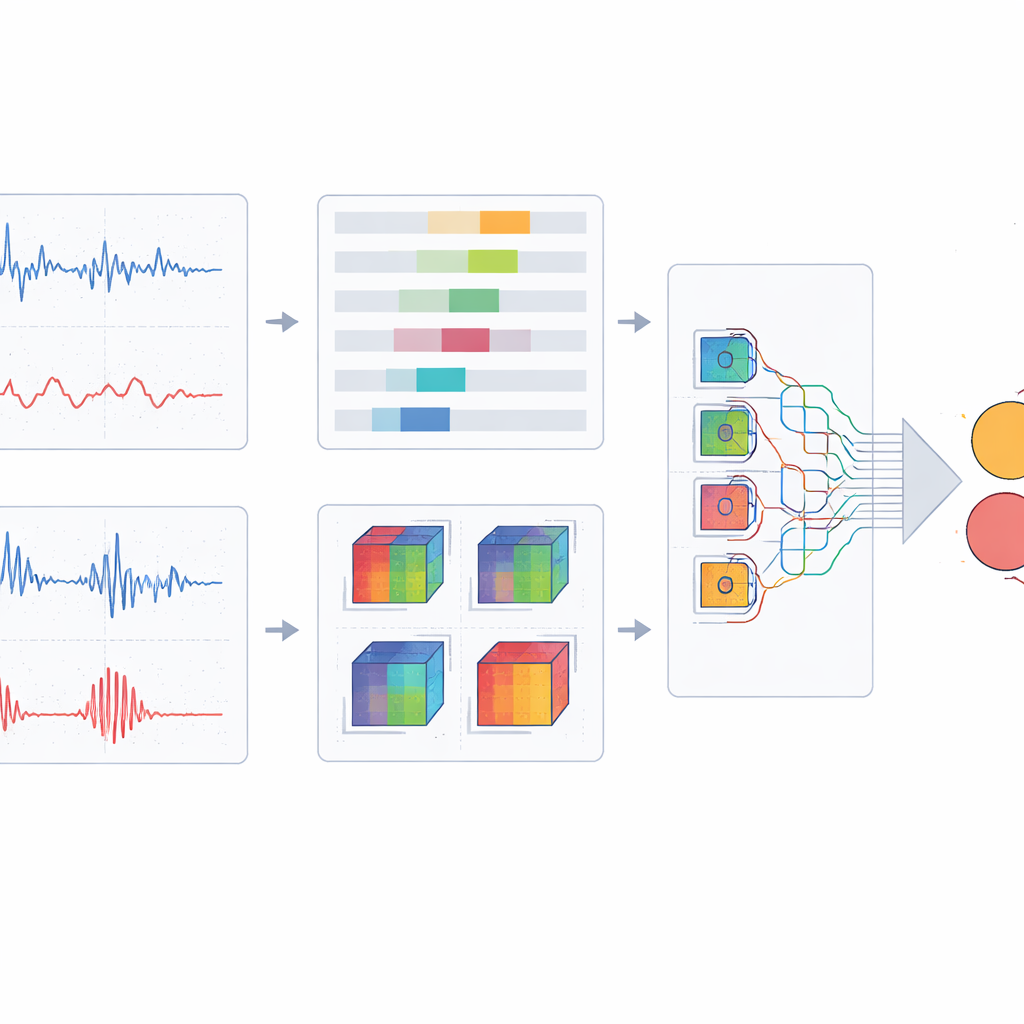
Una rete leggera che si concentra sull’essenziale
Per classificare queste immagini fuse in casi sani, a rischio o con neuropatia, il team progetta un’architettura di deep learning personalizzata basata su un backbone moderno ed efficiente. Sostituiscono i blocchi convoluzionali standard con un design a più rami che osserva ogni patch dell’immagine con kernel di forme e dimensioni diverse, catturando sia dettagli fini sia tendenze più ampie senza un grande incremento del carico computazionale. Su questo inseriscono un meccanismo di attention spaziale che permette alla rete di enfatizzare regioni e pattern informativi riducendo il peso dello sfondo ridondante. Il modello viene addestrato e ottimizzato con una accurata validazione incrociata, e le sue prestazioni sono confrontate con una serie di reti di classificazione d’immagini note, incluse diverse architetture convoluzionali e basate su transformer.
Cosa significano i risultati per le persone con diabete
Su dati costruiti a partire da più cicli cardiaci, il sistema proposto classifica correttamente lo stato di neuropatia in quasi il 94% dei casi, con sensibilità e precisione altrettanto elevate. Sovraperforma chiaramente sia le tradizionali soluzioni di elaborazione del segnale sia robusti baseline di deep learning moderno, indicando che la combinazione di denoising più intelligente, una codifica segnale‑a‑immagine più ricca e un design di rete su misura apporta un valore reale. Pur essendo lo studio basato su dati di un unico centro e richiedendo test su scale più ampie, suggerisce un futuro in cui misurazioni di routine, indolori e basate su semplici clip ed elettrodi — possibilmente anche in ambulatori di medicina generale o a casa — potrebbero segnalare danni nervosi precoci nelle persone con diabete molto prima che insorgano complicazioni gravi.
Citazione: Xiao, M., Wang, F., Fang, S. et al. An improved ICEEMDAN–depth hybrid network model integrating multimodal data for the screening of diabetic peripheral neuropathy. Sci Rep 16, 10954 (2026). https://doi.org/10.1038/s41598-026-45862-x
Parole chiave: neuropatia periferica diabetica, screening non invasivo, ECG, PPG, apprendimento profondo