Clear Sky Science · es
Un modelo híbrido mejorado ICEEMDAN–profundidad que integra datos multimodales para el cribado de la neuropatía periférica diabética
Por qué el daño nervioso en la diabetes necesita una prueba más suave
Para muchas personas con diabetes, el daño a los nervios de los pies y las piernas avanza de forma silenciosa y solo se hace evidente cuando aparecen dolor, entumecimiento o incluso úlceras y amputaciones. Las pruebas actuales para esta condición, denominada neuropatía periférica diabética, pueden ser invasivas, costosas o difíciles de repetir en la práctica clínica habitual. Este estudio explora una nueva forma de detectar precozmente el daño nervioso usando únicamente sensores ópticos y eléctricos inocuos sobre la piel, combinados con procesamiento inteligente de señales y un modelo de aprendizaje profundo adaptado.
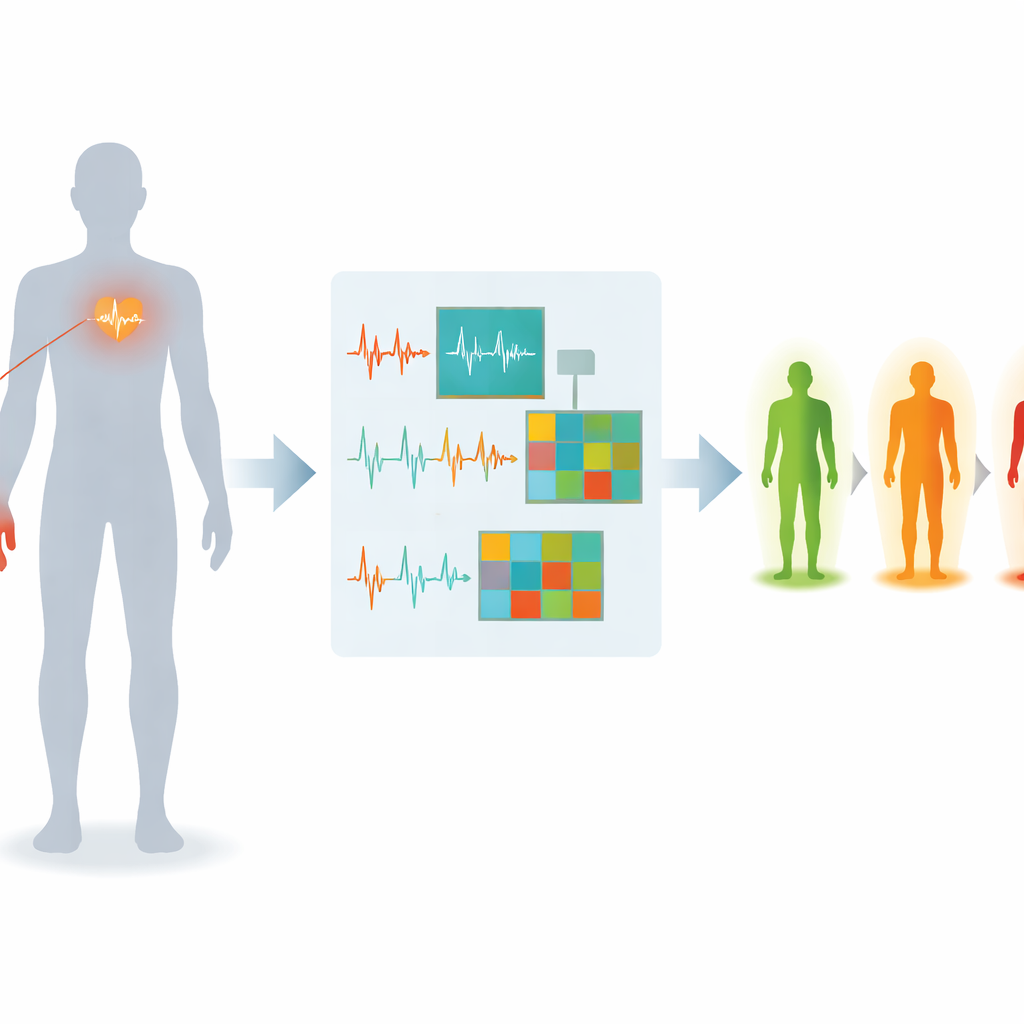
Una nueva forma de escuchar el corazón y el flujo sanguíneo
Los investigadores se centran en dos señales ya habituales en hospitales y dispositivos portátiles. Una es el electrocardiograma, o ECG, que registra la actividad eléctrica del corazón. La otra es el fotopletismograma, o PPG, una señal óptica de un sensor en la yema del dedo que rastrea el flujo sanguíneo con cada latido. Cada señal aporta una parte de la historia de cómo la diabetes afecta vasos y nervios; juntas pueden ofrecer una imagen más rica del daño nervioso temprano que cualquiera de las dos por separado. El equipo reclutó a 120 personas, incluidos voluntarios sanos, pacientes con diabetes sin diagnóstico de daño nervioso y pacientes con neuropatía confirmada. Para cada participante se registraron ECG y PPG en reposo bajo condiciones controladas para reducir fuentes habituales de ruido, como el movimiento y los cambios de temperatura.
Limpiando señales biológicas ruidosas
Las grabaciones reales del corazón y el pulso contienen multitud de perturbaciones no deseadas procedentes de la actividad muscular, la respiración y las interferencias eléctricas. Si estas distorsiones no se eliminan con cuidado, pueden ocultar los cambios sutiles que indican problemas nerviosos iniciales. El estudio presenta un método de eliminación de ruido mejorado que descompone cada señal en muchos “bloques” más simples, decide qué partes son principalmente ruido y cuáles contienen fisiología real, y luego reconstruye una versión más limpia. Para ello, los autores combinan una técnica de descomposición flexible con una estrategia de búsqueda basada en enjambre que ajusta automáticamente parámetros clave y aplican filtrado basado en wavelets solo donde resulta más útil. Las pruebas frente a varios métodos consolidados muestran que este enfoque mejora más la parte útil de las señales ECG y PPG a la vez que minimiza la distorsión.
Convertir ondas en imágenes que el ordenador puede ver
En lugar de alimentar ondas unidimensionales crudas a una red neuronal, los investigadores convierten segmentos cortos de ECG y PPG en pequeñas imágenes a color. Cada canal de color codifica un aspecto distinto de cómo evoluciona la señal en el tiempo: relaciones posicionales entre puntos del ciclo cardiaco, cambios en fase y ritmo, y patrones que se repiten de forma compleja y no lineal. Cuando estas tres vistas se apilan, forman un “retrato” compacto de cada ventana multi‑latido que resalta características dinámicas asociadas a la salud nerviosa y vascular. Al combinar varios ciclos consecutivos en lugar de un solo latido, el método captura patrones más estables e interacciones a largo alcance entre la actividad eléctrica cardíaca y la onda de pulso que recorre los vasos.
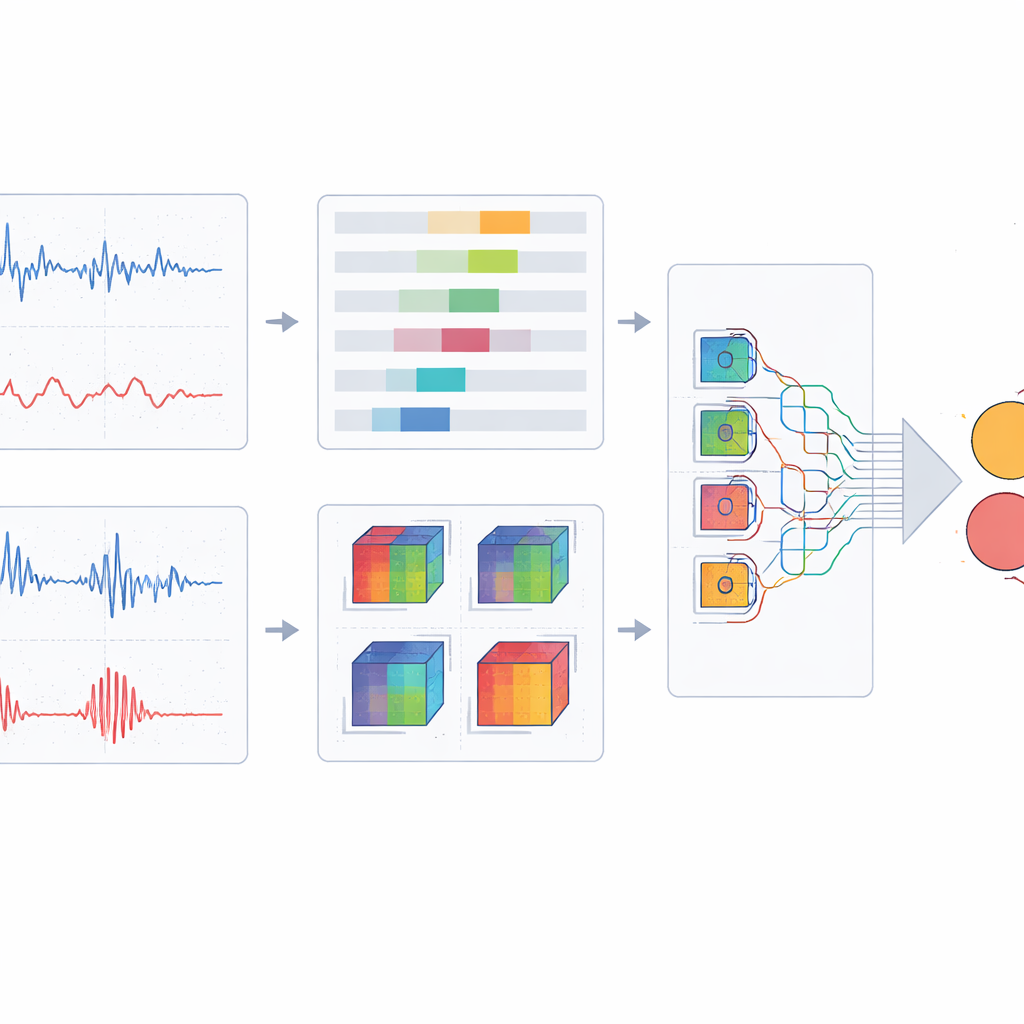
Una red ligera que se centra en lo importante
Para clasificar estas imágenes fusionadas en sanos, en riesgo o con neuropatía, el equipo diseña una arquitectura de aprendizaje profundo personalizada basada en un backbone moderno y eficiente. Sustituyen los bloques de convolución estándar por un diseño de múltiples ramas que analiza cada parche de la imagen con núcleos de distintas formas y tamaños, captando tanto detalles finos como tendencias más amplias sin un gran aumento del cómputo. Sobre esto añaden un mecanismo de atención espacial que permite a la red enfatizar regiones y patrones informativos mientras atenúa el fondo redundante. El modelo se entrena y ajusta mediante una validación cruzada cuidadosa, y su rendimiento se compara con una variedad de redes de clasificación de imágenes bien conocidas, incluidas varias arquitecturas populares basadas en convoluciones y transformers.
Qué significan los resultados para las personas con diabetes
En datos construidos a partir de múltiples ciclos cardiacos consecutivos, el sistema propuesto clasifica correctamente el estado de neuropatía en casi el 94% de los casos, con sensibilidad y precisión igualmente altas. Supera claramente tanto a los enfoques tradicionales de procesamiento de señales como a potentes modelos modernos de aprendizaje profundo, lo que indica que la combinación de un desruido más inteligente, una codificación señal‑a‑imagen más rica y un diseño de red a medida aporta valor real. Aunque el estudio se basa en datos de un solo centro y requerirá validación más amplia, apunta a un futuro en el que mediciones rutinarias e indoloras con simples pinzas y electrodos —posiblemente incluso en atención primaria o en el hogar— podrían detectar daño nervioso temprano en personas con diabetes mucho antes de que surjan complicaciones graves.
Cita: Xiao, M., Wang, F., Fang, S. et al. An improved ICEEMDAN–depth hybrid network model integrating multimodal data for the screening of diabetic peripheral neuropathy. Sci Rep 16, 10954 (2026). https://doi.org/10.1038/s41598-026-45862-x
Palabras clave: neuropatía periférica diabética, cribado no invasivo, ECG, PPG, aprendizaje profundo