Clear Sky Science · de
Ein verbessertes ICEEMDAN–Tiefen‑Hybridsystem, das multimodale Daten für das Screening der diabetischen peripheren Neuropathie integriert
Warum Nervenschäden bei Diabetes schonender geprüft werden sollten
Bei vielen Menschen mit Diabetes schleichen sich Schäden an den Nerven in Füßen und Beinen unbemerkt ein und werden erst sichtbar, wenn Schmerzen, Taubheitsgefühle oder sogar Geschwüre und Amputationen auftreten. Die heutigen Tests für diese Erkrankung, die diabetische periphere Neuropathie genannt wird, können invasiv, teuer oder in der täglichen Praxis schwer wiederholbar sein. Diese Studie untersucht einen neuen Ansatz zur Erkennung früher Nervenschäden, der ausschließlich harmlose Licht‑ und elektrische Sensoren auf der Haut verwendet, ergänzt durch intelligente Signalverarbeitung und ein speziell angepasstes Tiefenlernmodell.
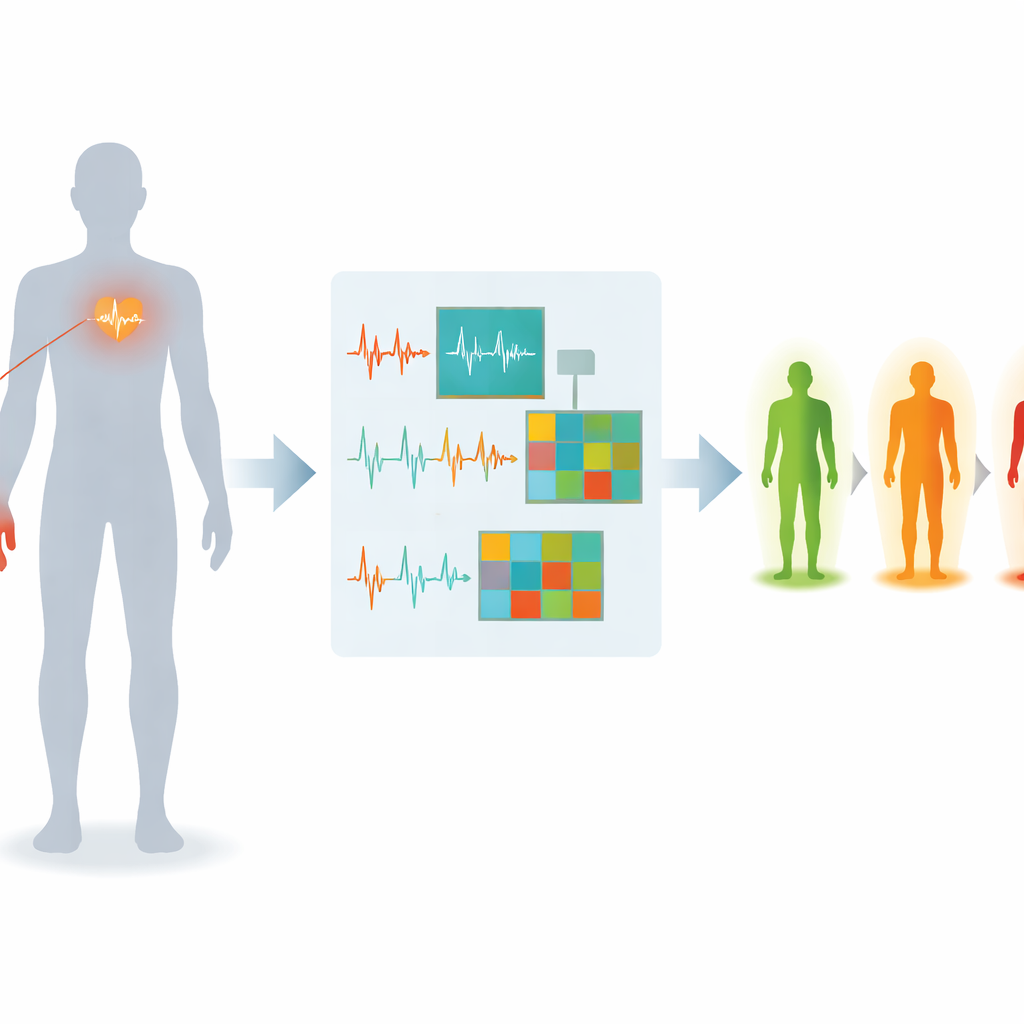
Eine neue Methode, Herz und Blutfluss zu beobachten
Die Forschenden konzentrieren sich auf zwei Signale, die bereits in Krankenhäusern und Wearables verbreitet sind. Das eine ist das Elektrokardiogramm (EKG), das die elektrische Aktivität des Herzens aufzeichnet. Das andere ist das Photoplethysmogramm (PPG), ein optisches Signal von einem Fingersensor, das den Blutfluss mit jedem Herzschlag verfolgt. Jedes Signal liefert einen Teil der Informationen darüber, wie Diabetes Blutgefäße und Nerven beeinflusst; zusammen können sie ein umfassenderes Bild früher Nervenschäden zeichnen als jedes Signal für sich. Das Team rekrutierte 120 Personen, darunter gesunde Freiwillige, Menschen mit Diabetes ohne diagnostizierte Nervenschädigung und Personen mit bestätigter Neuropathie. Für jede Teilnehmerin und jeden Teilnehmer wurden EKG und PPG in Ruhe unter kontrollierten Bedingungen aufgezeichnet, um alltägliche Störquellen wie Bewegung und Temperaturschwankungen zu minimieren.
Rauschen aus biologischen Signalen beseitigen
Aufzeichnungen von Herz- und Pulswellen im realen Umfeld sind voller unerwünschter Störungen durch Muskelaktivität, Atmung und elektrische Interferenzen. Werden diese Verzerrungen nicht sorgfältig entfernt, können sie die feinen Veränderungen überdecken, die auf frühe Nervenprobleme hinweisen. Die Studie stellt eine verbesserte Entstörungsmethode vor, die jedes Signal in viele einfachere „Bausteine“ zerlegt, entscheidet, welche Teile überwiegend Rauschen und welche echte physiologische Information enthalten, und anschließend eine sauberere Version rekonstruiert. Dazu kombinieren die Autorinnen und Autoren eine flexible Zerlegungstechnik mit einer schwarmbasierten Suchstrategie, die automatisch Schlüsselparameter abstimmt, und wenden anschließend Wavelet‑basiertes Filtern nur dort an, wo es am meisten nützt. Tests im Vergleich mit mehreren etablierten Methoden zeigen, dass dieser Ansatz den nützlichen Anteil sowohl von EKG‑ als auch von PPG‑Signalen besser hervorhebt, während Verzerrungen gering bleiben.
Wellen in Bilder verwandeln, die der Computer sehen kann
Anstatt rohe eindimensionale Wellen in ein neuronales Netz zu geben, wandeln die Forschenden kurze Segmente von EKG und PPG in kleine Farb‑bilder um. Jede Farbkanal kodiert einen anderen Aspekt der zeitlichen Entwicklung des Signals: Gesamtpositionsbeziehungen innerhalb des Herzzyklus, Veränderungen in Phase und Rhythmus sowie Muster, die sich auf komplexe, nichtlineare Weise wiederholen. Wenn diese drei Blickwinkel übereinandergelegt werden, entstehen kompakte „Porträts“ jedes mehrschlagigen Fensters, die dynamische Merkmale betonen, die mit Nerven‑ und Gefäßgesundheit verknüpft sind. Durch die Kombination mehrerer aufeinanderfolgender Zyklen statt eines einzelnen Herzschlags erfasst die Methode stabilere Muster und langfristige Wechselwirkungen zwischen der elektrischen Herzaktivität und der Pulswelle, die durch die Gefäße läuft.
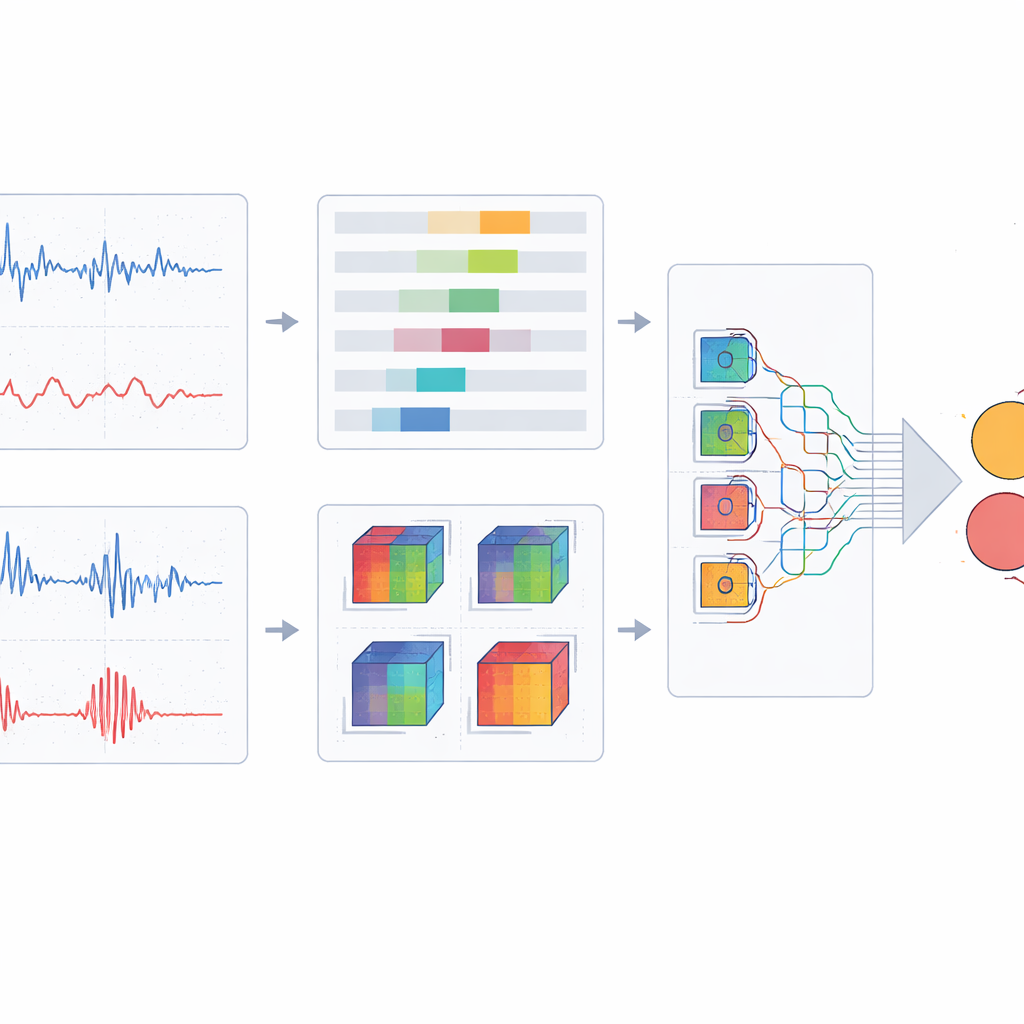
Ein leichtgewichtiges Netzwerk, das sich auf das Wesentliche konzentriert
Um diese fusionierten Bilder in gesund, gefährdet oder Neuropathie zu klassifizieren, entwirft das Team eine speziell angepasste Tiefenlernarchitektur auf Basis eines modernen, effizienten Backbones. Sie ersetzen standardmäßige Faltungsblöcke durch ein mehrgliedriges Design, das jeden Bildausschnitt mit Kernen unterschiedlicher Form und Größe betrachtet, sodass sowohl feine Details als auch gröbere Trends erfasst werden, ohne die Rechenlast stark zu erhöhen. Darauf aufbauend fügen sie einen räumlichen Aufmerksamkeitsmechanismus hinzu, der dem Netzwerk ermöglicht, informative Bereiche und Muster zu betonen und redundanten Hintergrund zu unterdrücken. Das Modell wird mittels sorgfältiger Kreuzvalidierung trainiert und abgestimmt, und seine Leistung wird mit einer Reihe bekannter Bildklassifikationsnetzwerke verglichen, darunter mehrere populäre Faltungs‑ und Transformer‑basierte Entwürfe.
Was die Ergebnisse für Menschen mit Diabetes bedeuten
Auf Basis von Daten, die mehrere Herzzyklus‑Fenster umfassen, klassifiziert das vorgeschlagene System den Neuropathiestatus in knapp 94 % der Fälle korrekt, mit ähnlich hoher Sensitivität und Präzision. Es übertrifft deutlich sowohl traditionelle Signalverarbeitungsansätze als auch starke moderne Tiefenlern‑Baselines, was darauf hindeutet, dass die Kombination aus intelligenterem Entstören, reicherer Signal‑zu‑Bild‑Kodierung und maßgeschneidertem Netzwerkdesign echten Mehrwert bietet. Obwohl die Studie auf Daten aus einem einzigen Zentrum beruht und breitere Tests benötigt, weist sie auf eine Zukunft hin, in der routinemäßige, schmerzfreie Messungen mit einfachen Clips und Elektroden – möglicherweise sogar in der hausärztlichen Versorgung oder zu Hause – frühe Nervenschäden bei Menschen mit Diabetes lange vor dem Auftreten schwerer Komplikationen erkennen könnten.
Zitation: Xiao, M., Wang, F., Fang, S. et al. An improved ICEEMDAN–depth hybrid network model integrating multimodal data for the screening of diabetic peripheral neuropathy. Sci Rep 16, 10954 (2026). https://doi.org/10.1038/s41598-026-45862-x
Schlüsselwörter: diabetische periphere Neuropathie, nichtinvasive Untersuchung, EKG, PPG, Tiefenlernen