Clear Sky Science · pt
Falta de evidências para a liberação de carga de EVs CD63 em células receptoras
Como pacotinhos minúsculos surpreenderam os cientistas
Nossas células constantemente enviam bolhas em escala nanométrica recheadas com proteínas e material genético, frequentemente descritas como pequenos pacotes para mensagens entre células. Muitos pesquisadores sugeriram que esses pacotes entregam seu conteúdo diretamente em outras células, influenciando saúde e doença de maneiras que estamos começando apenas a compreender. Este estudo examina essa ideia de forma rigorosa e conclui que, pelo menos para um tipo comum de vesícula, a entrega de carga nas células receptoras pode ser muito menos eficiente do que muitos supunham. 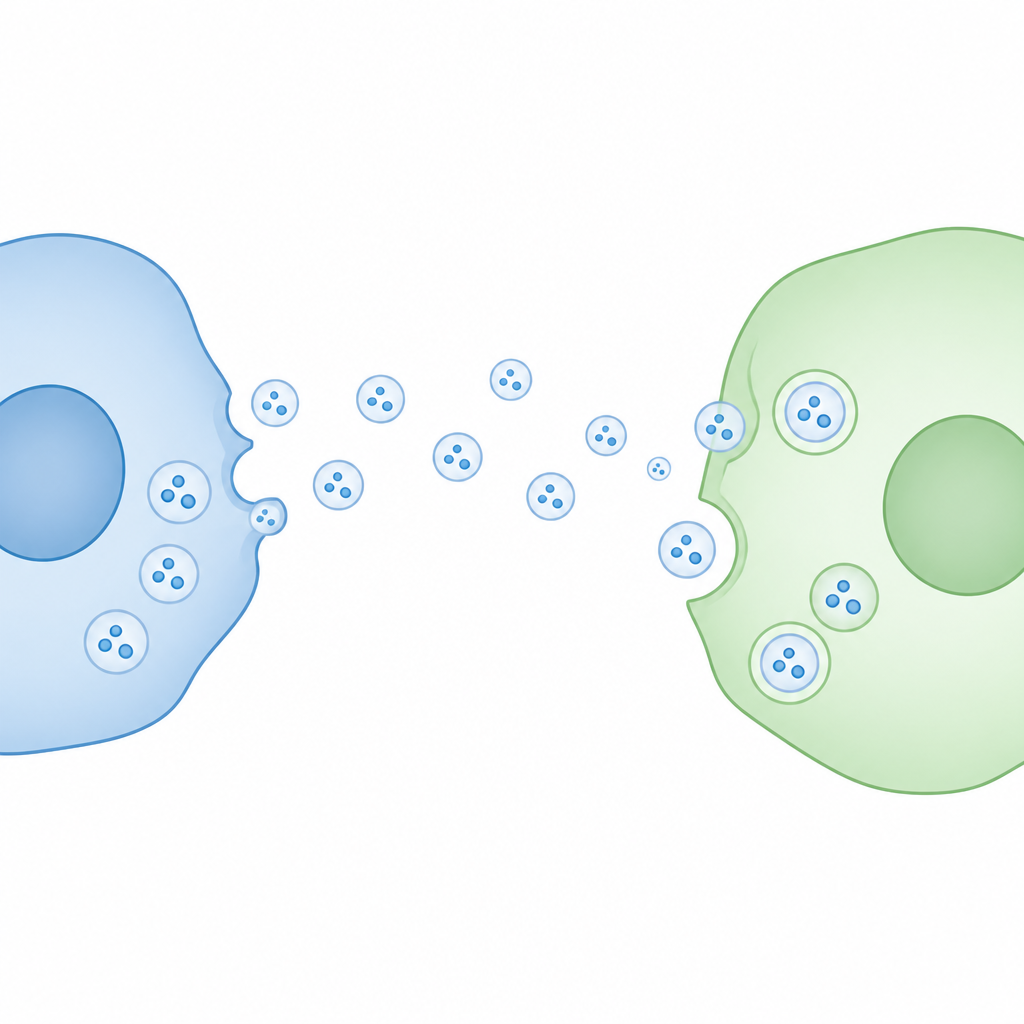
Bolhas pequenas que carregam grandes expectativas
As células liberam pequenas bolhas limitadas por membrana, chamadas vesículas extracelulares, para o meio ao seu redor. Uma subclasse importante, frequentemente chamada de exossomos, brota de compartimentos internos e transporta moléculas como proteínas e RNA. Como essas vesículas podem ser captadas por células distantes, propôs‑se amplamente que atuam como meio de comunicação celular em longa distância e como potenciais veículos para terapias futuras. Uma questão central em aberto, porém, é se sua carga realmente escapa para o interior da célula receptora, onde poderia alterar o comportamento dessa célula.
Um interruptor molecular de luz para rastrear a entrada real
Para investigar isso, os pesquisadores usaram um sistema repórter muito sensível que se comporta como um interruptor molecular de luz. Metade de uma enzima que produz luz, chamada HiBiT, foi colocada dentro das vesículas ao ser fundida à CD63, uma proteína marcador padrão que é abundante nessas bolhas. A metade complementar, LgBiT, foi produzida dentro das células receptoras, seja livre no fluido interior ou ligada às membranas endossomais, que se acredita serem pontos de pouso principais para vesículas entrantes. Se uma vesícula realmente fundisse com a membrana de uma célula e liberasse seu conteúdo interno, as duas metades se encontrariam, se encaixariam e emitiriam um brilho forte que pode ser medido com precisão.
Vesículas entram nas células, mas guardam seus segredos
Primeiro, a equipe confirmou que suas moléculas CD63 modificadas foram incorporadas corretamente às vesículas sem alterar seu tamanho ou forma. Quando essas vesículas foram misturadas com células, imagens e testes bioquímicos mostraram que elas podiam se ligar às células e provavelmente serem internalizadas por rotas de captação usuais. Ainda assim, apesar dessa interação clara, o sinal de luz esperado não aumentou ao longo do tempo. Mesmo quando o LgBiT foi concentrado nos endossomos, ou quando outra proteína de carga comum nas vesículas, HSP70, foi usada no lugar da CD63, a leitura permaneceu em níveis de fundo. Somente quando tanto as vesículas quanto as células foram artificialmente permeabilizadas com detergentes o sinal latente de luz apareceu, indicando que a carga ficou presa atrás de membranas intactas.
Máquinas de fusão virais mudam a história
Para ter certeza de que o ensaio era capaz de detectar eventos raros de fusão, os cientistas equiparam algumas vesículas com VSV G, uma proteína viral de fusão conhecida por ajudar vírus a se fundirem com membranas celulares. Desta vez, quando vesículas portadoras de VSV G e marcadas com HiBiT foram adicionadas a células com LgBiT, a luminescência aumentou claramente ao longo de algumas horas, provando que o sistema pode reportar a liberação de carga quando a fusão realmente ocorre. Curiosamente, apenas uma fração pequena das vesículas carregava essa proteína viral, ainda assim o sinal foi robusto, destacando a sensibilidade do método. As vesículas com VSV G também foram internalizadas com um pouco mais de eficiência, mas o grande aumento na emissão de luz mostrou que a fusão — e não apenas a captação — era a etapa crítica ausente nas vesículas não modificadas. 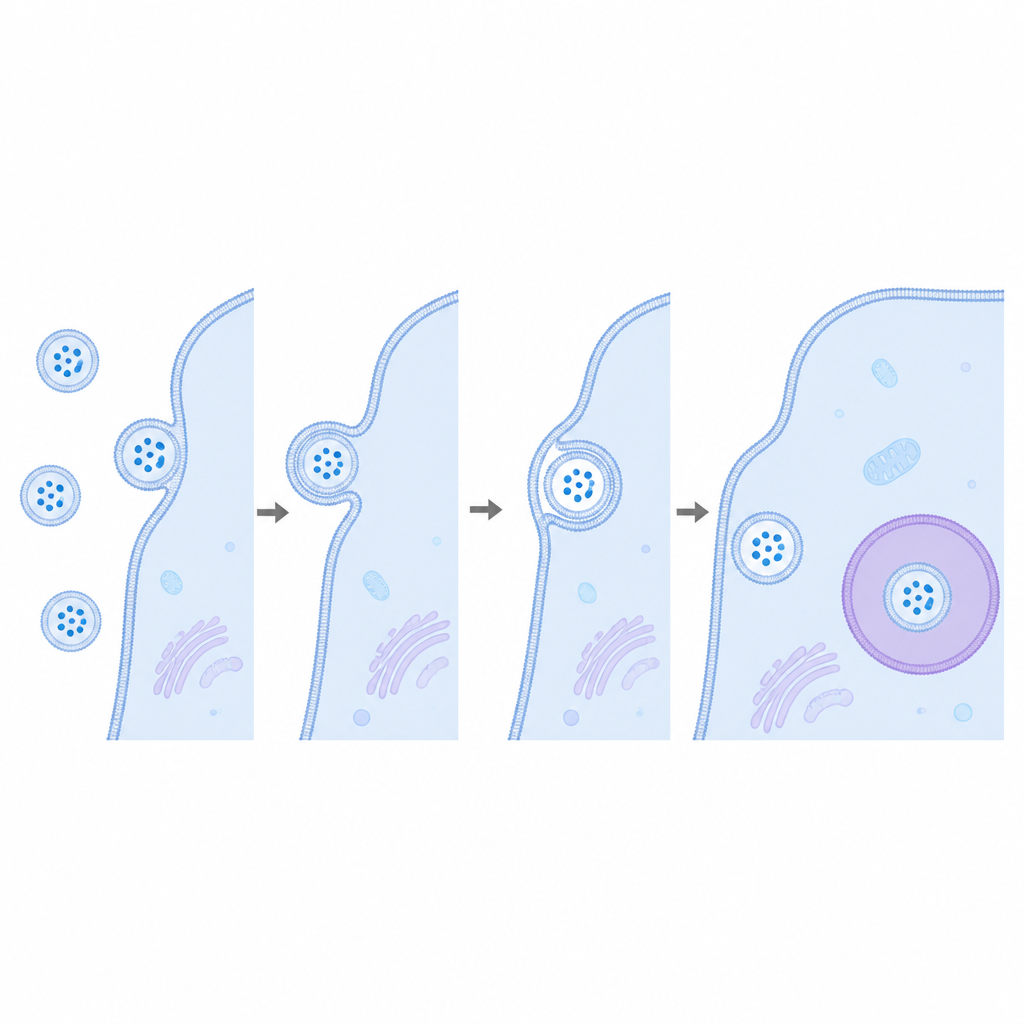
Repensando como essas bolhas se comunicam entre células
Em conjunto, o trabalho sugere que, em condições de laboratório padrão, vesículas positivas para CD63 de células renais humanas raramente, se é que alguma vez, se fundem com as membranas das células receptoras para derramar sua carga interna no interior celular. Elas podem ainda se ligar, ser engolidas em compartimentos internos ou sinalizar por interações de superfície, mas a entrega direta de sua carga interna parece ineficiente sem ajudantes de fusão adicionados, como proteínas virais. Para o leitor em geral, a mensagem é que esses pacotes naturais feitos por células podem não ser os mensageiros diretos que muitos imaginavam, e que os cientistas precisarão repensar tanto como as células se comunicam por meio deles quanto como melhor aproveitá‑los para tratamentos futuros.
Citação: Askarian-Amiri, S., Weissenhorn, W., Sadoul, R. et al. Lack of evidence for cargo release of CD63-EVs into recipient cells. Sci Rep 16, 15164 (2026). https://doi.org/10.1038/s41598-026-45021-2
Palavras-chave: vesículas extracelulares, exossomos, comunicação celular, fusão de membrana, ensaio de nanoluciferase