Clear Sky Science · fr
Pénurie de preuves concernant la libération de cargaison des vésicules CD63-EVs dans les cellules réceptrices
Comment de minuscules paquets cellulaires ont surpris les scientifiques
Nos cellules envoient en permanence des bulles nanoscale remplies de protéines et de matériel génétique, souvent décrites comme de petits colis pour la communication cellulaire. De nombreux chercheurs ont suggéré que ces colis livrent leur contenu directement dans d’autres cellules, influençant la santé et la maladie d’une manière que nous commençons à peine à comprendre. Cette étude examine de près cette idée et montre que, du moins pour un type courant de vésicule, la livraison de cargaison dans les cellules réceptrices peut être bien moins efficace que beaucoup ne le pensaient. 
Petites bulles qui portent de grandes attentes
Les cellules libèrent de petites bulles entourées de membrane appelées vésicules extracellulaires dans leur environnement. Une sous-classe majeure, souvent appelée exosomes, bourgeonne à partir de compartiments internes et transporte des molécules telles que des protéines et des ARN. Parce que ces vésicules peuvent être internalisées par des cellules distantes, elles ont été largement proposées comme moyen de communication à longue distance entre cellules et comme vecteurs potentiels pour de futures thérapies. Une question clé reste toutefois de savoir si leur cargaison s’échappe réellement dans l’intérieur de la cellule réceptrice, où elle pourrait modifier le comportement de cette cellule.
Un interrupteur moléculaire pour suivre la véritable entrée
Pour répondre à cette question, les chercheurs ont utilisé un système rapporteur très sensible qui se comporte comme un interrupteur moléculaire lumineux. Une moitié d’une enzyme productrice de lumière, appelée HiBiT, a été placée à l’intérieur des vésicules en la fusionnant à CD63, une protéine marqueur standard abondante dans ces bulles. La moitié complémentaire, LgBiT, a été produite à l’intérieur des cellules réceptrices, soit libre dans le cytosol, soit attachée aux membranes endosomales, qui sont considérées comme des points d’arrivée majeurs pour les vésicules entrantes. Si une vésicule fusionnait vraiment avec une membrane cellulaire et libérait son contenu interne, les deux moitiés se rencontreraient, s’assembleraient et émettraient une forte lueur mesurable avec précision.
Les vésicules entrent dans les cellules mais gardent leurs secrets
Dans un premier temps, l’équipe a confirmé que leurs molécules CD63 modifiées étaient correctement incorporées dans les vésicules sans en modifier la taille ni la forme. Lorsque ces vésicules ont été placées en présence de cellules, l’imagerie et les tests biochimiques ont montré qu’elles pouvaient se lier aux cellules et être probablement internalisées par des voies d’endocytose classiques. Pourtant, malgré cette interaction évidente, le signal lumineux attendu n’augmentait pas avec le temps. Même lorsque LgBiT était concentré sur les endosomes, ou lorsque HSP70, une autre protéine cargo courante des vésicules, était utilisée à la place de CD63, la lecture restait au niveau du bruit de fond. Ce n’est que lorsque vésicules et cellules ont été artificiellement perméabilisées avec des détergents que le signal lumineux latent est apparu, indiquant que la cargaison restait piégée derrière des membranes intactes.
La machinerie de fusion virale change la donne
Pour s’assurer que le test pouvait détecter des événements de fusion rares, les scientifiques ont équipé certaines vésicules de VSV G, une protéine de fusion virale connue pour aider les virus à fusionner avec des membranes cellulaires. Cette fois, lorsque des vésicules portant VSV G et marquées par HiBiT ont été ajoutées à des cellules exprimant LgBiT, la luminescence a augmenté de façon nette sur quelques heures, prouvant que le système peut signaler la libération de cargaison lorsque la fusion a effectivement lieu. Fait intéressant, seule une petite fraction des vésicules portait cette protéine virale, et pourtant le signal était robuste, illustrant la sensibilité de la méthode. Les vésicules avec VSV G étaient également internalisées un peu plus efficacement, mais la hausse beaucoup plus importante du signal lumineux montre que la fusion, et non l’endocytose seule, était l’étape critique manquante chez les vésicules non modifiées. 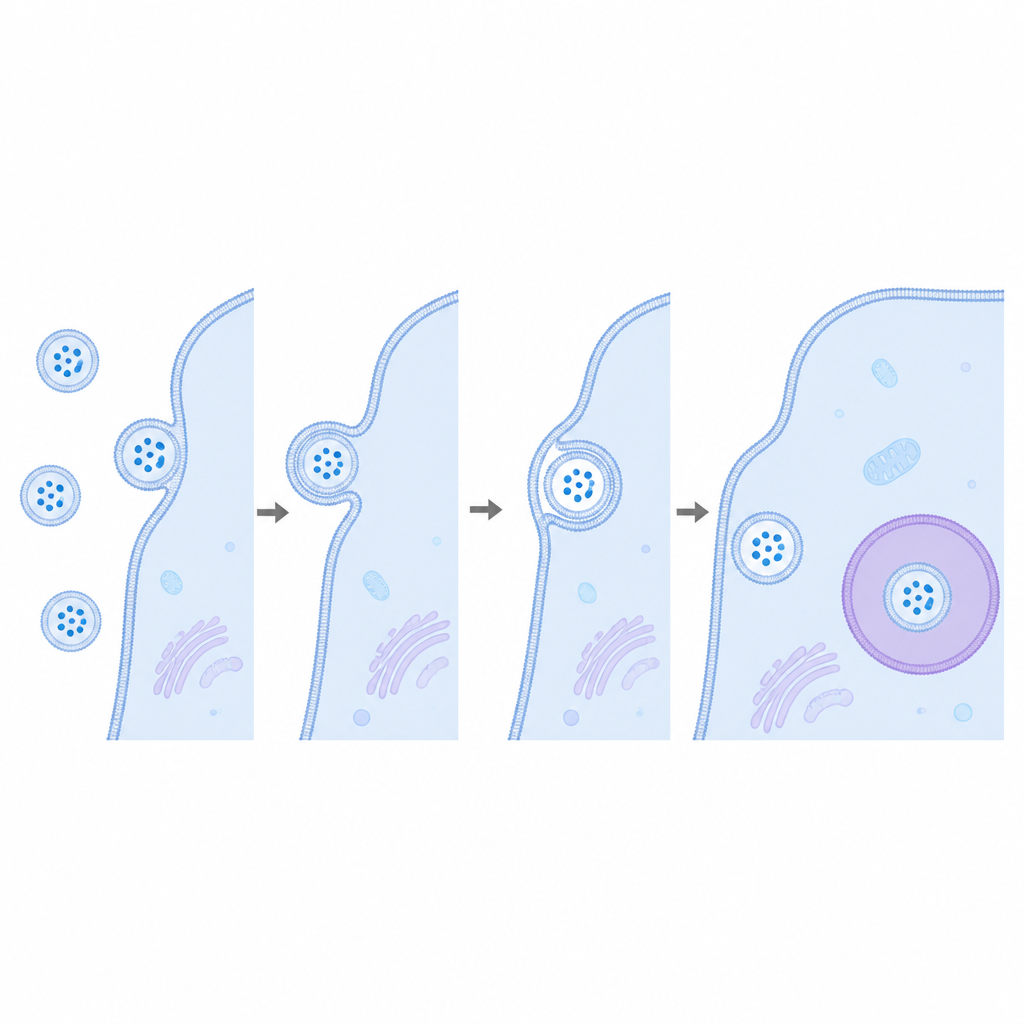
Repenser la façon dont ces bulles communiquent entre cellules
Dans l’ensemble, le travail suggère que, dans des conditions de laboratoire standard, les vésicules CD63 positives provenant de cellules rénales humaines fusionnent rarement, voire jamais, avec les membranes des cellules réceptrices pour déverser leur cargaison interne dans le cytosol. Elles peuvent toutefois rester à la surface, être avalées dans des compartiments internes ou agir par des interactions superficielles, mais la livraison directe de leur contenu interne semble inefficace sans aide de fusion supplémentaire comme des protéines virales. Pour un lecteur général, le message est que ces colis naturels fabriqués par les cellules ne sont peut‑être pas des transporteurs de messages aussi directs que beaucoup l’avaient imaginé, et que les scientifiques devront repenser à la fois la manière dont les cellules communiquent via ces vésicules et la façon de les exploiter au mieux pour de futurs traitements.
Citation: Askarian-Amiri, S., Weissenhorn, W., Sadoul, R. et al. Lack of evidence for cargo release of CD63-EVs into recipient cells. Sci Rep 16, 15164 (2026). https://doi.org/10.1038/s41598-026-45021-2
Mots-clés: vésicules extracellulaires, exosomes, communication cellulaire, fusion membranaire, essai nanoluciférase