Clear Sky Science · ar
غياب الأدلة على إطلاق الحمولة من الحويصلات الحاملة CD63 داخل الخلايا المستقبلة
كيف فاجأت حزَم الخلايا الصغيرة العلماء
ترسل خلايانا باستمرار فقاعات نانوية الحجم محمّلة بالبروتينات والمادة الوراثية، وغالباً ما توصف بأنها طرود صغيرة للرسائل بين الخلايا. اقترح العديد من الباحثين أن هذه الطرود تُسلم محتوياتها مباشرةً إلى خلايا أخرى، مما يؤثر على الصحة والمرض بطرق نبدأ للتو في فهمها. تُلقي هذه الدراسة نظرة نقدية على هذه الفكرة وتجد أنه، على الأقل لنوع شائع من الحويصلات، فإن تسليم الحمولة إلى الخلايا المستقبِلة قد يكون أقل كفاءة مما افترضه الكثيرون. 
فقاعات صغيرة تحمل توقعات كبيرة
تفرز الخلايا فقاعات صغيرة محاطة بغشاء تُسمى الحويصلات خارج الخلية إلى محيطها. فرع رئيسي منها، يُطلق عليه غالباً الإكسوسومات، ينشأ من مقصورات داخلية ويحمل جزيئات مثل البروتينات والـRNA. وبما أن هذه الحويصلات يمكن أن تُؤخذ up من قبل خلايا بعيدة، فقد اقترحت على نطاق واسع كوسيلة للتواصل الخلوي بعيد المدى وكناقلات محتملة للعلاجات المستقبلية. لكن سؤالاً أساسياً ما زال مفتوحاً: هل تخرج حمولتها فعلاً إلى داخل الخلية المستقبِلة، حيث يمكن أن تغير سلوك تلك الخلية؟
مفتاح ضوئي جزيئي لتتبع الدخول الحقيقي
لمعالجة هذا السؤال، استخدم الباحثون نظام إبلاغ حساس جداً يتصرف كمفتاح ضوئي جزيئي. وُضع نصف إنزيم مُنتج للضوء، يسمى HiBiT، داخل الحويصلات بدمجه مع CD63، وهو بروتين علامة معياري موجود بغزارة في هذه الفقاعات. النصف المتمم، LgBiT، تم إنتاجه داخل الخلايا المستقبِلة، إما حراً في السيتوسول أو مربوطاً بأغشية الإندوزومات، التي يُعتقد أنها مواقع هبوط رئيسية للحويصلات الواردة. إذا اندمجت الحويصلة حقاً مع غشاء الخلية وأطلقت محتوياتها الداخلية، فسيلتقي النصفان، ويتشابكا، ويصدران توهجاً قوياً يمكن قياسه بدقة.
الحويصلات تدخل الخلايا لكن تحتفظ بأسرارها
أولاً، أكدت الفريق أن جزيئات CD63 المعدلة قد دمِجت بشكل صحيح في الحويصلات دون تغيير حجمها أو شكلها. عندما خلطوا هذه الحويصلات مع الخلايا، أظهرت التصوير والاختبارات الكيميائية الحيوية أنها يمكن أن ترتبط بالخلايا وربما تُسحب إلى الداخل عبر طرق الامتزاز المعتادة. ومع ذلك، على الرغم من هذا التفاعل الواضح، لم يرتفع الإشارة الضوئية المتوقعة مع مرور الوقت. حتى عندما ركز LgBiT على الإندوزومات، أو عندما استُخدم بروتين حمولة حويصلات شائع آخر، HSP70، بدلاً من CD63، ظل العائد عند مستويات الخلفية. لم يظهر الإشارة الكامنة إلا عندما تم تمزق الغشاء في كل من الحويصلات والخلايا بشكل مصطنع باستخدام المنظفات، مما يشير إلى أن الحمولة بقيت محبوسة خلف أغشية سليمة.
آلية اندماج فيروسية تغيّر القصة
للتأكد من أن الاختبار قادر على اكتشاف أحداث الاندماج النادرة، زود العلماء بعض الحويصلات ببروتين اندماج فيروسي يُدعى VSV G، المعروف بمساعدته الفيروسات على الاندماج مع أغشية الخلايا. هذه المرة، عندما أضيفت الحويصلات الحاملة لـ VSV G والمعلَّمة بـ HiBiT إلى خلايا LgBiT، ارتفعت اللمعان بوضوح على مدى عدة ساعات، مما يثبت أن النظام يمكنه الإبلاغ عن إطلاق الحمولة عندما يحدث الاندماج فعلاً. والمثير للاهتمام أن جزءاً صغيراً فقط من الحويصلات كان يحمل هذا البروتين الفيروسي، ومع ذلك كانت الإشارة قوية، ما يبرز حساسية الطريقة. كما أن الحويصلات الحاملة لـ VSV G وُصفت بأنها تُؤخذ بكفاءة أكبر بعض الشيء، لكن الارتفاع الأكبر بكثير في خرج الضوء أظهر أن الاندماج، وليس مجرد الامتزاز أو الابتلاع، كان الخطوة الحاسمة المفقودة في الحويصلات غير المُعدّلة. 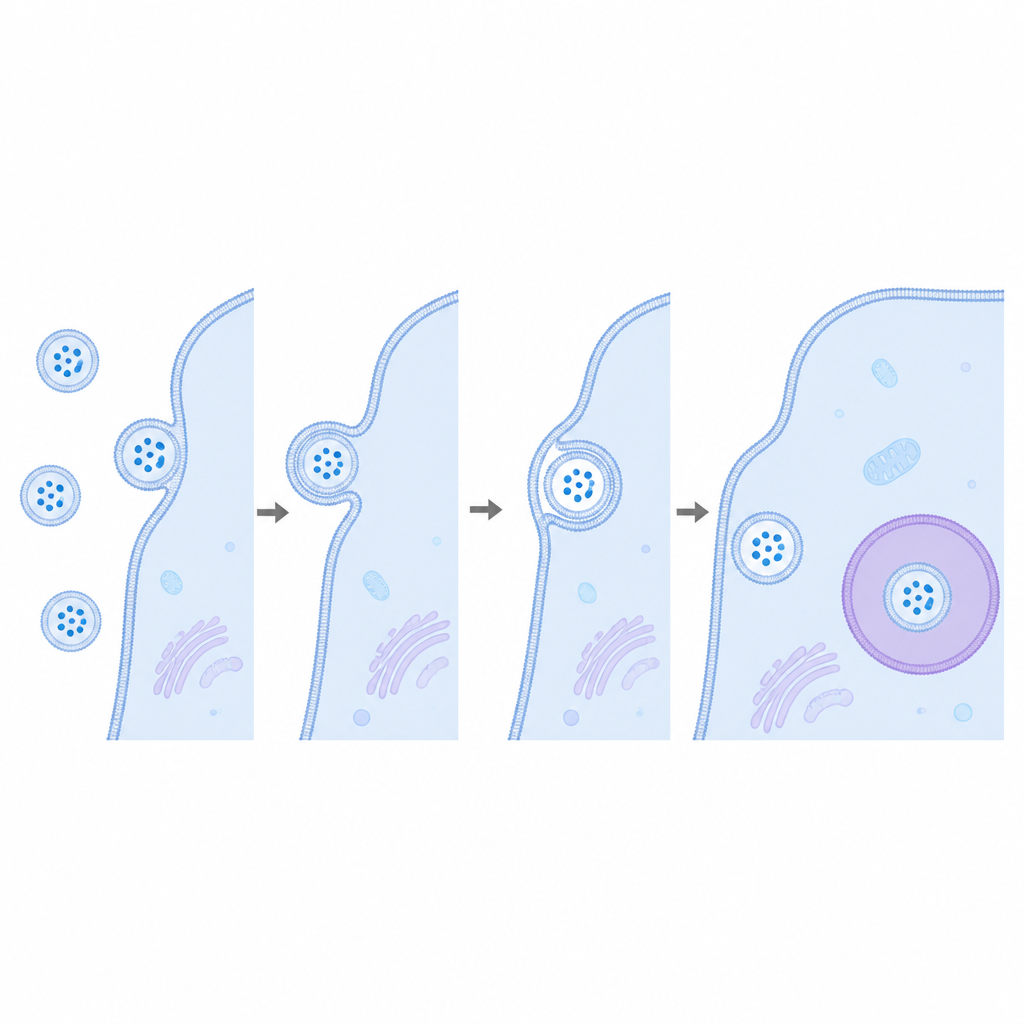
إعادة التفكير في كيفية تواصل هذه الفقاعات بين الخلايا
مجتمعة، تشير النتائج إلى أنه تحت ظروف المختبر القياسية، نادراً ما، إن حدث ذلك، تندمج الحويصلات الإيجابية لـ CD63 من خلايا كلوية بشرية مع أغشية الخلايا المستقبلة لتفرغ حمولتها الداخلية داخل الحيز الخلوي. قد تبقى مرتبطة، أو تُبتلع إلى مقصورات داخلية، أو تُرسل إشارات عبر تفاعلات سطحية، لكن التسليم المباشر لحمولتها الداخلية يبدو غير فعال دون مساعدات اندماج مثل البروتينات الفيروسية. والرسالة للقارئ العام هي أن هذه الطرود الطبيعية المصنوعة من الخلايا قد لا تكون ناقلات رسائل مباشرة وبسيطة كما تخيل الكثيرون، وأن على العلماء إعادة التفكير في كيفية تواصل الخلايا عبرها وكيفية استغلالها بأفضل شكل للعلاجات المستقبلية.
الاستشهاد: Askarian-Amiri, S., Weissenhorn, W., Sadoul, R. et al. Lack of evidence for cargo release of CD63-EVs into recipient cells. Sci Rep 16, 15164 (2026). https://doi.org/10.1038/s41598-026-45021-2
الكلمات المفتاحية: الحويصلات خارج الخلية, الإكسوسومات, الاتصال الخلوي, اندماج الغشاء, اختبار النانولوسيفيراز