Clear Sky Science · es
Falta de evidencia de liberación de carga de EVs CD63 dentro de células receptoras
Cómo unas minúsculas 'paquetes' celulares sorprendieron a los científicos
Nuestras células envían constantemente burbujas de tamaño nanométrico cargadas con proteínas y material genético, a menudo descritas como pequeños paquetes para la mensajería entre células. Muchos investigadores han sugerido que estos paquetes entregan su contenido directamente a otras células, influyendo en la salud y la enfermedad de formas que apenas comenzamos a comprender. Este estudio examina rigurosamente esa idea y encuentra que, al menos para un tipo común de vesícula, la entrega de carga a las células receptoras podría ser mucho menos eficiente de lo que muchos han supuesto. 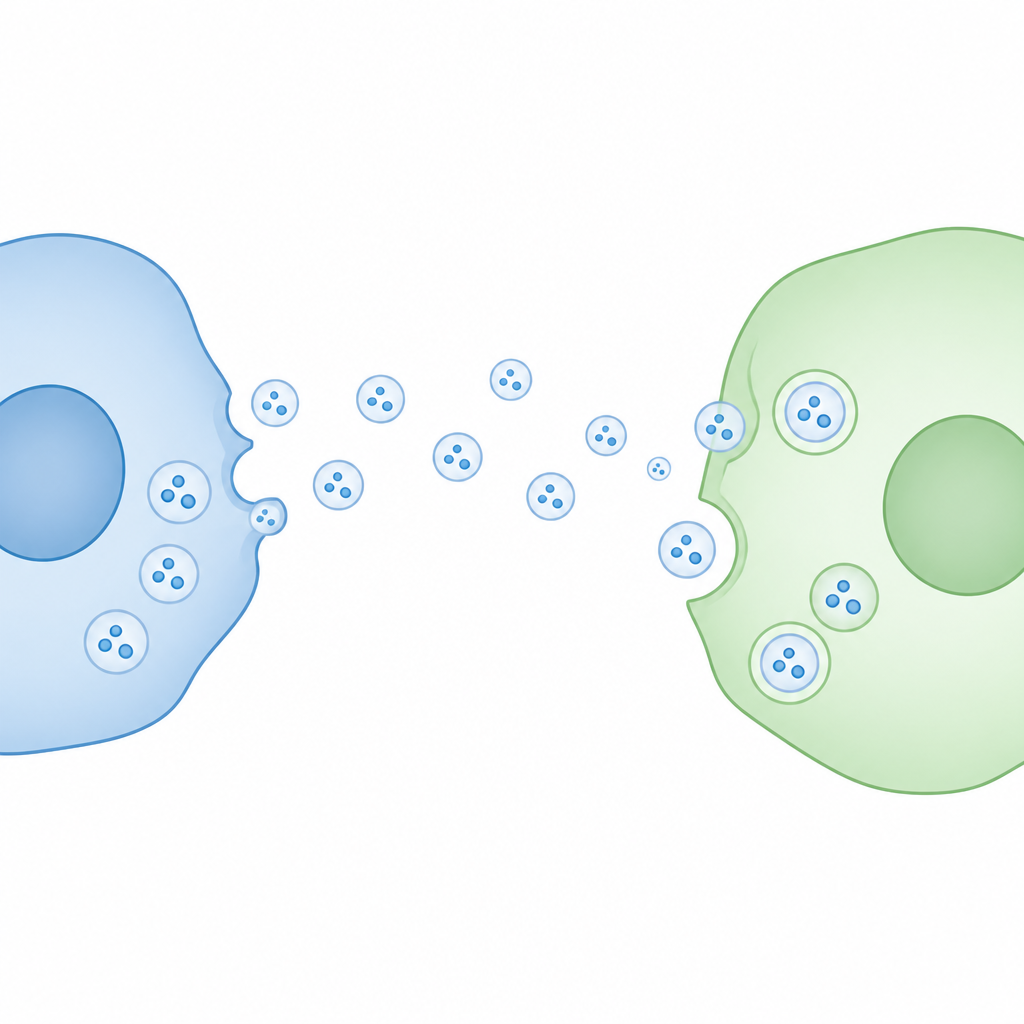
Pequeñas burbujas que cargan grandes expectativas
Las células liberan diminutas burbujas delimitadas por membrana llamadas vesículas extracelulares en su entorno. Una subclase importante, a menudo llamada exosomas, brota de compartimentos internos y transporta moléculas como proteínas y ARN. Dado que estas vesículas pueden ser captadas por células distantes, se las ha propuesto ampliamente como un medio de comunicación celular a larga distancia y como posibles vehículos para terapias futuras. Sin embargo, una cuestión clave abierta es si su carga realmente escapa al interior de la célula receptora, donde podría cambiar el comportamiento de esa célula.
Un interruptor molecular de luz para rastrear la entrada real
Para abordar esto, los investigadores usaron un sistema reportero muy sensible que actúa como un interruptor molecular de luz. Una mitad de una enzima productora de luz, llamada HiBiT, se colocó dentro de las vesículas fusionándola con CD63, una proteína marcadora estándar que es abundante en estas burbujas. La mitad complementaria, LgBiT, se produjo dentro de las células receptoras, ya sea libre en el fluido interior o unida a membranas endosómicas, que se consideran principales puntos de llegada para las vesículas entrantes. Si una vesícula realmente se fusionara con una membrana celular y liberara su contenido interno, las dos mitades se encontrarían, se acoplarían y emitirían un brillo intenso que puede medirse con precisión.
Las vesículas entran en las células pero guardan sus secretos
Primero, el equipo confirmó que sus moléculas CD63 diseñadas se incorporaron correctamente en las vesículas sin cambiar su tamaño ni forma. Cuando estas vesículas se mezclaron con células, la imagenología y las pruebas bioquímicas mostraron que podían unirse a las células y probablemente ser internalizadas por rutas de captura habituales. Aun así, a pesar de esta interacción clara, la señal luminosa esperada no aumentó con el tiempo. Incluso cuando LgBiT se concentró en endosomas, o cuando se empleó otra proteína de carga vesicular común, HSP70, en lugar de CD63, la lectura se mantuvo en niveles de fondo. Solo cuando tanto las vesículas como las células fueron permeabilizadas artificialmente con detergentes apareció la señal latente, lo que indica que la carga permanecía atrapada detrás de membranas intactas.
La maquinaria de fusión viral cambia la historia
Para asegurarse de que el ensayo podía detectar eventos de fusión raros, los científicos equiparon algunas vesículas con VSV G, una proteína de fusión viral conocida por ayudar a los virus a fusionarse con membranas celulares. Esta vez, cuando se añadieron a células con LgBiT las vesículas portadoras de HiBiT y VSV G, la luminiscencia aumentó claramente durante unas pocas horas, demostrando que el sistema puede informar la liberación de carga cuando la fusión ocurre realmente. Curiosamente, solo una pequeña fracción de las vesículas llevaba esta proteína viral, pero la señal fue robusta, lo que resalta la sensibilidad del método. Las vesículas con VSV G también se internalizaron algo más eficientemente, pero el aumento mucho mayor en la emisión de luz mostró que la fusión, no solo la captación, era el paso crítico que faltaba en las vesículas sin modificar. 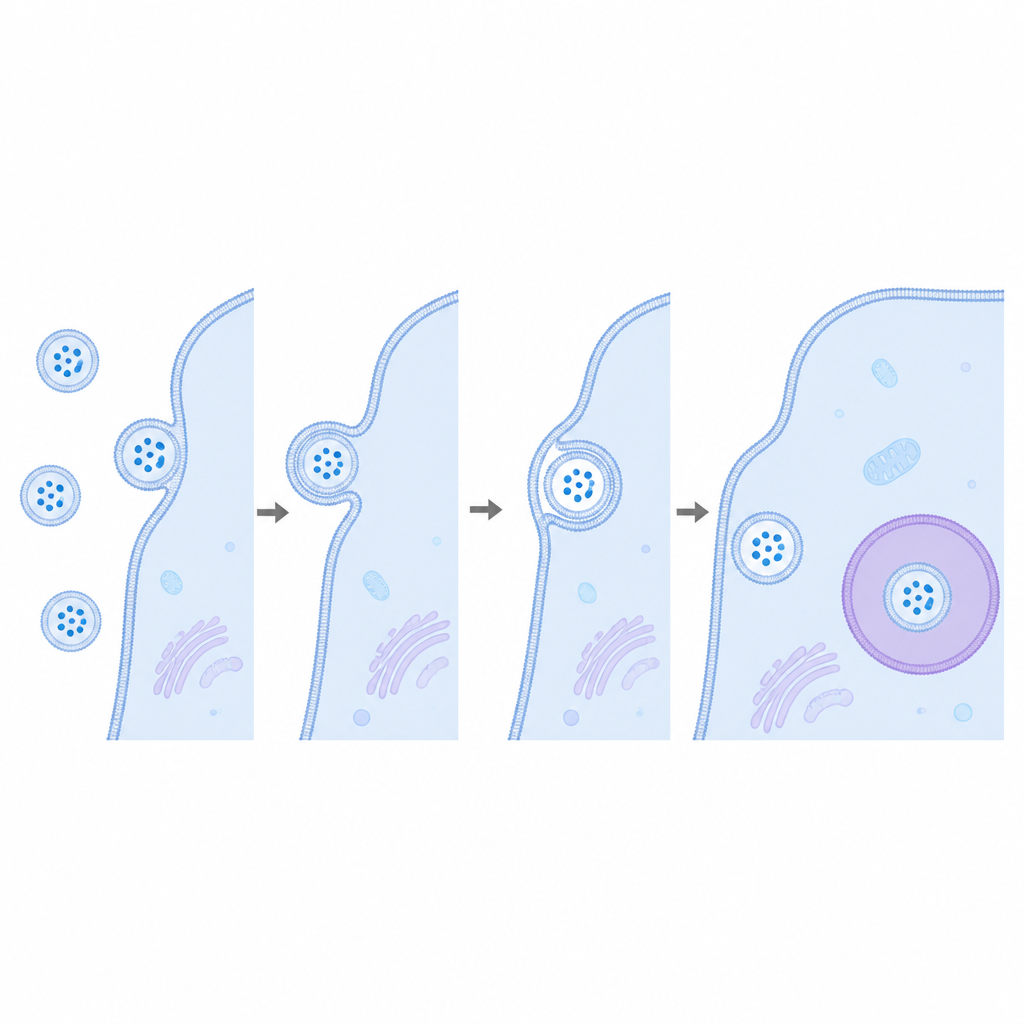
Repensar cómo estas burbujas comunican entre células
En conjunto, el trabajo sugiere que, bajo condiciones estándar de laboratorio, las vesículas positivas para CD63 procedentes de células renales humanas rara vez, si es que lo hacen, se fusionan con las membranas de las células receptoras para verter su carga interna en el interior celular. Pueden aún unirse, ser engullidas hacia compartimentos internos o señalizar mediante interacciones superficiales, pero la entrega directa de su carga interna parece ineficiente sin ayudantes de fusión añadidos, como proteínas virales. Para un lector general, el mensaje es que estos paquetes naturales hechos por células pueden no ser los portadores de mensajes tan directos que muchos imaginaban, y que los científicos deberán replantear tanto cómo las células se comunican mediante ellos como la mejor manera de aprovecharlos para tratamientos futuros.
Cita: Askarian-Amiri, S., Weissenhorn, W., Sadoul, R. et al. Lack of evidence for cargo release of CD63-EVs into recipient cells. Sci Rep 16, 15164 (2026). https://doi.org/10.1038/s41598-026-45021-2
Palabras clave: vesículas extracelulares, exosomas, comunicación celular, fusión de membranas, ensayo de nanoluciferasa