Clear Sky Science · it
Scarse prove del rilascio di contenuto degli EV CD63 nelle cellule riceventi
Come le piccole confezioni cellulari hanno sorpreso gli scienziati
Le nostre cellule inviano costantemente piccole bolle nanometriche piene di proteine e materiale genetico, spesso descritte come piccoli pacchetti per la comunicazione cellula‑cellula. Molti ricercatori hanno ipotizzato che questi pacchetti consegnino il loro contenuto direttamente ad altre cellule, influenzando salute e malattia in modi che stiamo solo iniziando a comprendere. Questo studio esamina a fondo quell'idea e rileva che, almeno per un tipo comune di vescicola, la consegna del contenuto nelle cellule riceventi potrebbe essere molto meno efficiente di quanto molti abbiano supposto. 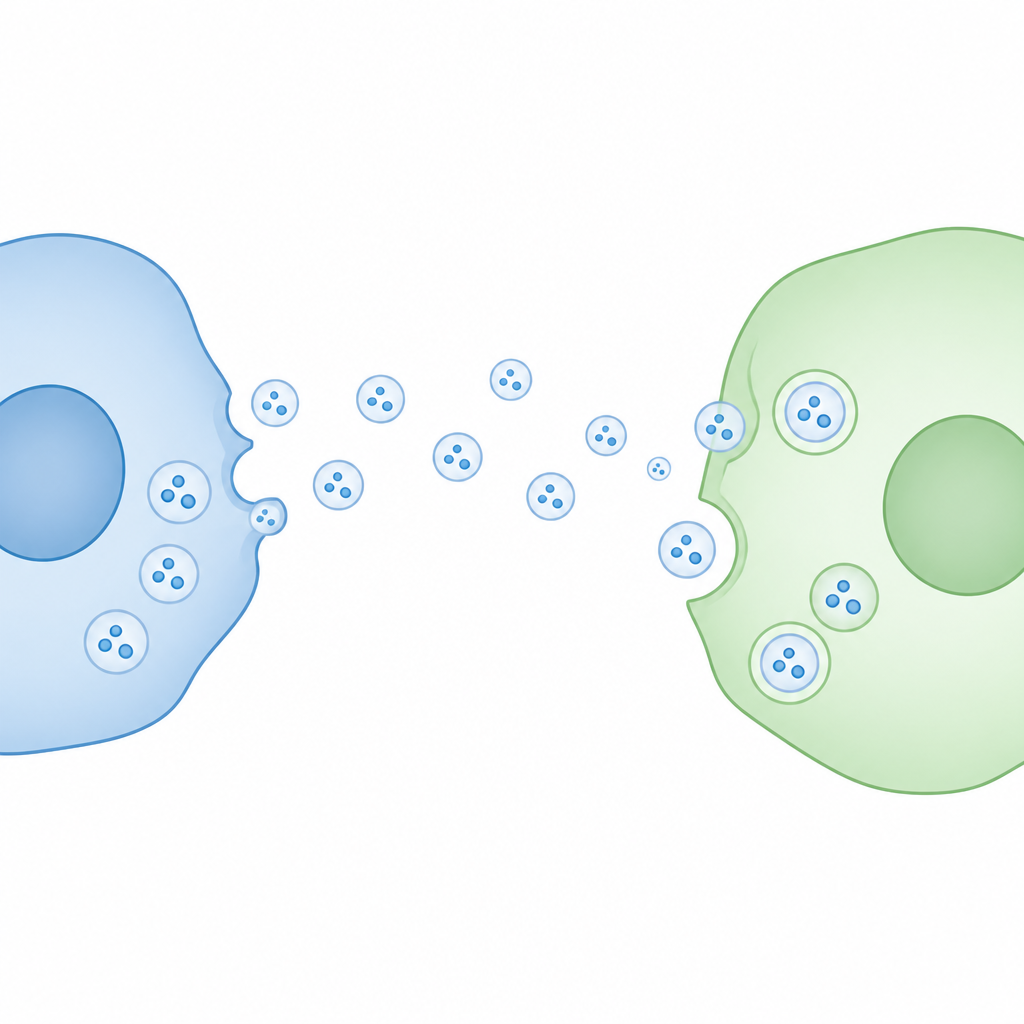
Piccole bolle che portano grandi aspettative
Le cellule rilasciano nell'ambiente minuscole bolle delimitate da membrana chiamate vescicole extracellulari. Una sottoclasse importante, spesso chiamata esosomi, si origina da compartimenti interni e trasporta molecole come proteine e RNA. Poiché queste vescicole possono essere assorbite da cellule distanti, sono state ampiamente proposte come mezzo per comunicazioni a lunga distanza tra cellule e come potenziali veicoli per future terapie. Una questione fondamentale, tuttavia, è se il loro carico scappi davvero nell'interno della cellula ricevente, dove potrebbe modificare il comportamento di quella cellula.
Un interruttore molecolare per tracciare l'ingresso reale
Per rispondere a questo, i ricercatori hanno usato un sistema di rilevamento molto sensibile che funziona come un interruttore molecolare di luce. Una metà di un enzima produttrice di luce, chiamata HiBiT, è stata posizionata all'interno delle vescicole fondendola a CD63, una proteina marcatore standard abbondante in queste bolle. L'altra metà corrispondente, LgBiT, è stata espressa all'interno delle cellule riceventi, libera nel fluido interno o legata alle membrane endosomiali, che si pensa siano principali siti di arrivo per le vescicole in entrata. Se una vescicola si fosse davvero fusa con una membrana cellulare e avesse rilasciato il suo contenuto interno, le due metà si sarebbero incontrate, agganciate e avrebbero emesso un forte bagliore misurabile con precisione.
Le vescicole entrano nelle cellule ma tengono i loro segreti
Per prima cosa, il gruppo ha confermato che le molecole CD63 ingegnerizzate erano correttamente incorporate nelle vescicole senza alterarne dimensione o forma. Quando queste vescicole sono state mescolate con cellule, l'imaging e i test biochimici hanno mostrato che potevano legarsi alle cellule ed essere probabilmente internalizzate tramite le vie di assorbimento standard. Eppure, nonostante questa chiara interazione, il segnale luminoso atteso non è aumentato nel tempo. Anche quando LgBiT era concentrato sugli endosomi, o quando un'altra proteina cargo comune delle vescicole, HSP70, è stata usata al posto di CD63, la lettura è rimasta a livelli di fondo. Solo quando sia le vescicole sia le cellule sono state artificialmente permeabilizzate con detergenti è apparso il segnale luminoso latente, indicando che il carico restava intrappolato dietro membrane intatte.
La macchina di fusione virale cambia la storia
Per accertarsi che il test fosse capace di rilevare eventi di fusione rari, gli scienziati hanno dotato alcune vescicole della proteina virale di fusione VSV G, nota per aiutare i virus a fondersi con le membrane cellulari. Questa volta, quando vescicole portatrici di VSV G e con il tag HiBiT sono state aggiunte a cellule con LgBiT, la luminescenza è aumentata chiaramente nel giro di poche ore, provando che il sistema può riportare il rilascio del carico quando la fusione avviene veramente. È interessante che solo una piccola frazione delle vescicole portasse questa proteina virale, eppure il segnale è stato robusto, evidenziando la sensibilità del metodo. Le vescicole con VSV G sono state anche assorbite con una certa maggiore efficienza, ma il forte aumento della luce mostra che la fusione, non solo l'assorbimento, era il passaggio critico mancante nelle vescicole non modificate. 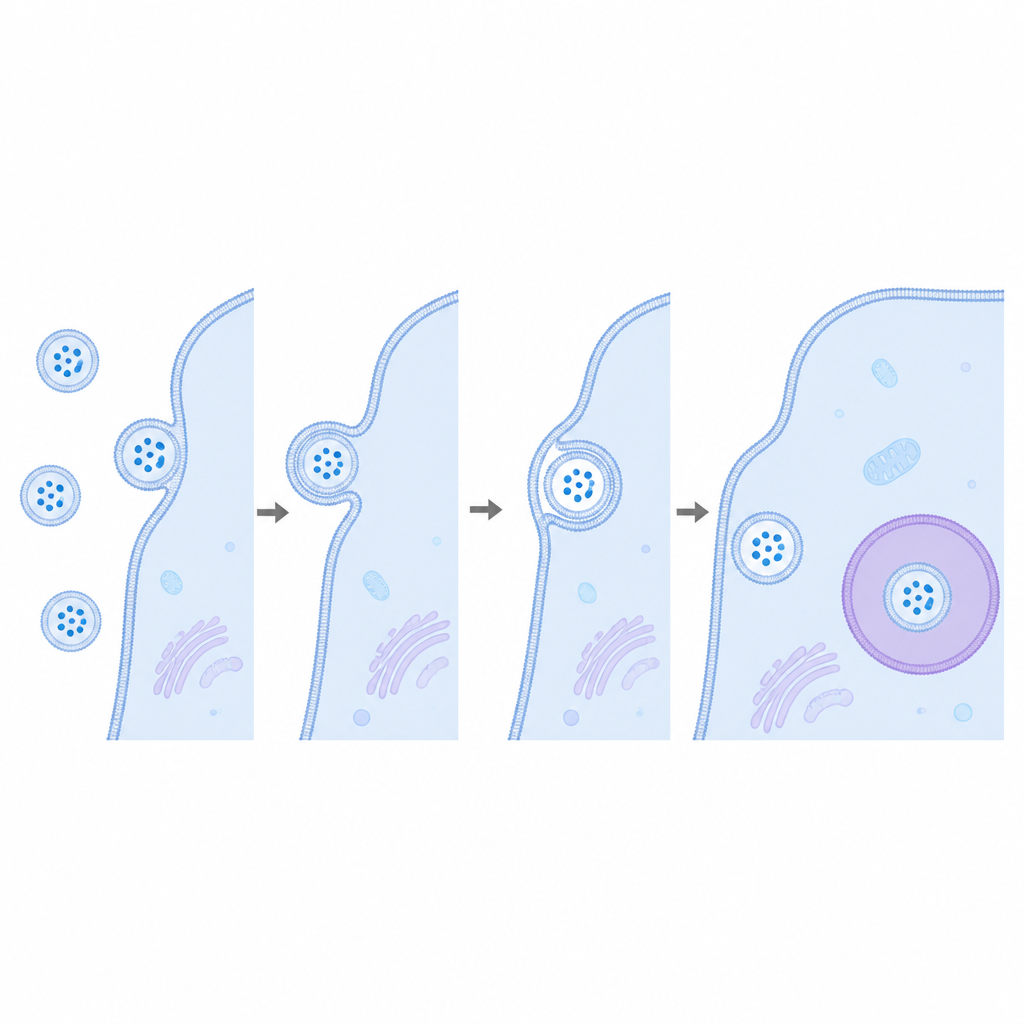
Riconsiderare come queste bolle comunicano tra le cellule
Nel complesso, il lavoro suggerisce che in condizioni di laboratorio standard le vescicole positive per CD63 provenienti da cellule renali umane raramente, se mai, si fondono con le membrane delle cellule riceventi per riversare il loro contenuto interno nell'interno della cellula. Possono comunque legarsi, essere inglobate in compartimenti interni o segnalare tramite interazioni superficiali, ma la consegna diretta del loro carico interno sembra inefficiente senza aiutanti di fusione aggiunti come proteine virali. Per il lettore generale, il messaggio è che questi pacchetti naturali prodotti dalle cellule potrebbero non essere i vettori di messaggi così diretti che molti avevano immaginato, e che gli scienziati dovranno ripensare sia come le cellule comunicano tramite di essi sia come sfruttarli al meglio per future terapie.
Citazione: Askarian-Amiri, S., Weissenhorn, W., Sadoul, R. et al. Lack of evidence for cargo release of CD63-EVs into recipient cells. Sci Rep 16, 15164 (2026). https://doi.org/10.1038/s41598-026-45021-2
Parole chiave: vescicole extracellulari, esosomi, comunicazione cellulare, fusione di membrane, saggio con nanoluciferasi