Clear Sky Science · pt
Alta magnitude de Acinetobacter baumannii produtores de carbapenemase em pacientes com sepse em hospitais de referência etíopes: uma análise de genoma completo
Por que isso importa para pacientes e familiares
Sepse é uma condição com risco de vida em que a resposta do corpo à infecção sai do controle. Tratá-la já é difícil, mas torna‑se ainda mais perigosa quando a infecção é causada por bactérias que resistem à maioria dos antibióticos disponíveis. Este estudo investigou um desses supermicróbios, Acinetobacter baumannii, em grandes hospitais etíopes e usou sequenciamento do genoma completo para revelar quão difundidas e profundamente resistentes essas bactérias se tornaram — e o que isso significa para pacientes vulneráveis, especialmente recém‑nascidos.
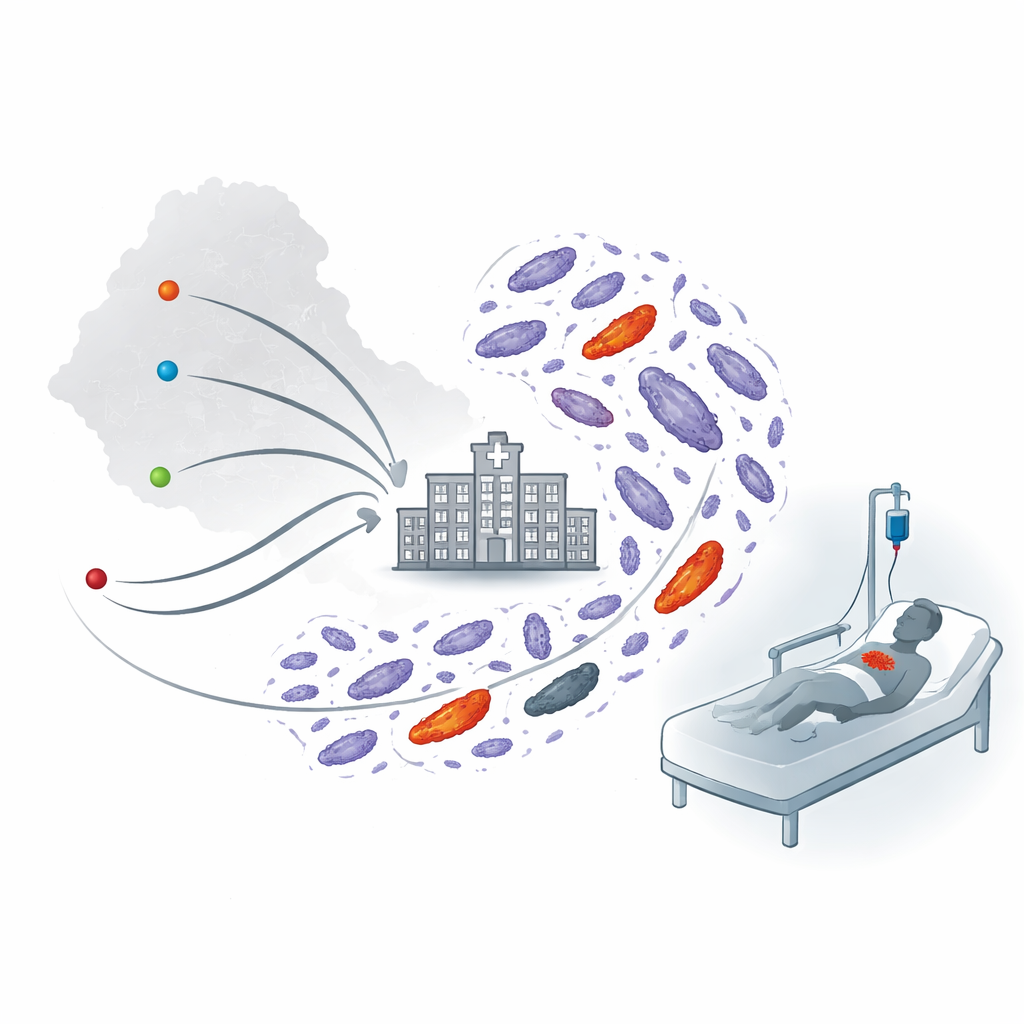
Ameaça hospitalar oculta na corrente sanguínea
Os pesquisadores acompanharam 1.416 pacientes diagnosticados com sepse entre o final de 2019 e 2020 em quatro grandes hospitais de referência no centro, norte e sul da Etiópia. Amostras de sangue foram coletadas para identificar quais bactérias causavam as infecções. Foram isolados 45 Acinetobacter, e a maioria — 38 no total — era Acinetobacter baumannii, espécie já conhecida mundialmente por provocar infecções hospitalares de difícil tratamento. Todas essas amostras vieram de pessoas já internadas, muitas por uma semana ou mais, e uma grande parcela foi encaminhada de outras unidades de saúde, apontando fortemente para infecções que surgem e se espalham dentro dos hospitais em vez de na comunidade.
Recém‑nascidos e crianças na linha de frente
O estudo mostrou que os pacientes mais jovens foram os mais afetados. Quase metade dos isolados de Acinetobacter veio de recém‑nascidos em unidades de terapia intensiva neonatal, e muitos outros de enfermarias pediátricas. Essas unidades cuidam de bebês e crianças frágeis cujos sistemas imunológicos não estão totalmente desenvolvidos, tornando‑os particularmente vulneráveis. Quando uma bactéria altamente resistente se estabelece nesses ambientes, ela pode se mover entre leitos e até entre hospitais à medida que pacientes são transferidos para cuidados mais avançados. O padrão de casos nas regiões central, sul e norte da Etiópia sugere que essas linhagens não são curiosidades isoladas, mas parte de um problema hospitalar mais amplo.
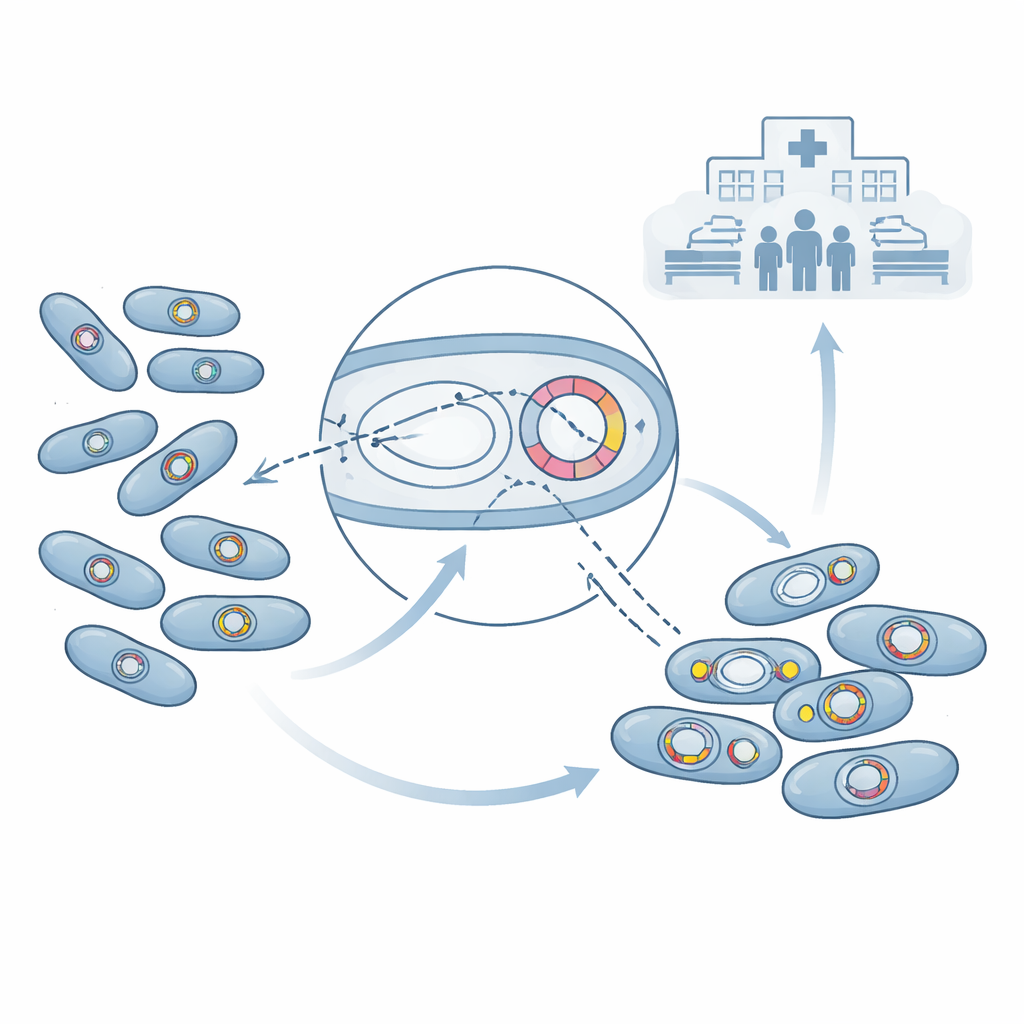
Genética do supermicróbio e resistência
Para entender por que essas bactérias eram tão difíceis de tratar, os cientistas leram seu código genético usando sequenciamento do genoma completo. Eles descobriram que quase metade das amostras de Acinetobacter baumannii carregava um poderoso gene de resistência chamado blaNDM-1, e muitas também apresentavam outro conjunto de genes conhecidos como carbapenemases do tipo OXA. Esses genes codificam enzimas que destroem carbapenêmicos — medicamentos frequentemente considerados recurso final quando outros antibióticos falham. Em algumas bactérias, blaNDM-1 e certos genes OXA foram encontrados juntos em círculos de DNA móveis chamados plasmídeos, que podem se mover entre bactérias como pequenos pen drives genéticos. Outros genes de resistência estavam integrados ao cromossomo bacteriano. Além da resistência a carbapenêmicos, a maioria das linhagens carregava genes adicionais que bloqueiam muitas outras famílias de antibióticos, assim como alguns desinfetantes, deixando os médicos com pouquíssimas opções de tratamento.
Clones em movimento entre enfermarias e hospitais
Ao comparar genomas, a equipe pôde ver quais linhagens bacterianas eram estreitamente relacionadas. Eles encontraram vários aglomerados, ou clones, que apareceram repetidamente dentro e entre hospitais, indicando disseminação contínua em vez de introduções isoladas. Dois importantes tipos de linhagens internacionais, conhecidos mundialmente por causar surtos, também eram comuns nos hospitais etíopes. Em um hospital do norte, um único clone dominou a unidade neonatal, sugerindo um surto local. Em outros locais, uma mistura de clones circulava pelas enfermarias neonatais e pediátricas. Essa impressão digital genética mostra que Acinetobacter resistente não está apenas presente, mas se move ativamente pelo sistema de saúde, frequentemente carreador de plasmídeos que transportam múltiplas características de resistência ao mesmo tempo.
O que isso significa para cuidado e controle
O quadro que emerge é preocupante: os hospitais de referência etíopes enfrentam uma alta carga de linhagens de Acinetobacter baumannii que resistem a muitos, e às vezes quase todos, os antibióticos padrão. A situação é particularmente alarmante em unidades neonatais, onde estão concentrados os pacientes mais doentes e pequenos. Num ponto positivo, um novo fármaco chamado cefiderocol ainda foi eficaz contra todas as cepas mais resistentes testadas neste estudo, embora as doses necessárias possam ser maiores. De forma geral, os achados apontam para a necessidade urgente de medidas mais fortes de prevenção de infecções, uso criterioso de antibióticos e programas nacionais de manejo antibiótico. Para pacientes e familiares, esta pesquisa reforça por que prevenir infecções em hospitais — e proteger a eficácia dos antibióticos existentes — é tão importante quanto desenvolver novos medicamentos.
Citação: Legese, M.H., Asrat, D., Mihret, A. et al. High magnitude of carbapenemase-producing Acinetobacter baumannii in sepsis patients at Ethiopian referral hospitals: a whole genome analysis. Sci Rep 16, 14009 (2026). https://doi.org/10.1038/s41598-026-44498-1
Palavras-chave: sepse, bactérias resistentes a medicamentos, infecções hospitalares, Acinetobacter baumannii, Etiópia