Clear Sky Science · fr
Forte prévalence d’Acinetobacter baumannii producteur de carbapénémase chez des patients septiques dans des hôpitaux de référence éthiopiens : une analyse du génome entier
Pourquoi c’est important pour les patients et les familles
La sepsie est une affection potentiellement mortelle où la réponse de l’organisme à une infection devient incontrôlable. La traiter est déjà difficile, mais cela devient encore plus dangereux lorsque l’infection est due à des bactéries qui résistent à presque tous les antibiotiques disponibles. Cette étude s’est intéressée à l’un de ces super‑agents, Acinetobacter baumannii, dans des hôpitaux majeurs d’Éthiopie et a utilisé le séquençage du génome entier pour montrer à quel point ces germes sont répandus et profondément résistants—et ce que cela signifie pour les patients vulnérables, en particulier les nouveau‑nés.
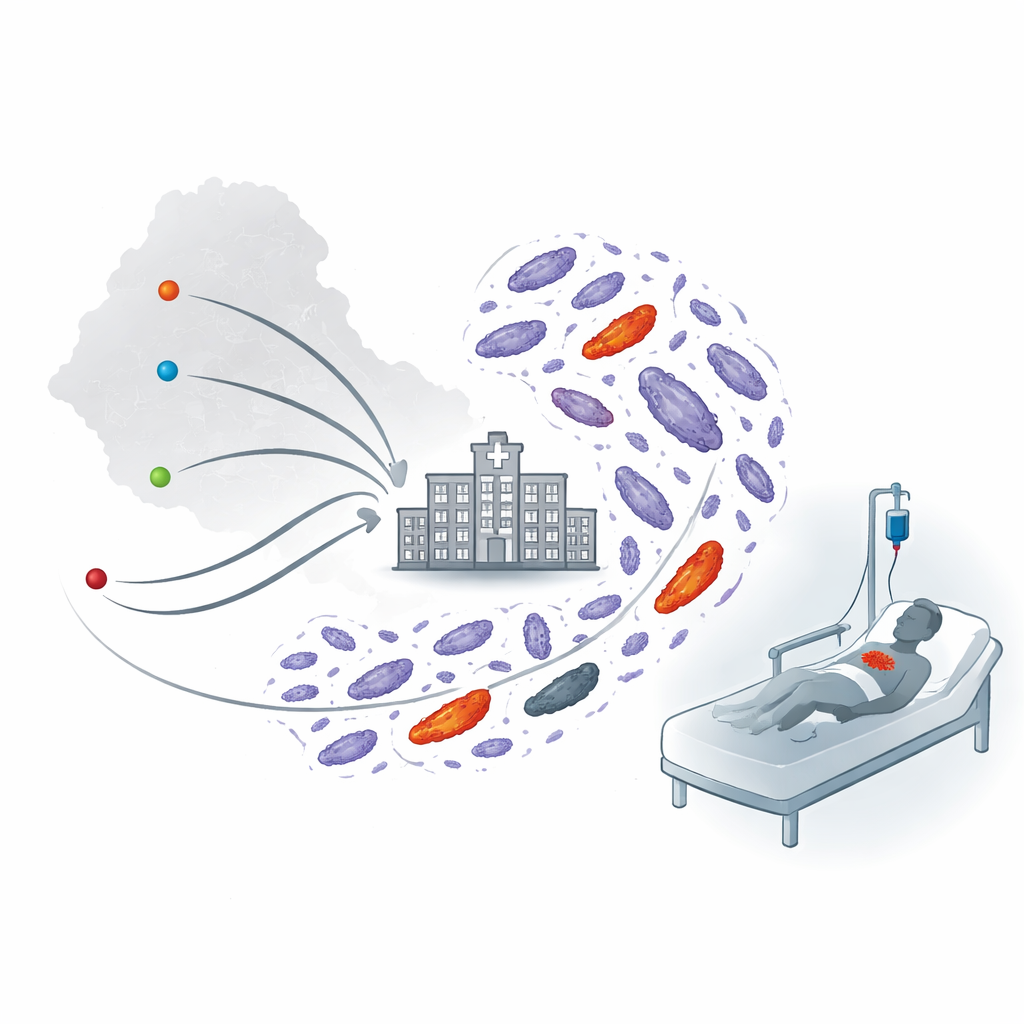
Une menace cachée dans le sang en milieu hospitalier
Les chercheurs ont suivi 1 416 patients diagnostiqués avec une sepsie entre la fin 2019 et 2020 dans quatre grands hôpitaux de référence du centre, du nord et du sud de l’Éthiopie. Des prélèvements sanguins ont été effectués pour identifier les bactéries responsables des infections. Quarante‑cinq isolats d’Acinetobacter ont été trouvés, dont la majorité—38 au total—étaient Acinetobacter baumannii, une espèce déjà connue dans le monde entier pour provoquer des infections nosocomiales difficiles à traiter. Tous ces prélèvements proviennent de patients déjà hospitalisés, souvent depuis une semaine ou plus, et une grande partie étaient adressés depuis d’autres établissements de santé, ce qui indique fortement des infections qui apparaissent et se propagent à l’hôpital plutôt que dans la communauté.
Les nouveau‑nés et les enfants en première ligne
L’étude montre que les patients les plus jeunes ont été les plus touchés. Près de la moitié des isolats d’Acinetobacter provenaient de nouveau‑nés en unités de soins intensifs néonatals, et beaucoup d’autres provenaient de services pédiatriques. Ces unités prennent en charge des nourrissons et des enfants fragiles dont le système immunitaire n’est pas pleinement développé, les rendant particulièrement vulnérables. Lorsqu’une bactérie hautement résistante s’établit dans de tels environnements, elle peut se déplacer d’un lit à l’autre et même d’un hôpital à l’autre lorsque des patients sont transférés pour des soins spécialisés. La répartition des cas dans les régions centrale, sud et nord de l’Éthiopie suggère que ces souches ne sont pas des curiosités isolées mais font partie d’un problème hospitalier plus large.
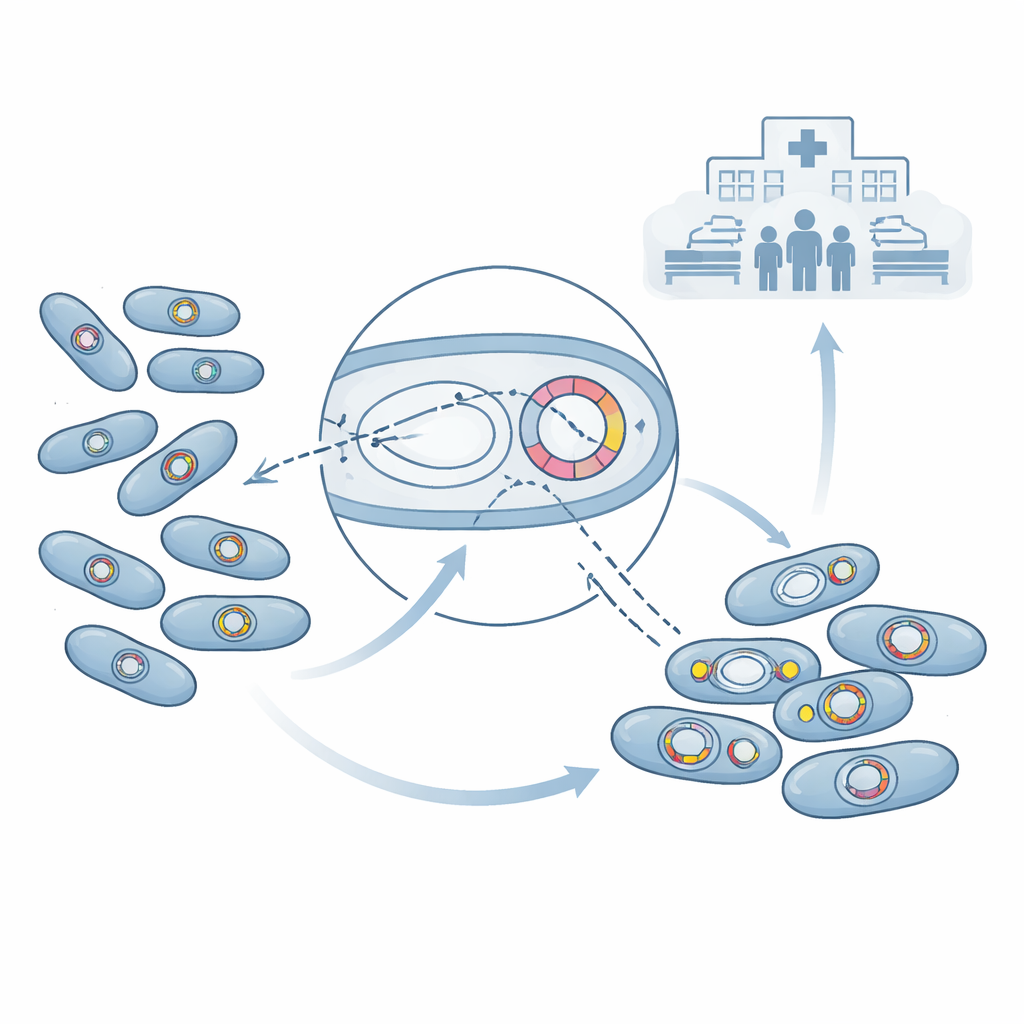
Génétique du super‑agent et mécanismes de résistance
Pour comprendre pourquoi ces bactéries étaient si difficiles à traiter, les scientifiques ont lu leur code génétique à l’aide du séquençage du génome entier. Ils ont constaté qu’un peu près la moitié des échantillons d’Acinetobacter baumannii portaient un gène de résistance puissant appelé blaNDM‑1, et que beaucoup portaient également un groupe de gènes connus sous le nom de carbapénémases de type OXA. Ces gènes codent des enzymes qui détruisent les carbapénèmes—des médicaments souvent considérés comme un dernier recours lorsque d’autres antibiotiques échouent. Chez certaines bactéries, blaNDM‑1 et certains gènes OXA ont été trouvés ensemble sur des cercles d’ADN mobiles appelés plasmides, qui peuvent se déplacer entre bactéries comme de petits clés USB génétiques. D’autres gènes de résistance étaient intégrés dans le chromosome bactérien. Au‑delà des carbapénèmes, la plupart des souches portaient des gènes supplémentaires neutralisant de nombreuses autres familles d’antibiotiques, ainsi que certains désinfectants, laissant aux médecins très peu d’options thérapeutiques.
Des clones en mouvement entre services et hôpitaux
En comparant les génomes, l’équipe a pu identifier quelles souches bactérielles étaient étroitement apparentées. Ils ont trouvé plusieurs grappes, ou clones, apparus à plusieurs reprises au sein et entre les hôpitaux, indiquant une propagation continue plutôt que des introductions ponctuelles. Deux types de souches internationaux majeurs, connus pour provoquer des flambées, étaient également courants dans les hôpitaux éthiopiens. Dans un hôpital du nord, un seul clone dominait l’unité de soins intensifs néonatals, suggérant une épidémie locale. Dans d’autres sites, un mélange de clones circulait dans les unités néonatales et pédiatriques. Ce fingerprinting génétique montre qu’Acinetobacter résistant n’est pas seulement présent, mais se déplace activement dans le système de santé, souvent transporté par des plasmides qui regroupent plusieurs caractères de résistance.
Ce que cela implique pour les soins et la prévention
Le tableau qui se dégage est alarmant : les hôpitaux de référence éthiopiens font face à un lourd fardeau de souches d’Acinetobacter baumannii résistantes à de nombreux—et parfois presque tous—les antibiotiques standard. La situation est particulièrement préoccupante dans les unités néonatales, où se concentrent les patients les plus petits et les plus malades. Côté positif, un nouvel antibiotique, la cefidérol, est resté actif contre toutes les souches les plus résistantes testées dans cette étude, bien que les doses nécessaires puissent être plus élevées. Globalement, les résultats soulignent la nécessité urgente de renforcer les mesures de prévention des infections, d’utiliser les antibiotiques avec prudence et de mettre en place des programmes nationaux de stewardship. Pour les patients et les familles, cette recherche rappelle pourquoi prévenir les infections à l’hôpital—et préserver l’efficacité des antibiotiques existants—est tout aussi important que le développement de nouveaux médicaments.
Citation: Legese, M.H., Asrat, D., Mihret, A. et al. High magnitude of carbapenemase-producing Acinetobacter baumannii in sepsis patients at Ethiopian referral hospitals: a whole genome analysis. Sci Rep 16, 14009 (2026). https://doi.org/10.1038/s41598-026-44498-1
Mots-clés: sepsie, bactéries résistantes aux médicaments, infections nosocomiales, Acinetobacter baumannii, Éthiopie