Clear Sky Science · es
Alta prevalencia de Acinetobacter baumannii productor de carbapenemasas en pacientes con sepsis en hospitales de referencia etíopes: un análisis del genoma completo
Por qué esto importa para pacientes y familias
La sepsis es una condición potencialmente mortal en la que la respuesta del organismo a una infección se descontrola. Tratarla ya es difícil, pero se vuelve aún más peligrosa cuando la infección la causan bacterias que resisten casi todos los antibióticos disponibles. Este estudio analizó a uno de esos superbacterias, Acinetobacter baumannii, en hospitales importantes de Etiopía y utilizó el análisis del genoma completo para revelar cuán extendidos y profundamente resistentes se han vuelto estos gérmenes—y qué significa eso para los pacientes vulnerables, especialmente los recién nacidos.
Amenaza hospitalaria oculta en el torrente sanguíneo
Los investigadores siguieron a 1.416 pacientes diagnosticados con sepsis entre finales de 2019 y 2020 en cuatro grandes hospitales de referencia del centro, norte y sur de Etiopía. Se tomaron muestras de sangre para identificar las bacterias causantes de las infecciones. Se encontraron 45 aislamientos de Acinetobacter y la mayoría—38 en total—eran Acinetobacter baumannii, una especie ya reconocida mundialmente por provocar infecciones nosocomiales difíciles de tratar. Todas estas muestras procedían de personas que ya estaban hospitalizadas, muchas por una semana o más, y una gran proporción habían sido referidas desde otros centros sanitarios, lo que apunta con fuerza a infecciones que surgen y se propagan dentro de los hospitales más que en la comunidad.
Recién nacidos y niños en la primera línea
El estudio mostró que los pacientes más jóvenes fueron los más afectados. Casi la mitad de los aislamientos de Acinetobacter procedían de recién nacidos en unidades de cuidados intensivos neonatales, y muchos otros de salas pediátricas. Estas unidades atienden a bebés y niños frágiles cuyos sistemas inmunitarios no están completamente desarrollados, lo que los hace particularmente vulnerables. Cuando una bacteria altamente resistente se establece en estos entornos, puede desplazarse entre camas e incluso entre hospitales a medida que los pacientes son transferidos para recibir atención avanzada. El patrón de casos en las regiones central, sur y norte de Etiopía sugiere que estas cepas no son curiosidades aisladas, sino parte de un problema hospitalario más amplio.
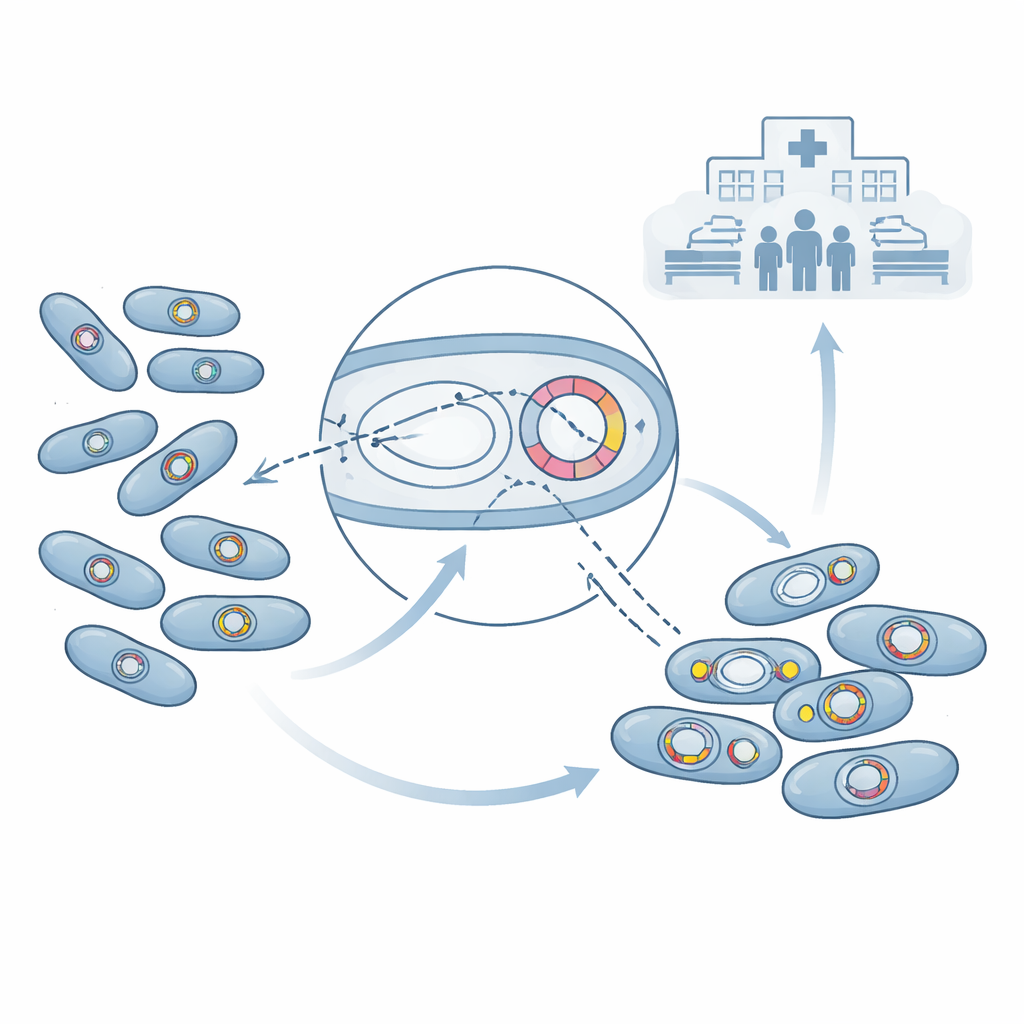
Genética del superbacteria y resistencia
Para entender por qué estas bacterias eran tan difíciles de tratar, los científicos leyeron su código genético mediante secuenciación del genoma completo. Encontraron que casi la mitad de las muestras de Acinetobacter baumannii portaban un poderoso gen de resistencia llamado blaNDM-1, y muchas también llevaban otro grupo de genes conocidos como carbapenemasas tipo OXA. Estos genes producen enzimas que destruyen los carbapenemes—fármacos considerados a menudo como último recurso cuando otros antibióticos fallan. En algunas bacterias, blaNDM-1 y ciertos genes OXA se encontraron juntos en círculos de ADN móviles llamados plásmidos, que pueden transferirse entre bacterias como pequeñas unidades genéticas extraíbles. Otros genes de resistencia estaban integrados en el cromosoma bacteriano. Más allá de los carbapenemes, la mayoría de las cepas portaban genes adicionales que anulan muchas otras familias de antibióticos, así como algunos desinfectantes, dejando a los médicos con muy pocas opciones terapéuticas.
Clones en movimiento entre salas y hospitales
Al comparar genomas, el equipo pudo identificar qué cepas bacterianas estaban estrechamente relacionadas. Encontraron varios grupos, o clones, que aparecían de forma repetida dentro y entre hospitales, lo que indica una propagación continua más que introducciones aisladas. Dos tipos de cepas internacionales importantes, conocidas mundialmente por causar brotes, eran comunes también en los hospitales etíopes. En un hospital del norte, un solo clon dominaba la unidad de cuidados intensivos neonatales, lo que sugiere un brote local. En otros centros, una mezcla de clones circulaba por las salas neonatales y pediátricas. Este perfil genético muestra que el Acinetobacter resistente no solo está presente, sino que se está moviendo activamente a través del sistema sanitario, con frecuencia transportado en plásmidos que llevan múltiples rasgos de resistencia a la vez.
Qué significa esto para la atención y el control
El panorama que emerge es preocupante: los hospitales de referencia etíopes enfrentan una alta carga de cepas de Acinetobacter baumannii que resisten muchos, y a veces casi todos, los antibióticos estándar. La situación es especialmente alarmante en las unidades neonatales, donde se concentran los pacientes más enfermos y pequeños. En el lado positivo, un fármaco nuevo llamado cefiderocol siguió siendo eficaz contra todas las cepas más resistentes probadas en este estudio, aunque las dosis necesarias pueden ser mayores. En conjunto, los hallazgos señalan la necesidad urgente de reforzar las medidas de prevención de infecciones, un uso más prudente de los antibióticos y programas nacionales de gestión de antimicrobianos. Para pacientes y familias, esta investigación subraya por qué prevenir infecciones en hospitales—y proteger la eficacia de los antibióticos existentes—es tan importante como desarrollar nuevos fármacos.
Cita: Legese, M.H., Asrat, D., Mihret, A. et al. High magnitude of carbapenemase-producing Acinetobacter baumannii in sepsis patients at Ethiopian referral hospitals: a whole genome analysis. Sci Rep 16, 14009 (2026). https://doi.org/10.1038/s41598-026-44498-1
Palabras clave: sepsis, bacterias multirresistentes, infecciones hospitalarias, Acinetobacter baumannii, Etiopía