Clear Sky Science · de
Hohe Häufigkeit von Carbapenemase-bildendem Acinetobacter baumannii bei Sepsispatienten in äthiopischen Überweisungskrankenhäusern: eine Ganzgenomanalyse
Warum das für Patienten und Familien wichtig ist
Sepsis ist ein lebensbedrohlicher Zustand, bei dem die körpereigene Reaktion auf eine Infektion außer Kontrolle gerät. Die Behandlung ist ohnehin schwierig, doch sie wird noch riskanter, wenn die Infektion von Bakterien verursacht wird, die nahezu allen verfügbaren Antibiotika trotzen. Diese Studie untersuchte einen solchen Erreger, Acinetobacter baumannii, in großen äthiopischen Krankenhäusern und nutzte Ganzgenomsequenzierung, um zu zeigen, wie weit verbreitet und tiefgreifend resistent diese Keime geworden sind – und was das für besonders gefährdete Patienten, vor allem Neugeborene, bedeutet.
Verborgene Krankenhausbedrohung im Blutkreislauf
Die Forschenden begleiteten 1.416 Patienten mit Sepsisdiagnose zwischen Ende 2019 und 2020 in vier großen Überweisungskrankenhäusern in Zentral-, Nord- und Südäthiopien. Es wurden Blutproben entnommen, um die verursachenden Bakterien zu identifizieren. Insgesamt wurden 45 Acinetobacter-Isolate gefunden; die Mehrheit davon – 38 Isolate – gehörte zur Art Acinetobacter baumannii, die weltweit für schwer behandelbare Krankenhausinfektionen bekannt ist. Alle Proben stammten von bereits stationär aufgenommenen Patienten, viele von ihnen lagen eine Woche oder länger im Krankenhaus, und ein großer Anteil war aus anderen Gesundheitseinrichtungen überwiesen worden. Das deutet stark darauf hin, dass die Infektionen in den Krankenhäusern entstanden und sich dort ausbreiten, statt in der Gemeinschaft erworben worden zu sein.
Neugeborene und Kinder in vorderster Reihe
Die Studie zeigte, dass die jüngsten Patienten am stärksten betroffen waren. Fast die Hälfte der Acinetobacter-Isolate stammte aus neonatalen Intensivstationen, viele weitere aus Kinderstationen. Diese Bereiche betreuen fragile Säuglinge und Kinder mit noch nicht voll entwickeltem Immunsystem, die besonders anfällig sind. Etabliert sich ein hochresistenter Erreger in solchen Einheiten, kann er zwischen Betten und sogar zwischen Krankenhäusern bei Verlegungen wandern. Das Verteilungsmuster der Fälle in Zentral-, Süd- und Nordäthiopien legt nahe, dass diese Stämme keine Einzelfälle sind, sondern Teil eines breiteren, krankenhausbasierten Problems.
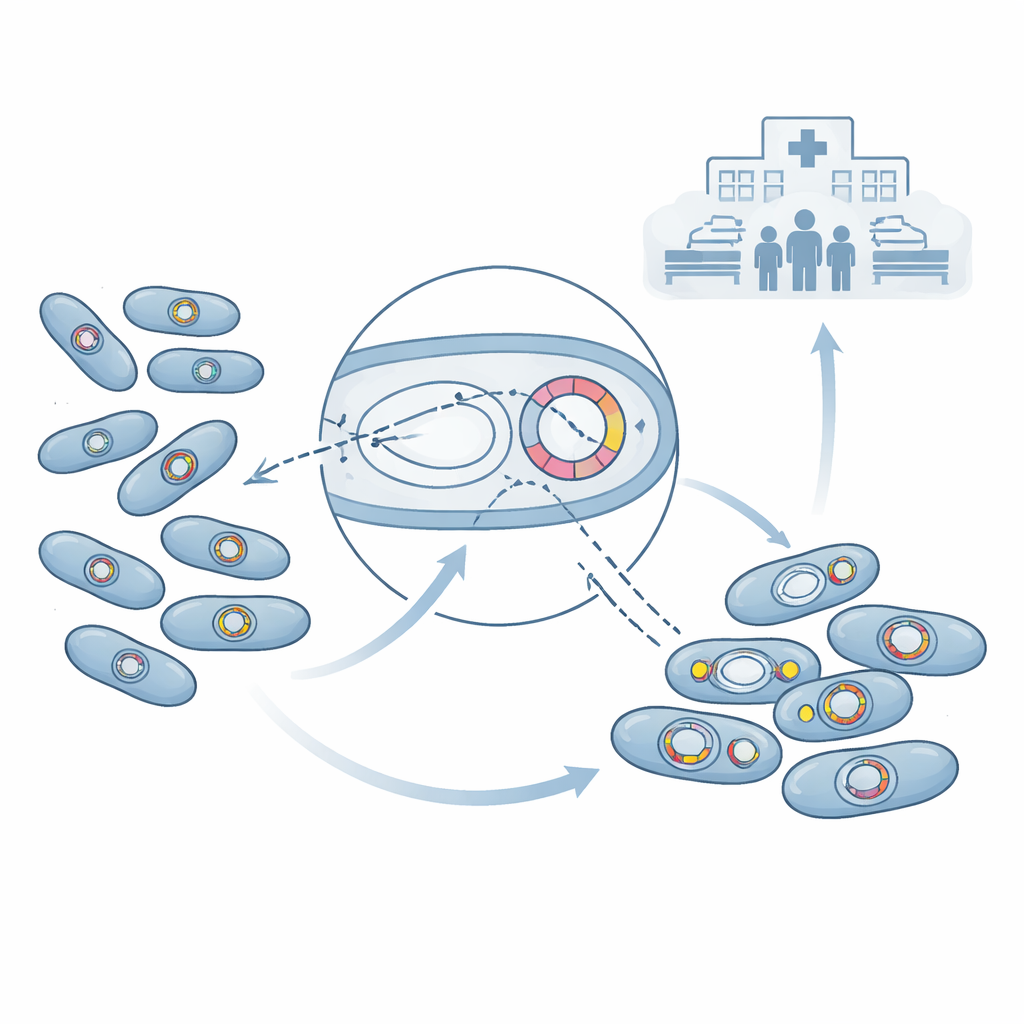
Genetik der Superkeime und Resistenzmechanismen
Um zu verstehen, warum diese Bakterien so schwer zu behandeln sind, lasen die Wissenschaftler ihren genetischen Code mittels Ganzgenomsequenzierung. Sie fanden, dass fast die Hälfte der Acinetobacter baumannii-Isolate ein starkes Resistenzgen namens blaNDM-1 trug, und viele zusätzlich Gene aus der Gruppe der OXA-Typ Carbapenemasen. Diese Gene kodieren Enzyme, die Carbapeneme zerstören – Wirkstoffe, die oft als letztes Mittel eingesetzt werden, wenn andere Antibiotika versagen. In einigen Bakterien kamen blaNDM-1 und bestimmte OXA-Gene gemeinsam auf mobilen DNA-Kreisen vor, sogenannten Plasmiden, die sich wie kleine genetische USB-Sticks zwischen Bakterien bewegen können. Andere Resistenzgene waren im bakteriellen Chromosom verankert. Neben der Carbapenemresistenz trugen die meisten Stämme weitere Gene, die viele andere Antibiotikaklassen sowie einige Desinfektionsmittel unwirksam machen, wodurch Ärztinnen und Ärzten nur noch sehr wenige Behandlungsoptionen bleiben.
Klone unterwegs zwischen Stationen und Krankenhäusern
Durch Genomvergleiche konnte das Team erkennen, welche Stämme eng verwandt waren. Sie identifizierten mehrere Cluster oder Klone, die innerhalb und zwischen Krankenhäusern wiederholt auftraten, was für eine andauernde Ausbreitung statt einmaliger Einschleppungen spricht. Zwei große internationale Stammtypen, die weltweit für Ausbrüche bekannt sind, waren auch in den äthiopischen Krankenhäusern häufig. In einem nördlichen Krankenhaus dominierte ein einzelner Klon die neonatale Intensivstation, ein Hinweis auf einen lokalen Ausbruch. An anderen Standorten zirkulierte ein Gemisch aus Klonen durch Neonatal- und Pediatriestation. Diese genetische Fingerabdruckanalyse zeigt, dass resistenter Acinetobacter nicht nur vorhanden ist, sondern aktiv im Gesundheitssystem unterwegs ist, oft unterstützt von Plasmiden, die mehrere Resistenzmerkmale gleichzeitig transportieren.
Was das für Pflege und Kontrolle bedeutet
Das Bild ist ernüchternd: Äthiopische Überweisungskrankenhäuser sehen sich einer hohen Belastung durch Acinetobacter baumannii-Stämme gegenüber, die gegen viele und teils fast alle Standardantibiotika resistent sind. Besonders besorgniserregend ist die Lage in Neonatalstationen, wo die kleinsten und schwer kranken Patienten konzentriert sind. Positiv ist, dass ein neues Antibiotikum namens Cefiderocol gegen alle in dieser Studie getesteten, am stärksten resistenten Stämme wirksam blieb, wenngleich möglicherweise höhere Dosen erforderlich sind. Insgesamt weisen die Ergebnisse auf einen dringenden Bedarf an stärkeren Maßnahmen zur Infektionsprävention, einem verantwortungsvollen Antibiotikaeinsatz und landesweiten Stewardship-Programmen hin. Für Patienten und Familien unterstreicht diese Forschung, warum die Verhinderung von Krankenhausinfektionen – und der Erhalt der Wirksamkeit vorhandener Antibiotika – genauso wichtig ist wie die Entwicklung neuer Medikamente.
Zitation: Legese, M.H., Asrat, D., Mihret, A. et al. High magnitude of carbapenemase-producing Acinetobacter baumannii in sepsis patients at Ethiopian referral hospitals: a whole genome analysis. Sci Rep 16, 14009 (2026). https://doi.org/10.1038/s41598-026-44498-1
Schlüsselwörter: Sepsis, multiresistente Bakterien, nosokomiale Infektionen, Acinetobacter baumannii, Äthiopien