Clear Sky Science · pl
Wysokie występowanie Acinetobacter baumannii produkującego karbapenemazy u pacjentów z sepsą w szpitalach referencyjnych w Etiopii: analiza całego genomu
Dlaczego to ma znaczenie dla pacjentów i rodzin
Sepsa to zagrażający życiu stan, w którym reakcja organizmu na infekcję wymyka się spod kontroli. Jej leczenie jest trudne, a staje się jeszcze bardziej niebezpieczne, gdy wywołuje ją bakteria odporna na niemal wszystkie dostępne antybiotyki. W tym badaniu przeanalizowano taki właśnie supermikrob — Acinetobacter baumannii — w głównych szpitalach etiopskich i zastosowano sekwencjonowanie całego genomu, aby pokazać, jak rozpowszechnione i głęboko oporne stały się te drobnoustroje — oraz co to oznacza dla najbardziej podatnych pacjentów, zwłaszcza noworodków.
Ukryte zagrożenie w krwiobiegu szpitalnym
Naukowcy obserwowali 1 416 pacjentów z rozpoznaną sepsą od końca 2019 do 2020 roku w czterech dużych szpitalach referencyjnych w centralnej, północnej i południowej Etiopii. Pobierano próbki krwi, by ustalić, które bakterie wywołują zakażenia. Znaleziono 45 izolatów Acinetobacter, z czego większość — 38 — stanowił Acinetobacter baumannii, gatunek powszechnie znany z powodowania trudnych do leczenia zakażeń szpitalnych. Wszystkie próbki pochodziły od osób już hospitalizowanych, wiele z nich przez tydzień lub dłużej, a znaczna część była przekierowana z innych placówek zdrowia, co wyraźnie wskazuje na zakażenia powstające i szerzące się w szpitalach, a nie w społecznościach.
Noworodki i dzieci na pierwszej linii
Badanie wykazało, że najsilniej dotknięte były najmłodsze pacjentki i pacjenci. Prawie połowa izolowanych szczepów Acinetobacter pochodziła od noworodków przebywających na oddziałach intensywnej opieki neonatologicznej, a wiele kolejnych z oddziałów pediatrycznych. Oddziały te opiekują się kruchymi niemowlętami i dziećmi o niedojrzałych układach odpornościowych, co czyni je szczególnie wrażliwymi. Gdy wysoce oporna bakteria zadomowi się w takich warunkach, może przemieszczać się między łóżkami, a nawet między szpitalami przy przenoszeniu pacjentów na bardziej zaawansowaną opiekę. Wzorzec przypadków w regionach centralnym, południowym i północnym Etiopii sugeruje, że te szczepy nie są odizolowanymi przypadkami, lecz częścią szerszego problemu szpitalnego.
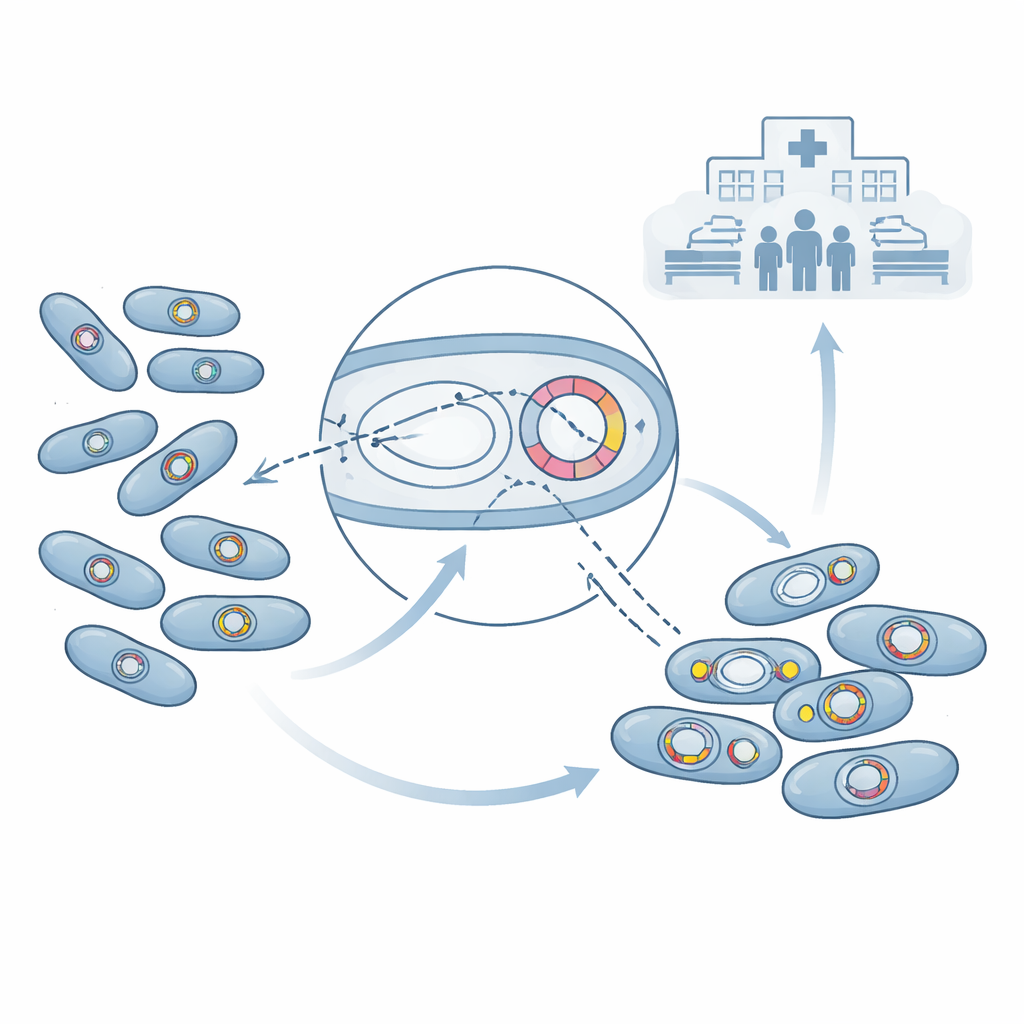
Genetyka supermikrobów i oporność
Aby zrozumieć, dlaczego te bakterie były tak trudne do leczenia, badacze odczytali ich kod genetyczny za pomocą sekwencjonowania całego genomu. Stwierdzili, że prawie połowa próbek Acinetobacter baumannii nosiła silne geny oporności o nazwie blaNDM-1, a wiele z nich miało też inne geny z grupy karbapenemaz typu OXA. Te geny kodują enzymy, które niszczą karbapenemy — leki często uważane za ostateczność, gdy inne antybiotyki zawodzą. W niektórych bakteriach blaNDM-1 i niektóre geny OXA znajdowały się razem na ruchomych okrągłych cząsteczkach DNA zwanych plazmidami, które mogą przemieszczać się między bakteriami niczym małe genetyczne pamięci USB. Inne geny oporności były wbudowane w chromosom bakterii. Poza karbapenemami większość szczepów miała dodatkowe geny blokujące wiele innych rodzin antybiotyków, a także niektóre środki dezynfekujące, co pozostawia lekarzom bardzo ograniczone opcje leczenia.
Klonowanie i przemieszczanie się między oddziałami i szpitalami
Porównując genomy, zespół mógł ustalić, które szczepy bakterii są ze sobą blisko spokrewnione. Znaleziono kilka klastrów, czyli klonów, które pojawiały się wielokrotnie w obrębie i pomiędzy szpitalami, co wskazuje na trwające rozprzestrzenianie się, a nie jednorazowe wprowadzenia. Dwa główne międzynarodowe typy szczepów, znane na całym świecie z wywoływania epidemii, były również powszechne w etiopskich szpitalach. W jednym szpitalu na północy jeden klon zdominował oddział intensywnej terapii neonatologicznej, dając przesłanki do lokalnego ogniska. W innych placówkach krążyła mieszanka klonów między oddziałami neonatologicznymi i pediatrycznymi. To genetyczne „odciskanie palca” pokazuje, że oporny Acinetobacter nie tylko istnieje, lecz aktywnie przemieszcza się w systemie opieki zdrowotnej, często podróżując na plazmidach niosących wiele cech oporności jednocześnie.
Co to oznacza dla opieki i kontroli
Obraz, który się wyłania, jest przygnębiający: szpitale referencyjne w Etiopii mierzą się z dużym obciążeniem szczepami Acinetobacter baumannii, odpornymi na wiele, a czasem niemal wszystkie standardowe antybiotyki. Sytuacja jest szczególnie niepokojąca na oddziałach neonatologicznych, gdzie koncentrują się najbardziej chore i najmniejsze pacjentki i pacjenci. Z drugiej strony, nowy lek o nazwie cefiderocol nadal działał przeciwko wszystkim najsilniej opornym szczepom przebadanym w tym badaniu, chociaż może wymagać stosowania wyższych dawek. Ogólnie wyniki wskazują na pilną potrzebę wzmocnienia środków zapobiegania zakażeniom, ostrożnego stosowania antybiotyków oraz ogólnokrajowych programów nadzoru i racjonalizacji antybiotykoterapii. Dla pacjentów i rodzin ta praca podkreśla, dlaczego zapobieganie zakażeniom w szpitalach — i ochrona skuteczności istniejących antybiotyków — jest równie ważne jak rozwój nowych leków.
Cytowanie: Legese, M.H., Asrat, D., Mihret, A. et al. High magnitude of carbapenemase-producing Acinetobacter baumannii in sepsis patients at Ethiopian referral hospitals: a whole genome analysis. Sci Rep 16, 14009 (2026). https://doi.org/10.1038/s41598-026-44498-1
Słowa kluczowe: sepsa, oporne na leki bakterie, infekcje szpitalne, Acinetobacter baumannii, Etiopia