Clear Sky Science · pt
Relação causal entre doenças autoimunes e anemia por deficiência de ferro: um estudo de randomização mendeliana de duas amostras
Por que isso importa para a saúde cotidiana
A anemia por deficiência de ferro é uma das causas mais comuns de cansaço e mau estado de saúde em todo o mundo, porém os médicos nem sempre sabem por que uma pessoa em particular fica anêmica. Este estudo faz uma pergunta simples, mas importante: certas doenças autoimunes realmente causam um risco maior de anemia por deficiência de ferro, em vez de apenas ocorrerem nas mesmas pessoas por acaso? Ao usar grandes conjuntos de dados genéticos em vez de ensaios clínicos tradicionais, os autores tentam separar causa e efeito de uma forma que, eventualmente, pode mudar a forma como pacientes de alto risco são monitorados e tratados.
Vínculos ocultos entre imunidade e baixo ferro
Doenças autoimunes surgem quando o sistema de defesa do corpo ataca equivocadamente seus próprios tecidos, levando a inflamação duradoura em órgãos como articulações, intestinos, rins e tecido conjuntivo. Separadamente, a anemia por deficiência de ferro se desenvolve quando o corpo não tem ferro utilizável suficiente para produzir glóbulos vermelhos saudáveis, deixando as pessoas fatigadas, com falta de ar e com menos capacidade de concentração. Estudos observacionais há muito tempo observam que pessoas com condições como artrite reumatoide ou doença inflamatória intestinal frequentemente também apresentam anemia, mas essas fotos momentâneas não conseguem mostrar se a doença autoimune realmente aumenta o risco de deficiência de ferro, ou se outros fatores compartilhados — como dieta, medicamentos ou perda de sangue — são os culpados.
Usando genes como um experimento natural
Os pesquisadores recorreram a um método chamado randomização mendeliana, que trata diferenças genéticas naturais como uma espécie de “atribuição” vitalícia a maior ou menor risco de uma dada doença. Como os genes são definidos na concepção e não são alterados pelo estilo de vida, eles podem ajudar a separar causa de coincidência. A equipe reuniu dados sumários de estudos genéticos muito grandes sobre oito doenças autoimunes — artrite reumatoide, doença inflamatória intestinal, colite ulcerativa, doença de Crohn, doença celíaca, lúpus eritematoso sistêmico, espondilite anquilosante e nefrite membranosa — todos em pessoas de ascendência europeia. Em seguida, compararam esses dados com informações genéticas de mais de 15.000 pessoas com anemia por deficiência de ferro e quase 400.000 sem a condição, do projeto finlandês FinnGen.
O que as evidências genéticas mostram
Usando várias camadas de checagens de qualidade, os autores selecionaram variantes genéticas fortemente associadas a cada doença autoimune, enquanto tentavam evitar variantes que pudessem influenciar a anemia por outras vias. A abordagem estatística principal, apoiada por múltiplos testes de sensibilidade, encontrou que pessoas com predisposição genética para artrite reumatoide, doença inflamatória intestinal e colite ulcerativa apresentaram um pequeno, porém claro, aumento do risco de anemia por deficiência de ferro. Sinais para doença celíaca, espondilite anquilosante, doença de Crohn, lúpus sistêmico e nefrite membranosa foram mais fracos: alguns pareceram ligados à anemia inicialmente, mas a força dessas associações caiu ou desapareceu depois que os pesquisadores removeram variantes de uma região complexa do genoma relacionada ao sistema imunológico que pode distorcer tais análises.
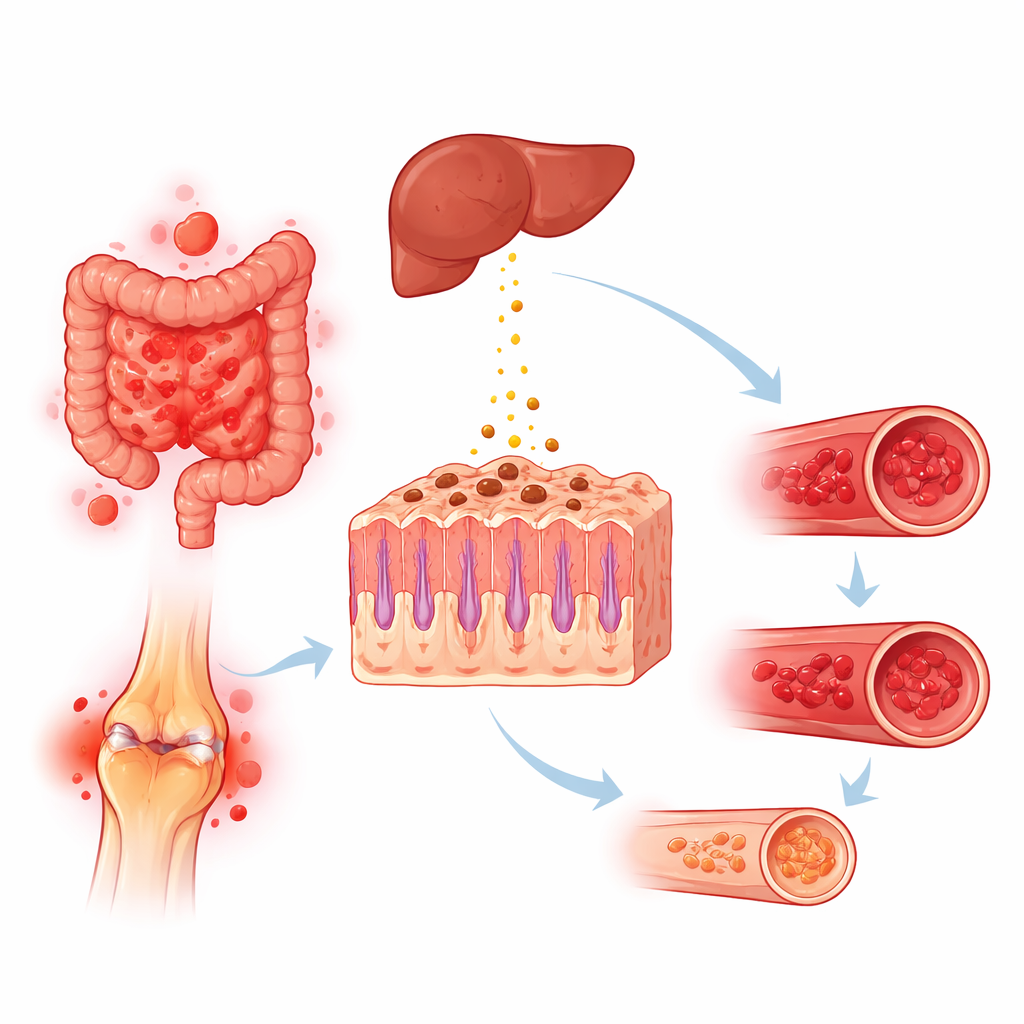
Como a atividade autoimune pode esgotar o ferro
Vários caminhos biológicos podem explicar por que doenças autoimunes, especialmente aquelas envolvendo o intestino e inflamação crônica, levam as pessoas à deficiência de ferro. Distúrbios intestinais podem causar sangramento interno lento, má absorção de nutrientes ou dano ao intestino delgado proximal, onde ocorre a maior parte da captação de ferro. O uso prolongado de analgésicos em doenças articulares também pode aumentar sangramentos no estômago e intestinos. Ao mesmo tempo, sinais inflamatórios comuns na autoimunidade estimulam o fígado a liberar hepcidina, um hormônio que aprisiona o ferro dentro das células de armazenamento e reduz sua passagem do intestino para a corrente sanguínea. O resultado pode ser perda absoluta de ferro, bloqueio funcional do uso do ferro, ou ambos, produzindo anemia mesmo quando as reservas corporais de ferro não estão completamente esgotadas.
O que isso significa para o futuro
Para uma pessoa vivendo com artrite reumatoide ou doença inflamatória intestinal, o estudo sugere que sua condição faz mais do que simplesmente coexistir com a anemia — ela provavelmente contribui para causá‑la, mesmo que o aumento do risco para cada indivíduo seja modesto. Como tanto as doenças autoimunes quanto a anemia por deficiência de ferro são comuns, uma pequena mudança no risco pode se traduzir em muitos casos adicionais a nível populacional. Clinicians may therefore want to monitor iron status more proactively in these patients and address subtle drops before they lead to severe symptoms. Ao mesmo tempo, os achados incertos para outras doenças autoimunes ressaltam que nem todo sinal estatístico é clinicamente grande ou totalmente compreendido; serão necessários mais trabalhos em populações diversas e entre faixas etárias e sexos para esclarecer quem é mais vulnerável e por quê.
Citação: Chen, W., Wang, Y., Long, H. et al. Causal relationship between autoimmune diseases and iron deficiency anemia: a two-sample mendelian randomization study. Sci Rep 16, 12935 (2026). https://doi.org/10.1038/s41598-026-42356-8
Palavras-chave: doença autoimune, anemia por deficiência de ferro, doença inflamatória intestinal, artrite reumatoide, epidemiologia genética