Clear Sky Science · it
Relazione causale tra malattie autoimmuni e anemia da carenza di ferro: uno studio di randomizzazione mendeliana a due campioni
Perché questo è importante per la salute quotidiana
L’anemia da carenza di ferro è una delle cause più comuni di affaticamento e cattivo stato di salute a livello mondiale, eppure i medici non sempre sanno perché una determinata persona diventi anemica. Questo studio pone una domanda semplice ma rilevante: alcune malattie autoimmuni causano davvero un rischio maggiore di anemia da carenza di ferro, invece di limitarsi a manifestarsi negli stessi individui? Utilizzando grandi set di dati genetici anziché i tradizionali studi clinici, gli autori cercano di districare causa ed effetto in modo che potrebbe, in futuro, modificare il modo in cui i pazienti ad alto rischio vengono monitorati e trattati.
Legami nascosti tra immunità e basso ferro
Le malattie autoimmuni insorgono quando il sistema di difesa dell’organismo attacca per errore i propri tessuti, causando infiammazione cronica in organi come articolazioni, intestino, reni e tessuto connettivo. Separatamente, l’anemia da carenza di ferro si sviluppa quando l’organismo non dispone di ferro utilizzabile a sufficienza per produrre globuli rossi sani, lasciando le persone affaticate, fiato corto e meno capaci di concentrarsi. Studi osservazionali hanno a lungo osservato che persone con condizioni come l’artrite reumatoide o le malattie infiammatorie intestinali spesso presentano anche anemia, ma queste fotografie istantanee non possono mostrare se la malattia autoimmune aumenti realmente il rischio di carenza di ferro, o se altri fattori condivisi — come dieta, farmaci o perdita di sangue — siano i responsabili.
Usare i geni come esperimento naturale
I ricercatori si sono rivolti a un metodo chiamato randomizzazione mendeliana, che considera le differenze genetiche naturali come una sorta di “assegnazione” a vita a un rischio maggiore o minore di una data malattia. Poiché i geni sono fissati alla concezione e non vengono modificati dallo stile di vita, possono aiutare a separare la causa dalla coincidenza. Il team ha raccolto dati riassuntivi da molto grandi studi genetici su otto malattie autoimmuni — artrite reumatoide, malattia infiammatoria intestinale, colite ulcerosa, malattia di Crohn, celiachia, lupus eritematoso sistemico, spondilite anchilosante e nefrite membranosa — tutti in persone di ascendenza europea. Hanno quindi confrontato questi dati con informazioni genetiche su più di 15.000 persone con anemia da carenza di ferro e quasi 400.000 senza, provenienti dal progetto finlandese FinnGen.
Cosa mostrano le prove genetiche
Utilizzando diversi livelli di controlli di qualità, gli autori hanno selezionato varianti genetiche fortemente associate a ciascuna malattia autoimmune, cercando al contempo di evitare varianti che potrebbero influenzare l’anemia attraverso vie alternative. Il loro approccio statistico principale, supportato da più test di sensibilità, ha rilevato che le persone geneticamente predisposte all’artrite reumatoide, alla malattia infiammatoria intestinale e alla colite ulcerosa presentavano un aumento piccolo ma chiaro del rischio di anemia da carenza di ferro. I segnali per la celiachia, la spondilite anchilosante, la malattia di Crohn, il lupus sistemico e la nefrite membranosa erano più deboli: alcuni sembravano inizialmente collegati all’anemia, ma la forza di questi legami è diminuita o è scomparsa dopo che i ricercatori hanno rimosso varianti provenienti da una regione complessa del genoma correlata al sistema immunitario che può distorcere tali analisi.
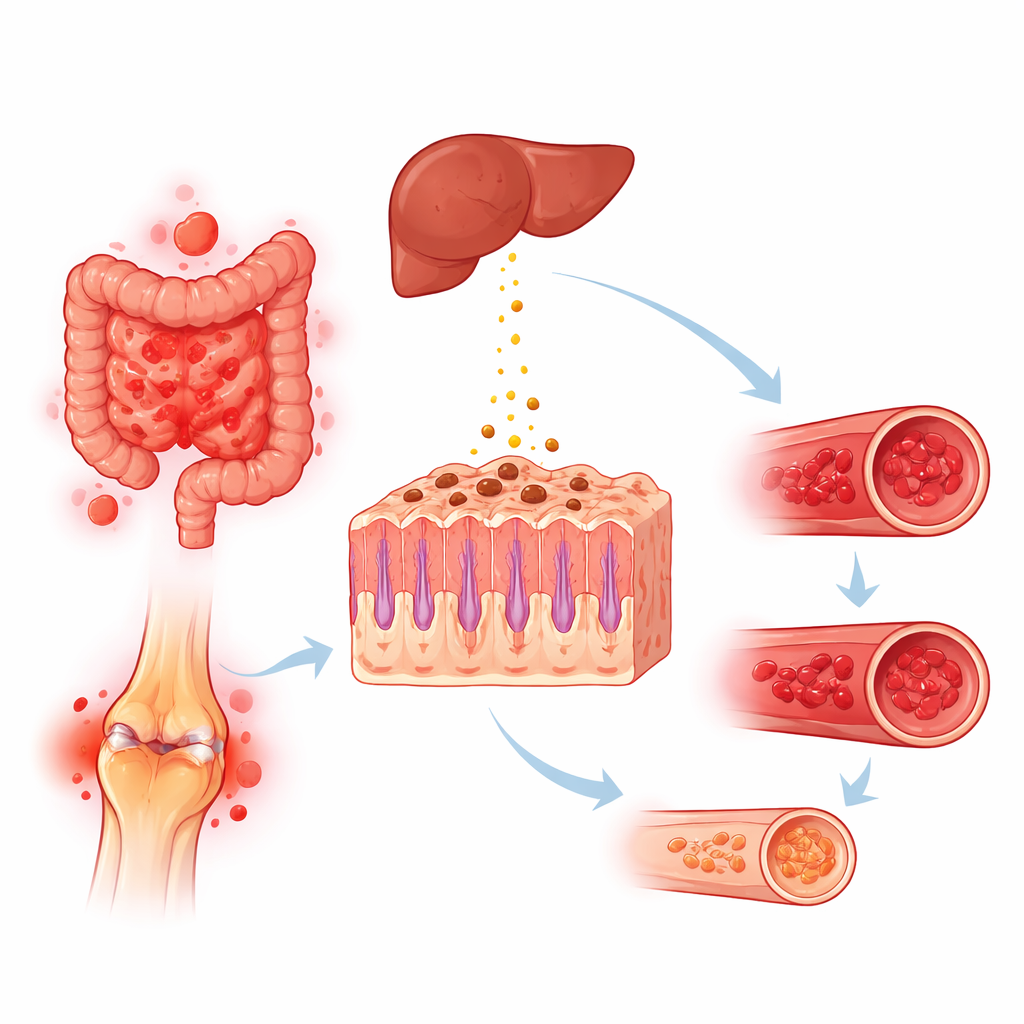
Come l’attività autoimmune può prosciugare il ferro
Diverse vie biologiche potrebbero spiegare perché le malattie autoimmuni, specialmente quelle che coinvolgono l’intestino e l’infiammazione cronica, spingono verso la carenza di ferro. I disturbi intestinali possono causare sanguinamento interno lento, scarsa assorbimento dei nutrienti o danni alla porzione superiore dell’intestino tenue dove avviene la maggior parte dell’assorbimento del ferro. L’uso prolungato di farmaci antidolorifici nelle malattie articolari può inoltre aumentare il sanguinamento da stomaco e intestino. Contemporaneamente, i segnali infiammatori tipici dell’autoimmunità stimolano il fegato a rilasciare l’epcidina, un ormone che trattiene il ferro all’interno delle cellule di deposito e ne riduce il passaggio dall’intestino al flusso sanguigno. Il risultato può essere una perdita assoluta di ferro, un blocco funzionale nell’utilizzo del ferro, o entrambi, causando anemia anche quando le riserve corporee complessive di ferro non sono completamente esaurite.
Cosa significa per il futuro
Per una persona che convive con artrite reumatoide o malattia infiammatoria intestinale, lo studio suggerisce che la loro condizione fa più che coesistere con l’anemia: probabilmente la favorisce, anche se l’aumento del rischio per ciascun individuo è modesto. Poiché sia le malattie autoimmuni sia l’anemia da carenza di ferro sono comuni, un piccolo spostamento del rischio può tradursi in molti casi aggiuntivi a livello di popolazione. I clinici potrebbero quindi voler monitorare lo stato del ferro in questi pazienti in modo più proattivo e intervenire su cali lievi prima che conducano a sintomi gravi. Allo stesso tempo, i risultati incerti per altre malattie autoimmuni sottolineano che non ogni segnale statistico è clinicamente rilevante o completamente compreso; saranno necessari ulteriori studi in popolazioni diverse e attraverso gruppi di età e sesso per chiarire chi è più vulnerabile e perché.
Citazione: Chen, W., Wang, Y., Long, H. et al. Causal relationship between autoimmune diseases and iron deficiency anemia: a two-sample mendelian randomization study. Sci Rep 16, 12935 (2026). https://doi.org/10.1038/s41598-026-42356-8
Parole chiave: malattia autoimmune, anemia da carenza di ferro, malattia infiammatoria intestinale, artrite reumatoide, epidemiologia genetica