Clear Sky Science · fr
Relation causale entre les maladies auto-immunes et l’anémie ferriprive : une étude de randomisation mendélienne à deux échantillons
Pourquoi c’est important pour la santé quotidienne
L’anémie ferriprive est l’une des causes les plus fréquentes de fatigue et de mauvaise santé dans le monde, pourtant les médecins ne savent pas toujours pourquoi une personne devient anémique. Cette étude pose une question simple mais importante : certaines maladies auto-immunes causent-elles réellement un risque accru d’anémie ferriprive, plutôt que de simplement coexister chez les mêmes personnes ? En utilisant de larges jeux de données génétiques plutôt que des essais cliniques classiques, les auteurs cherchent à démêler la causalité de la simple association d’une manière qui pourrait, à terme, modifier la surveillance et la prise en charge des patients à haut risque.
Liens cachés entre le système immunitaire et la carence en fer
Les maladies auto-immunes surviennent lorsque le système de défense de l’organisme attaque par erreur ses propres tissus, entraînant une inflammation chronique d’organes tels que les articulations, les intestins, les reins et le tissu conjonctif. De leur côté, les anémies ferriprives se développent lorsque l’organisme ne dispose pas d’assez de fer utilisable pour fabriquer des globules rouges sains, laissant les personnes fatiguées, essoufflées et moins capables de se concentrer. Les études observationnelles ont depuis longtemps noté que les personnes atteintes de pathologies comme la polyarthrite rhumatoïde ou la maladie inflammatoire de l’intestin présentent souvent aussi une anémie, mais ces photographies instantanées ne permettent pas de savoir si la maladie auto-immune augmente réellement le risque de carence en fer, ou si d’autres facteurs partagés — alimentation, médicaments ou pertes sanguines — en sont responsables.
Utiliser les gènes comme expérience naturelle
Les chercheurs ont eu recours à une méthode appelée randomisation mendélienne, qui considère les différences génétiques naturelles comme une sorte « d’attribution » à long terme d’un risque plus élevé ou plus faible d’une maladie donnée. Parce que les gènes sont fixés à la conception et ne sont pas modifiés par le mode de vie, ils aident à séparer la cause de la coïncidence. L’équipe a rassemblé des données récapitulatives issues de très grandes études génétiques portant sur huit maladies auto-immunes — polyarthrite rhumatoïde, maladie inflammatoire de l’intestin, rectocolite hémorragique, maladie de Crohn, maladie cœliaque, lupus érythémateux systémique, spondylarthrite ankylosante et néphropathie membraneuse — toutes chez des personnes d’ascendance européenne. Ils ont ensuite comparé ces données à des données génétiques de plus de 15 000 personnes atteintes d’anémie ferriprive et d’environ 400 000 personnes non atteintes, issues du projet finlandais FinnGen.
Ce que montrent les preuves génétiques
Après plusieurs niveaux de vérification de qualité, les auteurs ont sélectionné des variantes génétiques fortement liées à chaque maladie auto-immune, en évitant autant que possible les variantes susceptibles d’influencer l’anémie par d’autres voies. Leur approche statistique principale, appuyée par de multiples tests de sensibilité, a montré que les personnes prédisposées génétiquement à la polyarthrite rhumatoïde, à la maladie inflammatoire de l’intestin et à la rectocolite hémorragique présentaient une augmentation modeste mais nette du risque d’anémie ferriprive. Les signaux pour la maladie cœliaque, la spondylarthrite ankylosante, la maladie de Crohn, le lupus systémique et la néphropathie membraneuse étaient plus faibles : certains semblaient liés à l’anémie au départ, mais l’intensité de ces liens a diminué ou disparu après que les chercheurs eurent retiré des variantes situées dans une région complexe du génome liée au système immunitaire, susceptible de fausser ce type d’analyse.
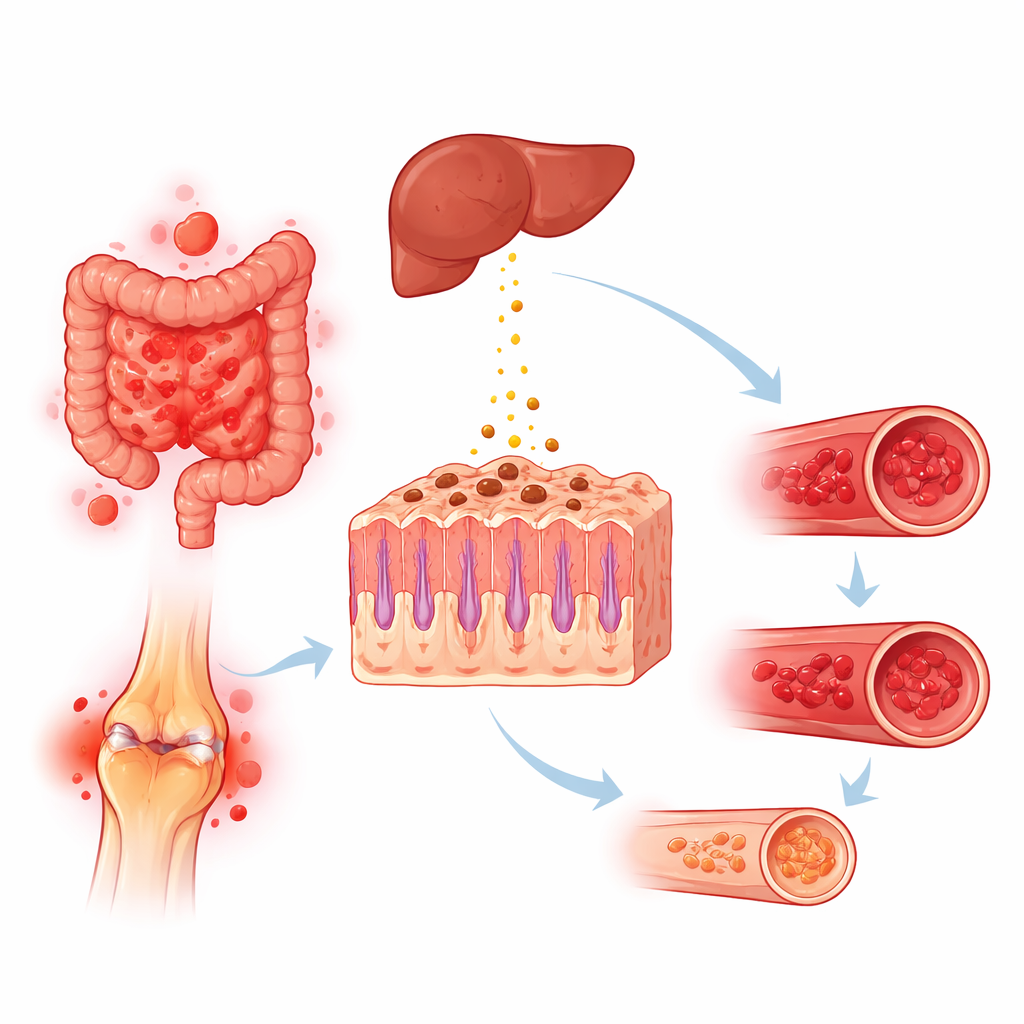
Comment l’activité auto-immune peut épuiser le fer
Plusieurs voies biologiques peuvent expliquer pourquoi les maladies auto-immunes, en particulier celles qui touchent l’intestin et s’accompagnent d’une inflammation chronique, favorisent la carence en fer. Les troubles intestinaux peuvent provoquer des saignements internes lents, une mauvaise absorption des nutriments ou des lésions de l’intestin grêle supérieur où s’effectue la majeure partie de l’absorption du fer. L’utilisation prolongée d’anti-inflammatoires dans les maladies articulaires peut également augmenter les saignements gastriques et intestinaux. Parallèlement, les signaux inflammatoires fréquents en auto-immunité stimulent le foie à libérer l’hepcidine, une hormone qui piège le fer dans les cellules de stockage et réduit son passage de l’intestin vers la circulation sanguine. Le résultat peut être une perte absolue de fer, un blocage fonctionnel de son utilisation, ou les deux, entraînant une anémie même lorsque les réserves corporelles de fer ne sont pas complètement épuisées.
Implications pour l’avenir
Pour une personne atteinte de polyarthrite rhumatoïde ou de maladie inflammatoire de l’intestin, l’étude suggère que sa maladie fait plus que simplement coexister avec une anémie — elle la favorise probablement, même si l’augmentation du risque pour chaque individu reste modeste. Comme les maladies auto-immunes et l’anémie ferriprive sont courantes, un faible déplacement du risque peut se traduire par de nombreux cas supplémentaires au niveau de la population. Les cliniciens pourraient donc envisager de surveiller l’état du fer de manière plus proactive chez ces patients et de corriger des diminutions subtiles avant qu’elles ne provoquent des symptômes sévères. En même temps, les résultats incertains pour d’autres maladies auto-immunes soulignent que tout signal statistique n’est pas nécessairement d’importance clinique majeure ni complètement compris ; des travaux supplémentaires dans des populations diverses et selon l’âge et le sexe seront nécessaires pour clarifier qui est le plus vulnérable et pourquoi.
Citation: Chen, W., Wang, Y., Long, H. et al. Causal relationship between autoimmune diseases and iron deficiency anemia: a two-sample mendelian randomization study. Sci Rep 16, 12935 (2026). https://doi.org/10.1038/s41598-026-42356-8
Mots-clés: maladie auto-immune, anémie ferriprive, maladie inflammatoire de l’intestin, polyarthrite rhumatoïde, épidémiologie génétique