Clear Sky Science · de
Kausaler Zusammenhang zwischen Autoimmunerkrankungen und Eisenmangelanämie: eine Two‑Sample‑Mendelian‑Randomization‑Studie
Warum das für die Alltagsgesundheit wichtig ist
Eisenmangelanämie gehört weltweit zu den häufigsten Ursachen für Müdigkeit und schlechte Gesundheit, doch Ärztinnen und Ärzte wissen nicht immer, warum eine bestimmte Person anämisch wird. Diese Studie stellt eine einfache, aber wichtige Frage: Verursachen bestimmte Autoimmunerkrankungen tatsächlich ein höheres Risiko für Eisenmangelanämie, anstatt nur zufällig bei denselben Personen aufzutreten? Indem die Autorinnen und Autoren große genetische Datensätze statt herkömmlicher klinischer Studien nutzen, versuchen sie, Ursache und Wirkung zu entwirren — auf eine Weise, die langfristig verändern könnte, wie Patientinnen und Patienten mit erhöhtem Risiko überwacht und behandelt werden.
Verborgene Verknüpfungen zwischen Immunität und Eisenmangel
Autoimmunerkrankungen entstehen, wenn das Abwehrsystem des Körpers fälschlicherweise eigenes Gewebe angreift und zu lang anhaltenden Entzündungen in Organen wie Gelenken, Darm, Nieren und Bindegewebe führt. Eisenmangelanämie entsteht separiert, wenn dem Körper nicht genügend verwertbares Eisen für die Produktion gesunder roter Blutkörperchen zur Verfügung steht; Betroffene sind dann müde, kurzatmig und weniger konzentriert. Beobachtungsstudien haben schon lange festgestellt, dass Menschen mit Erkrankungen wie rheumatoider Arthritis oder entzündlichen Darmerkrankungen häufig auch eine Anämie haben. Solche Momentaufnahmen können jedoch nicht zeigen, ob die Autoimmunerkrankung tatsächlich das Eisenmangelrisiko erhöht oder ob andere gemeinsame Faktoren — etwa Ernährung, Medikamente oder Blutverlust — verantwortlich sind.
Gene als natürliches Experiment nutzen
Die Forschenden nutzten eine Methode namens Mendelsche Randomisierung, die natürlich vorkommende genetische Unterschiede als eine Art lebenslange „Zuweisung" zu einem höheren oder niedrigeren Risiko für eine bestimmte Krankheit betrachtet. Weil Gene bei der Zeugung festgelegt sind und nicht durch Lebensstil verändert werden, können sie helfen, Ursache von Zufall zu trennen. Das Team sammelte Summary‑Daten aus sehr großen genetischen Studien zu acht Autoimmunerkrankungen — rheumatoide Arthritis, entzündliche Darmerkrankung, Colitis ulcerosa, Morbus Crohn, Zöliakie, systemischer Lupus erythematodes, ankylosierende Spondylitis und membranöse Nephropathie — jeweils bei Menschen europäischer Abstammung. Diese verglichen sie mit genetischen Daten von mehr als 15.000 Menschen mit Eisenmangelanämie und fast 400.000 ohne aus dem finnischen FinnGen‑Projekt.
Was die genetischen Befunde zeigen
Mithilfe mehrerer Qualitätskontrollen wählten die Autorinnen und Autoren genetische Varianten aus, die stark mit jeder Autoimmunerkrankung verknüpft sind, und versuchten gleichzeitig, Varianten zu vermeiden, die Anämie auf anderem Weg beeinflussen könnten. Ihr hauptsächlicher statistischer Ansatz, gestützt durch mehrere Sensitivitätstests, ergab, dass genetisch bedingte Prädispositionen für rheumatoide Arthritis, entzündliche Darmerkrankung und Colitis ulcerosa mit einem kleinen, aber klaren erhöhten Risiko für Eisenmangelanämie einhergehen. Signale für Zöliakie, ankylosierende Spondylitis, Morbus Crohn, systemischen Lupus und membranöse Nephropathie waren schwächer: Einige schienen zunächst mit Anämie verknüpft, doch die Stärke dieser Zusammenhänge nahm ab oder verschwand, nachdem die Forschenden Varianten aus einer komplexen, immunbezogenen Region des Genoms entfernt hatten, die solche Analysen verzerren kann.
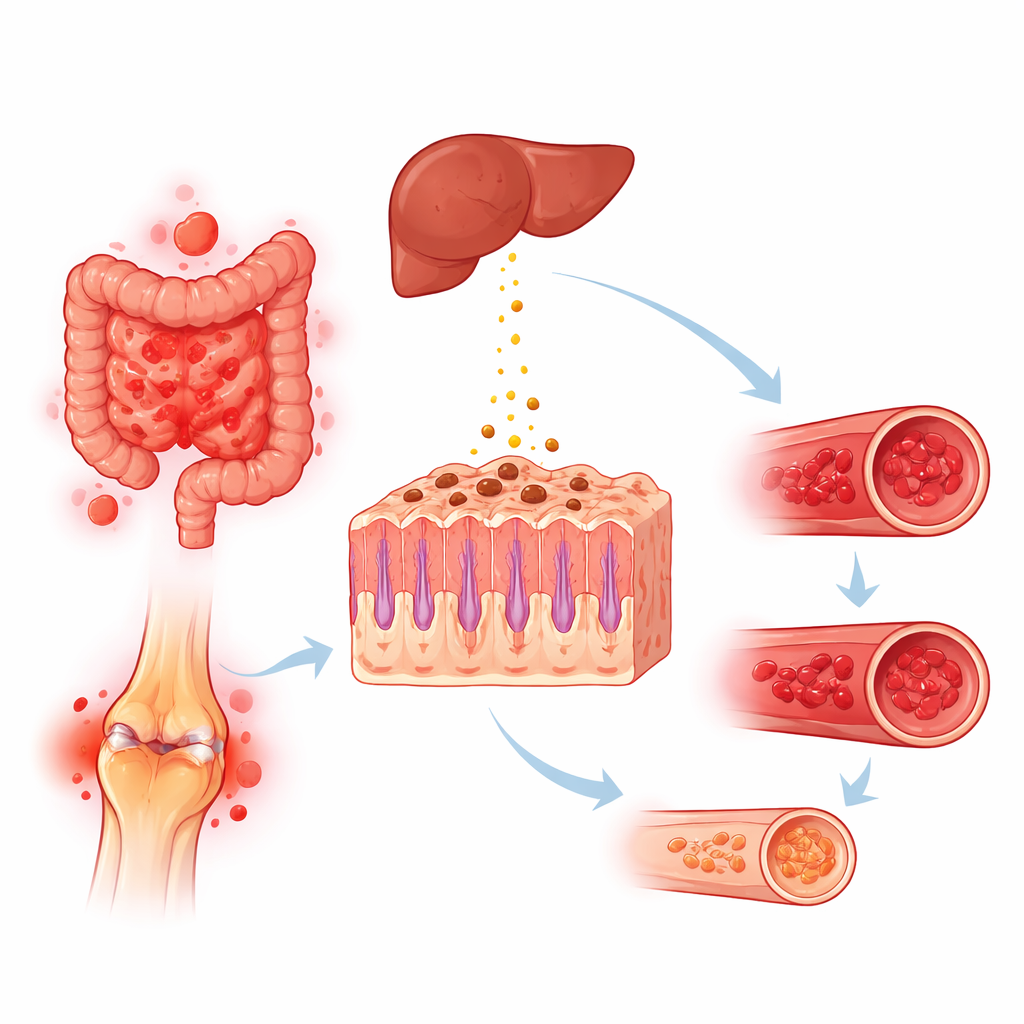
Wie autoimmune Aktivität Eisen entziehen kann
Mehrere biologische Mechanismen könnten erklären, warum Autoimmunerkrankungen, insbesondere solche mit Darmbeteiligung und chronischer Entzündung, Menschen in Richtung Eisenmangel treiben. Darmstörungen können zu langsamem inneren Blutverlust, schlechter Nährstoffaufnahme oder Schäden am oberen Dünndarm führen, wo der Großteil des Eisens aufgenommen wird. Langfristiger Einsatz von Schmerzmitteln bei Gelenkerkrankungen kann ebenfalls Blutungen im Magen‑Darm‑Trakt begünstigen. Gleichzeitig regen entzündliche Signale, die bei Autoimmunität häufig vorkommen, die Leber zur Freisetzung von Hepcidin an — einem Hormon, das Eisen in Speicherzellen „einsperrt“ und dessen Übertritt aus dem Darm in den Blutkreislauf vermindert. Ergebnis kann entweder ein tatsächlicher Eisenverlust, eine funktionelle Blockade der Eisenverfügbarkeit oder beides sein, sodass eine Anämie entstehen kann, auch wenn die gesamten körpereigenen Eisenspeicher nicht vollständig aufgebraucht sind.
Was das für die Zukunft bedeutet
Für eine Person mit rheumatoider Arthritis oder entzündlicher Darmerkrankung legt die Studie nahe, dass ihre Erkrankung mehr tut, als nur mit Anämie koexistieren — sie trägt wahrscheinlich zu ihrer Entstehung bei, auch wenn das individuelle Risikozuwachs moderat ist. Da sowohl Autoimmunerkrankungen als auch Eisenmangelanämie häufig vorkommen, kann eine kleine Verschiebung des Risikos auf Bevölkerungsebene viele zusätzliche Fälle bedeuten. Klinikerinnen und Kliniker sollten daher erwägen, den Eisenstatus bei diesen Patientengruppen proaktiver zu überwachen und subtile Abnahmen zu behandeln, bevor schwere Symptome auftreten. Gleichzeitig unterstreichen die unsicheren Befunde für andere Autoimmunerkrankungen, dass nicht jedes statistische Signal klinisch groß oder vollständig verstanden ist; weitere Untersuchungen in verschiedenartigen Bevölkerungen sowie über Alters‑ und Geschlechtsgruppen hinweg sind nötig, um zu klären, wer am meisten gefährdet ist und warum.
Zitation: Chen, W., Wang, Y., Long, H. et al. Causal relationship between autoimmune diseases and iron deficiency anemia: a two-sample mendelian randomization study. Sci Rep 16, 12935 (2026). https://doi.org/10.1038/s41598-026-42356-8
Schlüsselwörter: Autoimmunerkrankung, Eisenmangelanämie, entzündliche Darmerkrankung, rheumatoide Arthritis, genetische Epidemiologie