Clear Sky Science · pt
A classe I de MHC nas células‑alvo regula a imunidade mediada por células T CD4+
Por que esta descoberta imunológica importa
Costumamos descrever o sistema imunológico como um exército com funções bem definidas: algumas células detectam ameaças, outras lembram combates anteriores e outras executam o ataque. Este estudo derruba uma regra de longa data sobre quem pode atacar quais alvos. Os pesquisadores mostram que um marcador comum em nossas células, chamado MHC classe I, faz mais do que simplesmente ajudar um tipo de célula imune a reconhecer perigo. Quando esse marcador está ausente, ele muda de forma inesperada a capacidade de outro tipo de célula imune, as células T CD4+, de matar tanto tecidos normais quanto células tumorais. Os resultados podem ajudar a explicar por que alguns cânceres que se escondem do sistema imune ainda respondem bem às imunoterapias modernas, além de apontar novas formas de tratar câncer e complicações de transplantes de medula óssea.
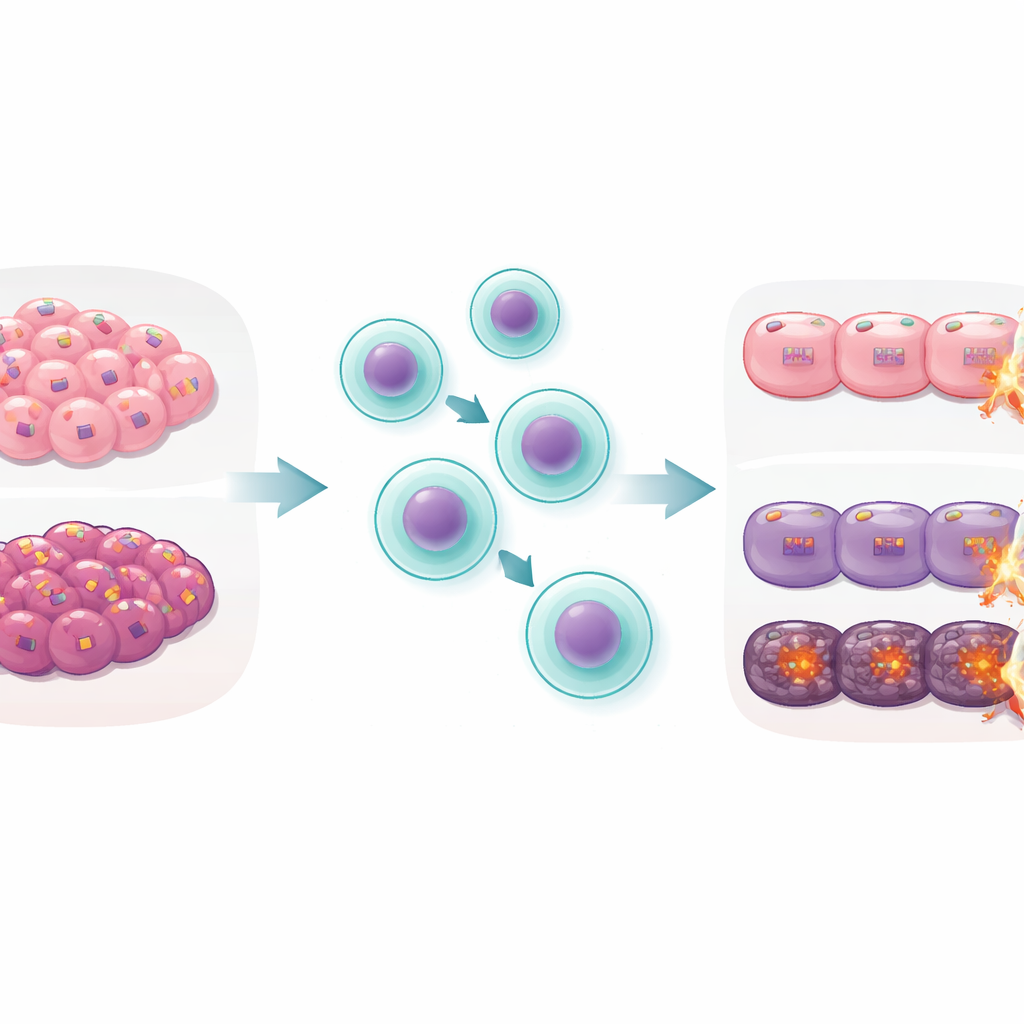
Um crachá de segurança com uma função oculta
Toda célula nucleada do nosso corpo normalmente carrega moléculas de MHC classe I na superfície, como crachás de identificação exibindo pequenos fragmentos de proteína. Os livros didáticos dizem que esses crachás servem principalmente para as células T CD8, as clássicas células “assassinas”, enquanto um tipo diferente de crachá, o MHC classe II, orienta as células T CD4, as células “auxiliares”. Muitos vírus e tumores escapam das células T CD8 reduzindo seus crachás de MHC I — um truque de evasão bem conhecido. Os autores fizeram uma pergunta em grande parte negligenciada: além de seu papel como crachá para células T CD8 e células NK, o MHC I na própria célula‑alvo altera o quão vulnerável essa célula é a ser destruída por células T CD4?
Quando crachás ausentes tornam tecidos frágeis
Para testar isso, a equipe usou modelos de camundongos de uma complicação grave do transplante de medula óssea chamada doença do enxerto contra o hospedeiro, em que células imunes do doador atacam o intestino e outros órgãos do receptor. Eles geraram camundongos cujos tecidos careciam de MHC I, enquanto as células doadoras ainda viam os mesmos sinais estranhos de MHC II. Esse arranjo isola o dano dirigido por células T CD4. Surpreendentemente, camundongos cujas células intestinais não tinham MHC I apresentaram doença muito mais grave e morreram com mais frequência do que camundongos normais, embora as células T CD4 doadoras estivessem ativadas em grau semelhante em ambos os grupos. O dano extra não apareceu quando o intestino foi lesionado apenas por produtos químicos ou radiação, e não dependia de células NK. Isso apontou para uma vulnerabilidade específica de tecidos deficientes em MHC I ao ataque de células T CD4, e não para uma fragilidade geral.
Cânceres que se escondem tornam‑se alvos mais fáceis
Os pesquisadores então se voltaram para o melanoma, um câncer de pele comum. Eles usaram edição gênica para remover o MHC I de células de melanoma de camundongos. Em culturas, essas células tumorais deficientes em MHC I foram mortas com mais eficiência por células T CD4 que reconheciam um antígeno de melanoma. Em camundongos, tumores sem MHC I encolheram mais após a transferência dessas células T CD4 do que tumores com MHC I normal. Esses resultados sugerem que, quando os cânceres perdem MHC I para escapar das células T CD8, podem inadvertidamente tornar‑se mais vulneráveis a outro tipo de ataque imune conduzido por células T CD4, especialmente sob condições terapêuticas adequadas.
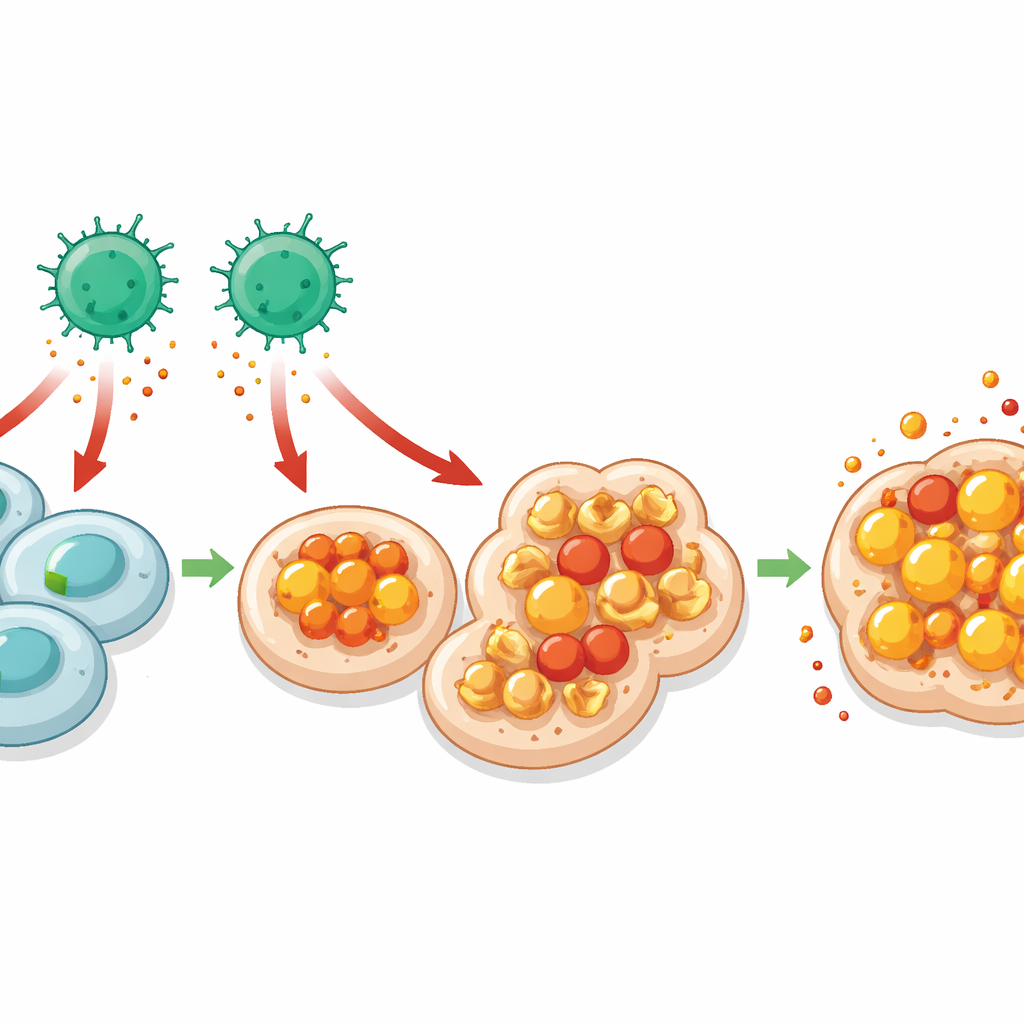
Ferro, gorduras oxidadas e uma morte celular flamejante
Investigando mais a fundo, a equipe perguntou por que células deficientes em MHC I são mais fáceis de serem mortas por células T CD4. Análises de RNA de célula única das células intestinais revelaram sinais mais fortes de resposta ao interferon‑gama, um potente sinal de alarme frequentemente liberado por células T, especificamente nas células que não tinham MHC I. Essas mesmas células exibiram assinaturas de manejo de ferro perturbado e aumento da peroxidação lipídica — dano químico às gorduras nas membranas celulares. Juntas, essas características apontam para a ferroptose, uma forma de morte celular dependente de ferro marcada pela oxidação descontrolada de lipídios. Os autores confirmaram que células intestinais e tumorais sem MHC I acumularam mais dano lipídico e foram protegidas quando o ferro foi quelado ou quando a ferroptose foi quimicamente bloqueada. Neutralizar o interferon‑gama reduziu esse dano, ligando os sinais derivados de células T CD4 à ferroptose nas células‑alvo vulneráveis.
Pistas de pacientes em imunoterapia
Para saber se esse mecanismo poderia importar em humanos, os pesquisadores analisaram grandes conjuntos de dados de pacientes com melanoma e câncer colorretal tratados com bloqueadores de pontos de controle imune. Em vários estudos, tumores com baixa expressão de MHC I tendiam a conter mais células T CD4, mas não mais células T CD8, e, no melanoma, pacientes cujos tumores com MHC I baixo tinham abundantes células T CD4 viveram mais. Tumores com MHC I baixo também mostraram sinais moleculares de defesas anti‑ferroptose mais fracas e respostas mais fortes a interferon‑gama, ecoando os padrões observados em camundongos. Essas descobertas sugerem que, em alguns cânceres humanos, reduzir o MHC I não desliga simplesmente o ataque imune; em vez disso, pode deslocar o equilíbrio para uma morte do tipo ferroptose dirigida por células T CD4.
O que isso significa para tratamentos futuros
No geral, o estudo revela que o MHC classe I nas células‑alvo funciona como mais do que uma etiqueta de reconhecimento para células T CD8; ele também ajuda a proteger tecidos normais e tumores da morte celular dependente de ferro induzida por células T CD4. Quando esse escudo é perdido, células T CD4 que reconhecem o alvo via MHC II podem desencadear dano oxidativo intenso e ferroptose, agravando lesões intestinais relacionadas ao transplante, mas potencialmente melhorando o controle de determinados cânceres. Para pacientes, essa nova compreensão pode orientar estratégias que aproveitem intencionalmente células T CD4 e a ferroptose para tratar tumores que perderam MHC I, ao mesmo tempo em que aponta para drogas que modulam o ferro como forma de proteger tecidos vulneráveis durante o transplante de medula óssea.
Citação: Lauder, E., Gondal, M., Wu, MC. et al. MHC class I on target cells regulates CD4+ T cell-mediated immunity. Nat Immunol 27, 1000–1012 (2026). https://doi.org/10.1038/s41590-026-02480-z
Palavras-chave: células T CD4, MHC classe I, ferroptose, imunoterapia contra o câncer, doença do enxerto contra o hospedeiro