Clear Sky Science · es
La clase I de MHC en las células diana regula la inmunidad mediada por células T CD4+
Por qué importa esta historia inmunológica
Nuestro sistema inmune a menudo se describe como un ejército con roles claramente asignados: algunas células detectan amenazas, otras recuerdan batallas pasadas y otras atacan. Este estudio derriba una regla antigua sobre quién puede atacar a qué objetivos. Los investigadores demuestran que un marcador común en nuestras células, llamado MHC clase I, hace más que ayudar a un tipo de células inmunitarias a reconocer el peligro. Cuando este marcador falta, cambia de forma inesperada cómo otro tipo de célula inmunitaria, las células T CD4, pueden matar tanto tejidos normales como células cancerosas. Los resultados pueden ayudar a explicar por qué algunos cánceres que se ocultan del sistema inmune aún responden bien a las inmunoterapias modernas, y señalan nuevas vías para tratar el cáncer y las complicaciones de los trasplantes de médula ósea.
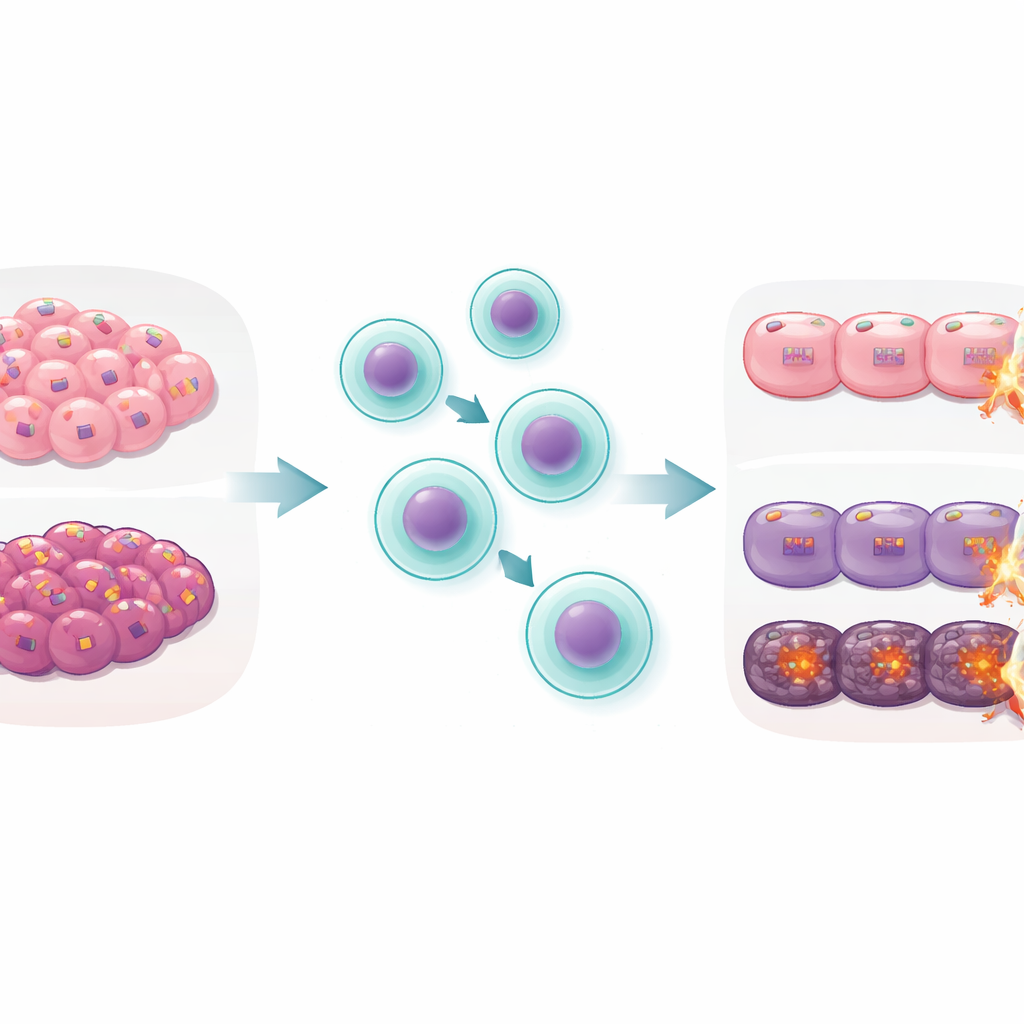
Una placa de seguridad con un trabajo oculto
Toda célula nucleada de nuestro cuerpo normalmente porta moléculas de MHC clase I en su superficie, como placas de seguridad que muestran pequeños fragmentos proteicos. Los libros de texto dicen que estas placas son principalmente para las células T CD8, las “asesinas” clásicas, mientras que otro tipo de placa, el MHC clase II, guía a las células T CD4, las “auxiliares”. Muchos virus y tumores eluden a las células T CD8 reduciendo sus placas de MHC I, un truco de escape bien conocido. Los autores se plantearon una pregunta en gran parte descuidada: más allá de su papel como placa para las células T CD8 y las células asesinas naturales, ¿cambia el MHC I en la propia célula diana la vulnerabilidad de esa célula frente a la destrucción por células T CD4?
Cuando faltan placas y los tejidos se vuelven frágiles
Para probarlo, el equipo utilizó modelos murinos de una complicación grave del trasplante de médula denominada enfermedad injerto contra huésped, en la que las células inmunitarias del donante atacan el intestino u otros órganos del receptor. Diseñaron ratones cuyos tejidos carecían de MHC I pero cuyos linfocitos entrantes seguían percibiendo las mismas señales extranjeras de MHC II. Este diseño aísla el daño impulsado por células T CD4. Sorprendentemente, los ratones cuyos enterocitos carecían de MHC I sufrieron una enfermedad mucho más grave y murieron con mayor frecuencia que los ratones normales, a pesar de que las células T CD4 del donante estaban activadas en un grado similar en ambos grupos. El daño adicional no apareció cuando el intestino se lesionó solo con productos químicos o radiación, y no dependía de las células asesinas naturales. Esto apuntó a una vulnerabilidad específica de los tejidos deficientes en MHC I frente al ataque de las células T CD4, no a una fragilidad general.
Los cánceres que se esconden se vuelven objetivos más fáciles
Los investigadores pasaron luego al melanoma, un cáncer de piel común. Emplearon edición genética para eliminar el MHC I de células de melanoma murino. En cultivos, estas células tumorales deficientes en MHC I fueron eliminadas con más eficacia por células T CD4 que reconocían un antígeno de melanoma. En ratones, los tumores sin MHC I se redujeron más tras la transferencia de esas células T CD4 que los tumores con MHC I normal. Estos resultados sugieren que cuando los cánceres pierden MHC I para evitar a las células T CD8, pueden, sin querer, volverse más vulnerables a un tipo distinto de ataque inmunitario impulsado por células T CD4, especialmente en condiciones terapéuticas adecuadas.
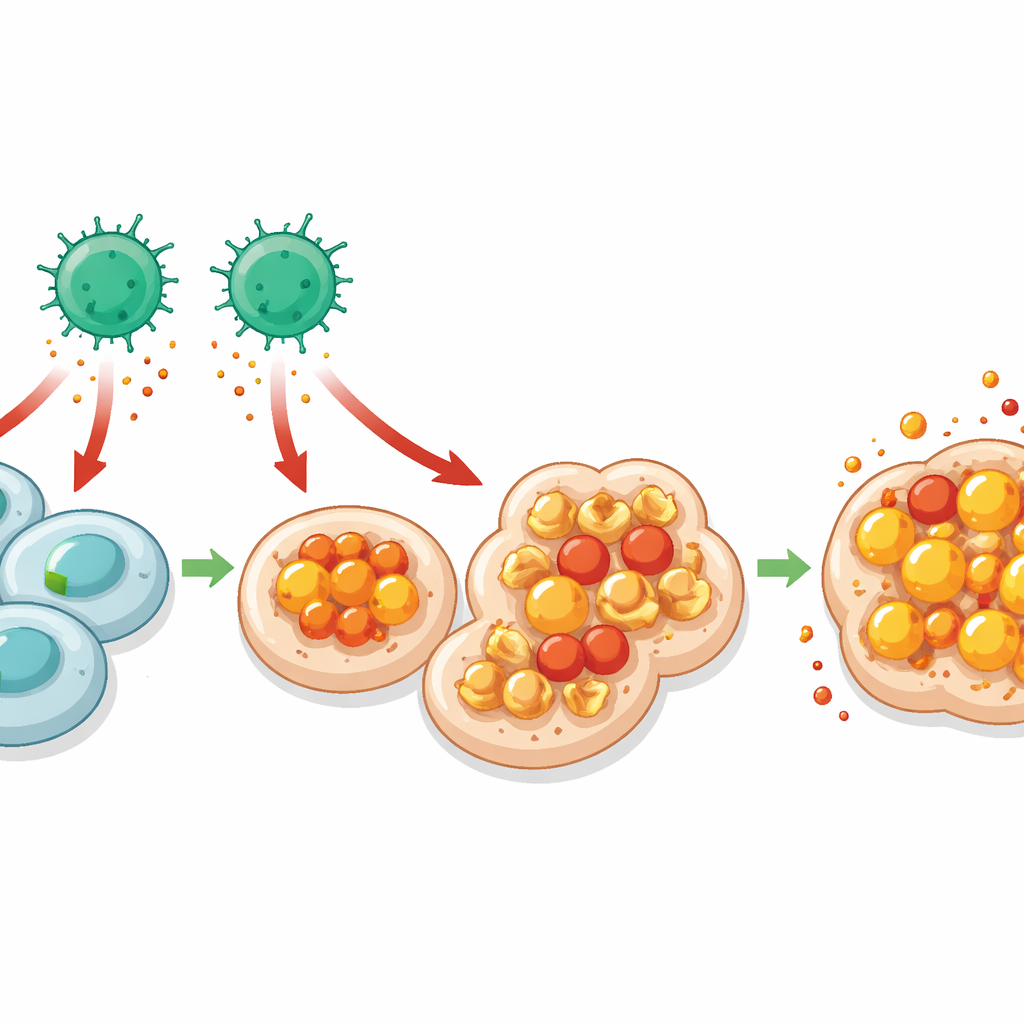
Hierro, grasas oxidadas y una muerte celular ardiente
Profundizando, el equipo preguntó por qué las células deficientes en MHC I son más fáciles de eliminar por las células T CD4. La secuenciación de ARN de célula única de células intestinales reveló señales más intensas de respuesta a interferón-gamma, una potente señal de alarma a menudo liberada por las células T, específicamente en las células sin MHC I. Esas mismas células mostraron huellas de manejo de hierro alterado y un aumento de la peroxidación lipídica: daño químico a las grasas en las membranas celulares. En conjunto, estas características apuntan a la ferroptosis, una forma de muerte celular dependiente del hierro marcada por la oxidación descontrolada de lípidos. Los autores confirmaron que las células intestinales y tumorales sin MHC I acumulaban más daño lipídico y estaban protegidas cuando se quelaba el hierro o se bloqueaba químicamente la ferroptosis. Neutralizar el interferón-gamma redujo este daño, vinculando las señales derivadas de células T CD4 con la ferroptosis en las células diana vulnerables.
Pistas de pacientes bajo inmunoterapia
Para ver si este mecanismo podría importar en humanos, los investigadores analizaron grandes conjuntos de datos de pacientes con melanoma y cáncer de colon tratados con inhibidores de puntos de control inmunitario. En varios estudios, los tumores con baja expresión de MHC I tendían a contener más células T CD4 pero no más células T CD8, y en melanoma, los pacientes cuyos tumores con bajo MHC I tenían abundantes células T CD4 vivieron más tiempo. Los tumores con bajo MHC I también mostraron señales moleculares de defensas anti‑ferroptosis más débiles y respuestas a interferón‑gamma más fuertes, reflejando los patrones observados en ratones. Estos hallazgos sugieren que, en algunos cánceres humanos, la reducción del MHC I no apaga simplemente el ataque inmune; en cambio, puede cambiar el equilibrio hacia una eliminación tipo ferroptosis impulsada por células T CD4.
Qué significa esto para tratamientos futuros
En conjunto, el estudio revela que el MHC clase I en las células diana actúa como algo más que una etiqueta de reconocimiento para las células T CD8; también ayuda a proteger tejidos normales y tumores de la muerte celular dependiente del hierro inducida por células T CD4. Cuando se pierde este escudo, las células T CD4 que reconocen el objetivo mediante MHC II pueden desencadenar un daño oxidativo intenso y ferroptosis, empeorando la lesión intestinal relacionada con trasplantes pero potencialmente mejorando el control de ciertos cánceres. Para los pacientes, esta nueva comprensión podría orientar estrategias que aprovechen intencionalmente las células T CD4 y la ferroptosis para tratar tumores que han perdido MHC I, a la vez que señalan a fármacos moduladores del hierro como forma de proteger tejidos vulnerables durante el trasplante de médula ósea.
Cita: Lauder, E., Gondal, M., Wu, MC. et al. MHC class I on target cells regulates CD4+ T cell-mediated immunity. Nat Immunol 27, 1000–1012 (2026). https://doi.org/10.1038/s41590-026-02480-z
Palabras clave: células T CD4, MHC clase I, ferroptosis, inmunoterapia del cáncer, enfermedad injerto contra huésped