Clear Sky Science · ja
標的細胞上のMHC class IはCD4+ T細胞媒介の免疫を制御する
この免疫の話が重要な理由
免疫系はしばしば明確に役割分担された軍隊に例えられます:ある細胞は敵を察知し、ある細胞は過去の戦いを記憶し、別の細胞が実際に攻撃を行います。本研究は、どの細胞がどの標的を攻撃できるかについての長年の定説を覆します。研究者たちは、MHC class Iと呼ばれる細胞表面の一般的なマーカーが、単にある種の免疫細胞に危険を認識させる以上の働きをしていることを示しました。このマーカーが欠失すると、予期せずに別の免疫細胞であるCD4 T細胞の、正常組織やがん細胞の殺傷のされ方が変わるのです。これらの結果は、免疫から身を隠す一部のがんが最新の免疫療法に良好に反応する理由を説明する助けになり得るほか、がん治療や骨髄移植に伴う合併症の新たな治療方針を示唆します。
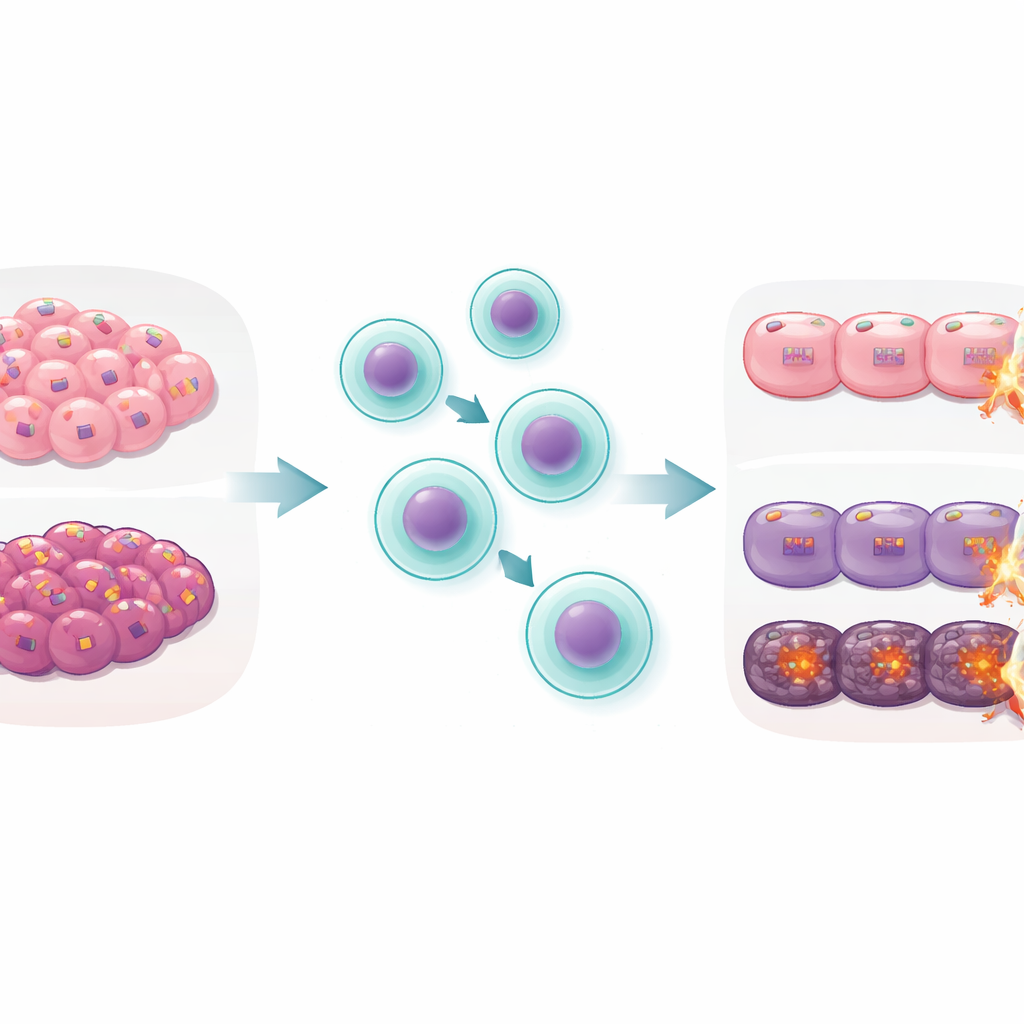
隠れた役割を持つ身分証明バッジ
私たちの体のすべての有核細胞は通常、MHC class I分子を表面に持ち、小さなタンパク断片を示す身分証のように振る舞います。教科書的には、これらのバッジは主に古典的な“キラー”細胞であるCD8 T細胞のためのもので、CD4 T細胞(“ヘルパー”細胞)には別のタイプのバッジであるMHC class IIが案内役を果たすとされています。多くのウイルスや腫瘍はMHC Iの発現を減少させてCD8 T細胞を回避する、よく知られた逃避戦略を取ります。著者らは見落とされがちだった疑問を投げかけました:標的細胞上のMHC Iは、CD8 T細胞やナチュラルキラー細胞のためのバッジとしての役割を超えて、CD4 T細胞による標的の脆弱性を変えるのでしょうか?
バッジが欠けると組織が脆くなるとき
この問いを検証するために、研究チームは移植片対宿主病と呼ばれる骨髄移植後の重篤な合併症のマウスモデルを用いました。ここではドナー由来の免疫細胞が受容体の腸や他の臓器を攻撃します。彼らは、組織がMHC Iを欠くように遺伝子改変したマウスを作り、同時に侵入するドナー細胞は同じ異種のMHC IIシグナルを認識するようにしました。この配置によりCD4 T細胞が駆動するダメージを孤立して評価できます。驚くべきことに、腸細胞がMHC Iを欠くマウスは、ドナーのCD4 T細胞の活性化度合いは両群でほぼ同じであったにもかかわらず、通常のマウスよりはるかに重篤な病態を示し、死亡率も高くなりました。化学物質や放射線による単独の腸障害ではこの追加のダメージは見られず、ナチュラルキラー細胞にも依存しませんでした。これは、MHC I欠損組織が一般的に脆弱であるというより、CD4 T細胞による攻撃に対して特異的に弱いことを示しています。
隠れるがんが逆に狙いやすくなる
研究者らは次に皮膚がんで一般的なメラノーマに目を向けました。彼らは遺伝子編集でマウスのメラノーマ細胞からMHC Iを除去しました。培養皿内では、これらのMHC I欠損腫瘍細胞はメラノーマ抗原を認識するCD4 T細胞によりより効率的に殺されました。マウスでは、MHC Iを欠く腫瘍はこれらのCD4 T細胞移入後に通常のMHC Iを持つ腫瘍よりも大きく縮小しました。これらの結果は、がんがCD8 T細胞を回避するためにMHC Iを失うと、適切な治療条件下ではCD4 T細胞が駆動する別種の免疫攻撃に対して不意に脆弱になる可能性を示唆します。
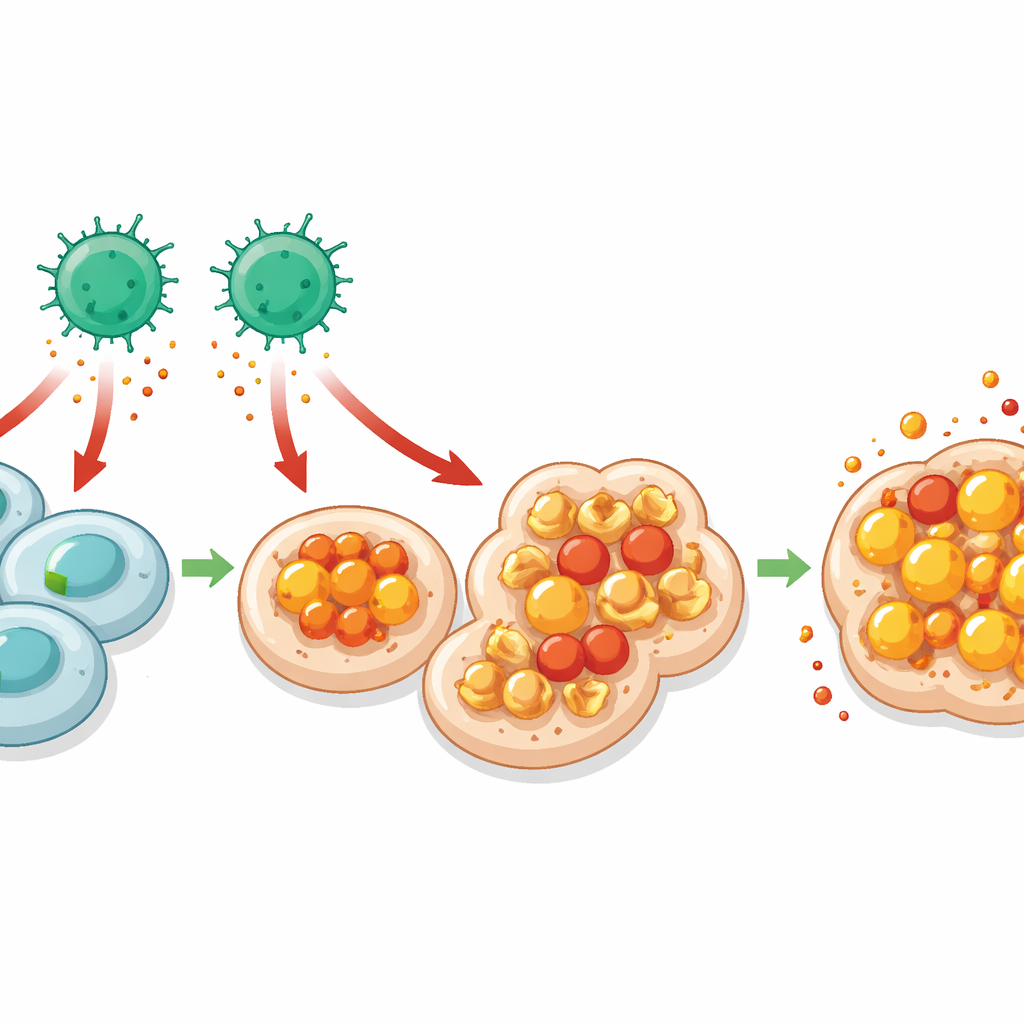
鉄、酸化した脂質、そして燃え上がる細胞死
さらに詳細を調べると、なぜMHC I欠損細胞がCD4 T細胞にとって殺しやすいのかが明らかになりました。腸細胞の単一細胞RNAシーケンシングは、MHC Iを欠く細胞でインターフェロン‑γに対する応答の兆候がより強いことを示しました。インターフェロン‑γはT細胞がしばしば放出する強力な警報シグナルです。同じ細胞群は鉄代謝の乱れや脂質過酸化の増加、すなわち細胞膜脂質の化学的損傷の指標も示していました。これらの特徴は、脂質酸化の暴走を特徴とする鉄依存性の細胞死「フェロトーシス」を示唆します。著者らは、MHC Iを欠く腸および腫瘍細胞がより多くの脂質損傷を蓄積し、鉄をキレートしたりフェロトーシスを化学的に阻害したりすると保護されることを確認しました。インターフェロン‑γを中和するとこの損傷は軽減され、CD4 T細胞由来のシグナルが脆弱な標的細胞でのフェロトーシスに結びつくことが示されました。
免疫療法を受ける患者からの手がかり
この機序がヒトでも重要かを調べるために、研究者らは免疫チェックポイント阻害剤で治療を受けたメラノーマおよび結腸がん患者の大規模データセットを解析しました。複数の研究を通じて、MHC I発現の低い腫瘍はCD8 T細胞の増加ではなくむしろCD4 T細胞の増加を伴う傾向があり、メラノーマではMHC I低発現でCD4 T細胞が豊富な患者の生存が長いことが示されました。MHC I低発現腫瘍はまた、抗フェロトーシス防御の弱さやより強いインターフェロン‑γ応答の分子学的指標を示し、マウスで観察されたパターンと一致していました。これらの知見は、一部のヒト腫瘍ではMHC Iの低下が単に免疫攻撃を遮断するだけでなく、CD4 T細胞駆動のフェロトーシス様の殺傷へとバランスを傾ける可能性があることを示唆します。
将来の治療への意味
総じて、この研究は標的細胞上のMHC class IがCD8 T細胞の認識タグである以上の働きをし、正常組織や腫瘍をCD4 T細胞による鉄依存性の細胞死から保護する役割を果たしていることを明らかにしました。この保護が失われると、MHC IIを介して標的を認識するCD4 T細胞は激しい酸化的損傷とフェロトーシスを誘導し、移植関連の腸障害を悪化させる一方で特定のがんの制御を改善する可能性があります。患者にとって、この新たな理解はMHC Iを失った腫瘍を治療するために意図的にCD4 T細胞とフェロトーシスを活用する戦略の設計を導きうるとともに、骨髄移植中に脆弱な組織を保護するための鉄調節薬の利用を示唆します。
引用: Lauder, E., Gondal, M., Wu, MC. et al. MHC class I on target cells regulates CD4+ T cell-mediated immunity. Nat Immunol 27, 1000–1012 (2026). https://doi.org/10.1038/s41590-026-02480-z
キーワード: CD4 T細胞, MHC class I, フェロトーシス, がん免疫療法, 移植片対宿主病