Clear Sky Science · pt
Alquilação descarboxilativa de alcenos
Uma nova maneira de ajustar moléculas do dia a dia
Muitos dos produtos de que dependemos — desde plásticos e sabões até medicamentos e defensivos agrícolas — são construídos a partir de unidades químicas simples chamadas alcenos. Químicos gostariam de uma forma fácil de "encaixar" novos fragmentos de carbono nessas unidades em etapas finais do processo de fabricação, permitindo ajustar com precisão um fármaco ou material sem reconstruí‑lo do zero. Este artigo apresenta um método novo e de ampla aplicação para ligar blocos alquil aos mais diversos alcenos, abrindo atalhos para moléculas que antes eram lentas, difíceis ou impossíveis de obter.
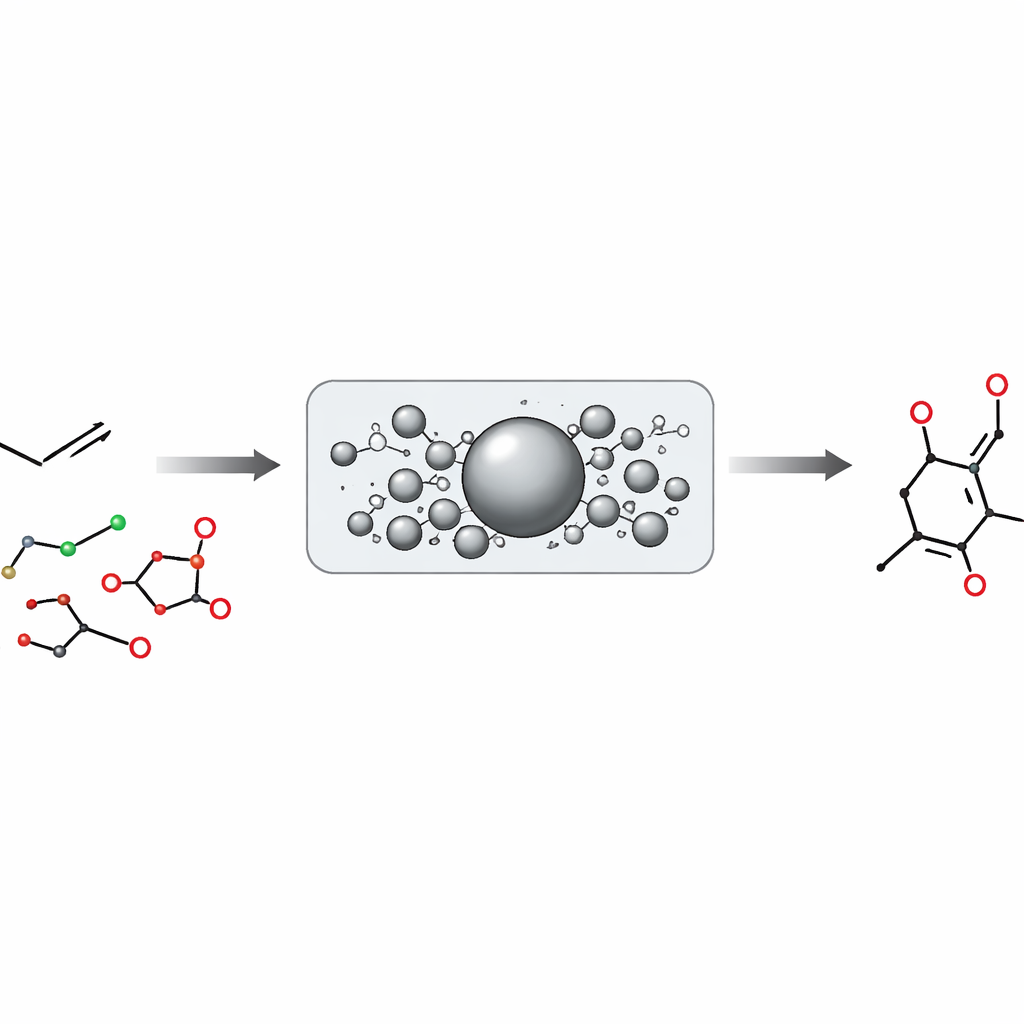
Por que modificar alcenos tem sido tão difícil
Alcenos são ligações dupla carbono–carbono que se comportam como pequenos ímãs para outros grupos químicos. Quando encontram parceiros reativos, costumam adicionar novos átomos através da dupla ligação, alterando completamente sua natureza em vez de simplesmente trocar um pedaço por outro. Em contraste, anéis aromáticos em corantes e fármacos podem sofrer facilmente substituição, onde um hidrogênio é trocado por um novo grupo. Como os alcenos não têm uma reação equivalente e geral de "troca", os químicos frequentemente precisam recorrer a rotas mais longas e em várias etapas que só formam a dupla ligação depois que o resto da molécula já está montado.
Transformando ingredientes simples em conectores versáteis
Os autores enfrentam esse problema combinando dois ingredientes extremamente comuns: alcenos e ácidos carboxílicos. Ácidos carboxílicos são abundantes, estáveis e estruturalmente diversos; aparecem em produtos naturais, medicamentos e químicos a granel. A equipe converte esses ácidos em "ésteres redox‑ativos" especiais, que podem perder dióxido de carbono e revelar um fragmento de carbono oculto pronto para ser ligado em outro lugar. Ao mesmo tempo, eles transformam alcenos ordinários em parceiros "eletrofílicos" usando um reagente à base de tiantreno, permitindo que esses alcenos se comportem como se um de seus hidrogênios da dupla ligação fosse uma alça para substituição em vez de uma simples adição.
De radicais fugazes a parceiros metálicos domesticados
Tentativas anteriores de combinar esses dois tipos de componentes dependeram principalmente de espécies radicais altamente reativas — fragmentos de curta vida que são difíceis de controlar e tendem a gerar subprodutos em vez de ligações limpas e seletivas. A inovação chave aqui é desviar o processo do acoplamento radical direto e, em vez disso, criar um parceiro organometálico mais controlado: um composto alquil‑zinco. Ao escolher cuidadosamente o solvente e usar zinco metálico, os autores mostram que os ésteres redox‑ativos podem ser convertidos em intermediários alquil‑zinco relativamente persistentes. Essas espécies sobrevivem tempo suficiente para serem conduzidas, sob catálise de paládio, a uma união precisa com o alceno ativado, forjando uma nova ligação entre um carbono da dupla ligação e um carbono do ácido.
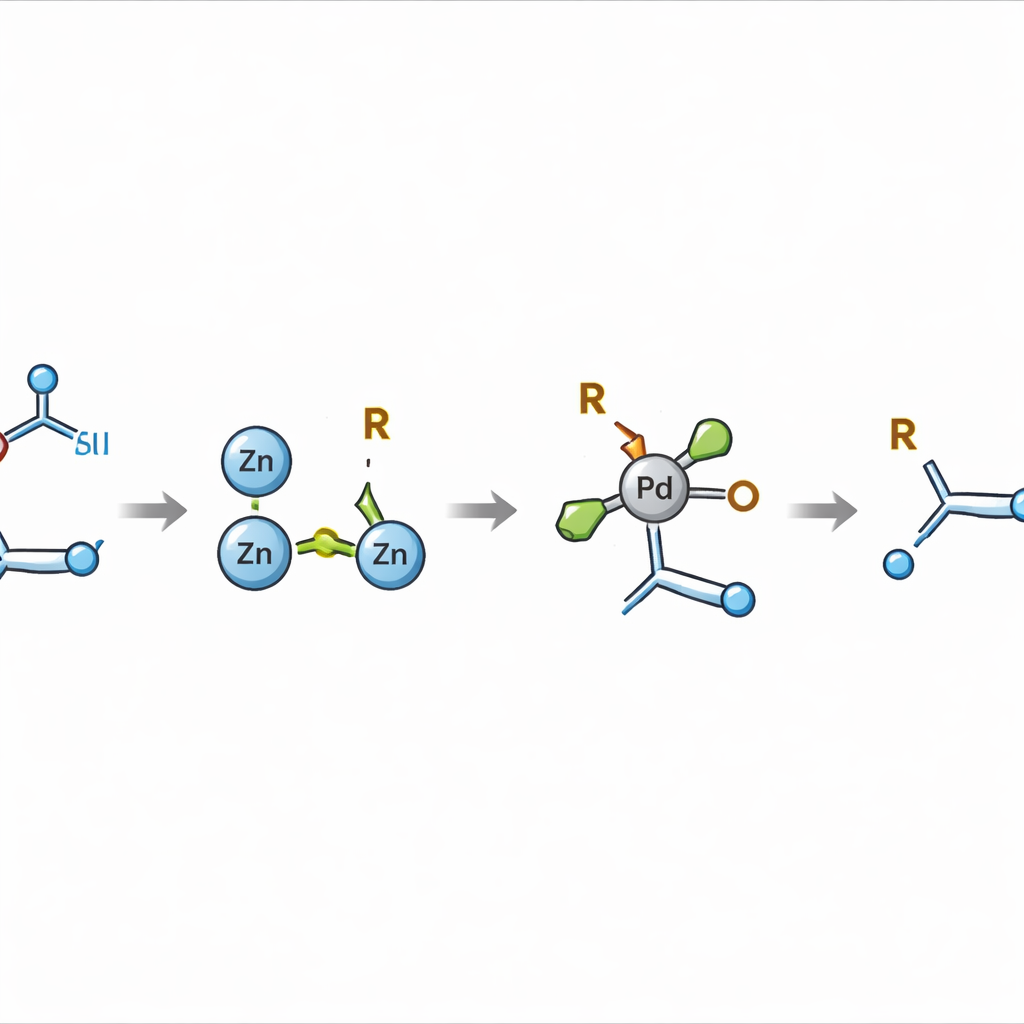
Alcançando alvos moleculares difíceis
Porque ambos os passos — a conversão do alceno em um sal tiantrênio e o acoplamento com o parceiro alquil‑zinco — são altamente seletivos, o método funciona em muitas estruturas desafiadoras. Pode modificar alcenos de matérias‑primas simples, duplas ligações internas e cíclicas, e até alcenos tri‑substituídos que são notoriamente difíceis de alterar. Grupos sensíveis, como aldeídos, cetonas e alcinos terminais, podem permanecer intactos, tornando a abordagem adequada para diversificação em estágio tardio de moléculas complexas, incluindo terpenos e compostos com perfil farmacológico. A reação também aceita uma ampla gama de fragmentos alquil primários e secundários, incluindo anéis tensionados e heterociclos, ampliando muito o cardápio de formas que os químicos podem encaixar em um dado alceno.
Uma nova lógica para construir esqueletos de carbono
Além da conveniência sintética imediata, este trabalho introduz um princípio de design inédito para formar ligações carbono–carbono. Em vez de planejar rotas em torno de radicais instáveis, os químicos podem pensar em termos de um caminho "polar" que transforma ácidos carboxílicos em parceiros ligados a metal estáveis, e então os acopla com alcenos especificamente ativados. Essa estratégia baseada em polaridade fornece uma nova maneira de desconectar moléculas‑alvo no papel e depois montá‑las no laboratório. Para não especialistas, a conclusão é que o estudo oferece uma ferramenta poderosa para anexar fragmentos de carbono a um dos motivos mais comuns na química orgânica, abreviando o caminho para descoberta e otimização mais rápidas de materiais, agroquímicos e medicamentos.
Citação: Roy, T.K., Tamborini, F.M., Petzold, R. et al. Decarboxylative alkylation of alkenes. Nature 653, 104–109 (2026). https://doi.org/10.1038/s41586-026-10463-1
Palavras-chave: funcionalização de alcenos, acoplamento descarboxilativo, catálise por paládio, química organometálica, ácidos carboxílicos