Clear Sky Science · de
Decarboxylative Alkylierung von Alkenen
Ein neuer Weg, alltägliche Moleküle zu verändern
Viele der Produkte, auf die wir angewiesen sind – von Kunststoffen und Seifen bis zu Arzneimitteln und Pflanzenschutzmitteln – werden aus einfachen Bausteinen hergestellt, den Alkenen. Chemiker wünschen sich eine einfache Möglichkeit, spät in der Herstellungskette neue Kohlenstoff‑Fragmente an diese Bausteine »anzustecken«, um ein Medikament oder Material zu verfeinern, ohne es von Grund auf neu aufzubauen. Diese Arbeit stellt eine neue, breit einsetzbare Methode vor, mit der Alkyl‑Bausteine an ein weites Spektrum von Alkenen gekoppelt werden können und so Abkürzungen zu Molekülen eröffnet werden, die zuvor langsam, schwierig oder unmöglich herzustellen waren.
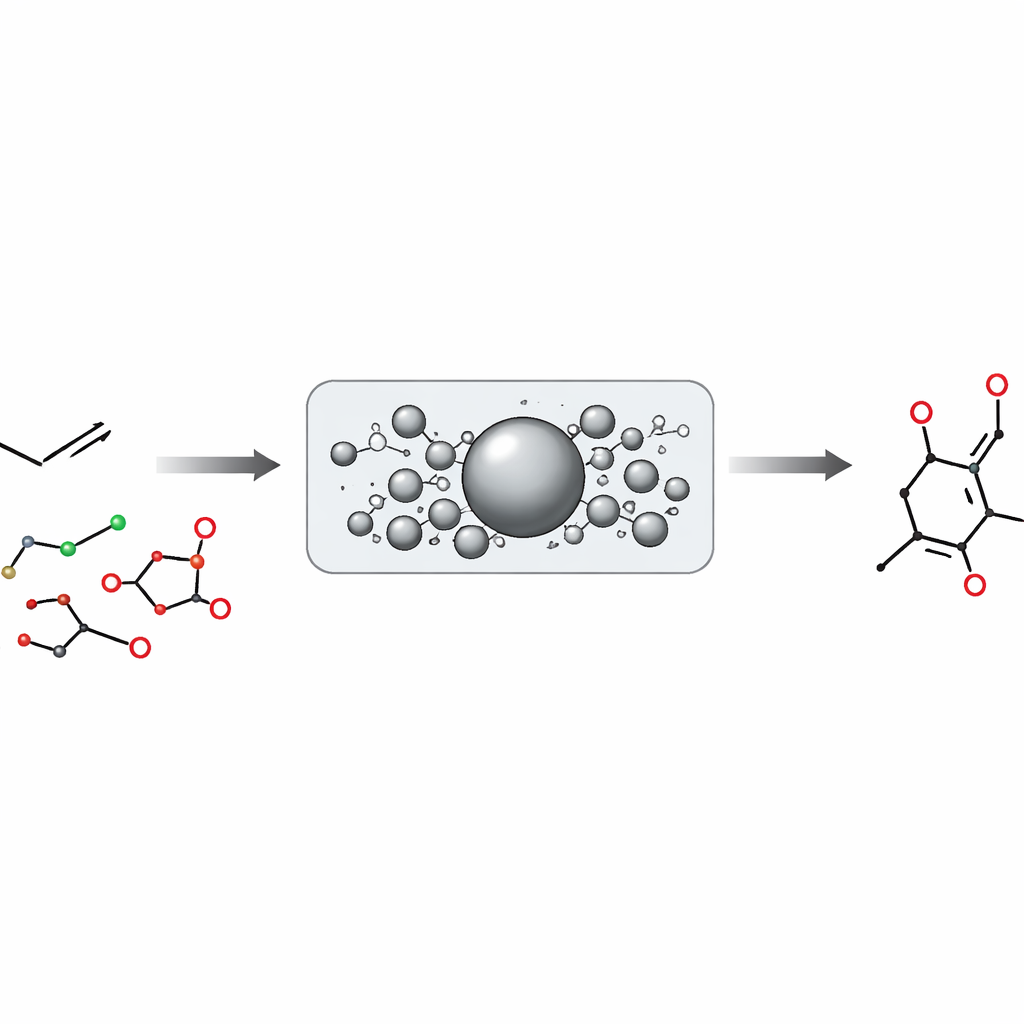
Warum das Ändern von Alkenen so schwer war
Alkene sind Kohlenstoff–Kohlenstoff‑Doppelbindungen, die wie kleine Anziehungspunkte für andere Gruppen wirken. Treffen sie auf reaktive Partner, addieren sich meist neue Atome über die Doppelbindung und verändern dadurch deren Natur vollständig, anstatt einfach ein Fragment gegen ein anderes auszutauschen. Im Gegensatz dazu können aromatische Ringe in Farbstoffen und Arzneistoffen leicht Substitutionsreaktionen durchlaufen, bei denen ein Wasserstoff durch eine neue Gruppe ersetzt wird. Da Alkene kein gleichwertiges, allgemeines »Einstück‑Austausch«‑Verfahren besitzen, greifen Chemiker häufig zu längeren, mehrstufigen Routen, bei denen die Doppelbindung erst nach dem Aufbau des übrigen Moleküls eingeführt wird.
Einfache Zutaten in vielseitige Verbindungsstücke verwandeln
Die Autoren gehen das Problem, indem sie zwei äußerst verbreitete Ausgangsstoffe kombinieren: Alkene und Carbonsäuren. Carbonsäuren sind reichlich vorhanden, stabil und strukturell vielfältig; sie kommen in Naturstoffen, Arzneimitteln und Basischemikalien vor. Das Team wandelt diese Säuren in spezielle „redox‑aktive Ester“ um, die Kohlendioxid abspalten können und ein verborgenes Kohlenstofffragment frelegen, das bereit ist, anderswo angefügt zu werden. Gleichzeitig machen sie gewöhnliche Alkene mit einem auf Thianthren basierenden Reagenz zu electrophilen Partnern, sodass diese Alkene so reagieren, als sei eines ihrer Doppelbindungs‑Wasserstoffe ein Griff für Substitution statt für einfache Addition.
Von flüchtigen Radikalen zu gezähmten Metall‑Partnern
Frühere Versuche, diese beiden Komponententypen zu kombinieren, stützten sich meist auf hochreaktive Radikalarten – kurzlebige Fragmente, die schwer zu kontrollieren sind und eher Nebenprodukte als saubere, selektive Bindungen liefern. Die wesentliche Neuerung hier besteht darin, den Prozess von direkter Radikalkupplung wegzulenken und stattdessen einen besser kontrollierten organometallischen Partner zu erzeugen: ein Alkyl‑Zink‑Kompound. Durch sorgsame Wahl des Lösungsmittels und den Einsatz von Zinkmetall zeigen die Autoren, dass sich die redox‑aktiven Ester in relativ beständige Alkyl‑Zink‑Zwischenstufen überführen lassen. Diese Spezies überdauern lange genug, um unter Palladiumkatalyse in eine präzise Vereinigung mit dem aktivierten Alken gelenkt zu werden und so eine neue Bindung zwischen einem Kohlenstoff der Doppelbindung und einem Kohlenstoff aus der Säure zu schmieden.
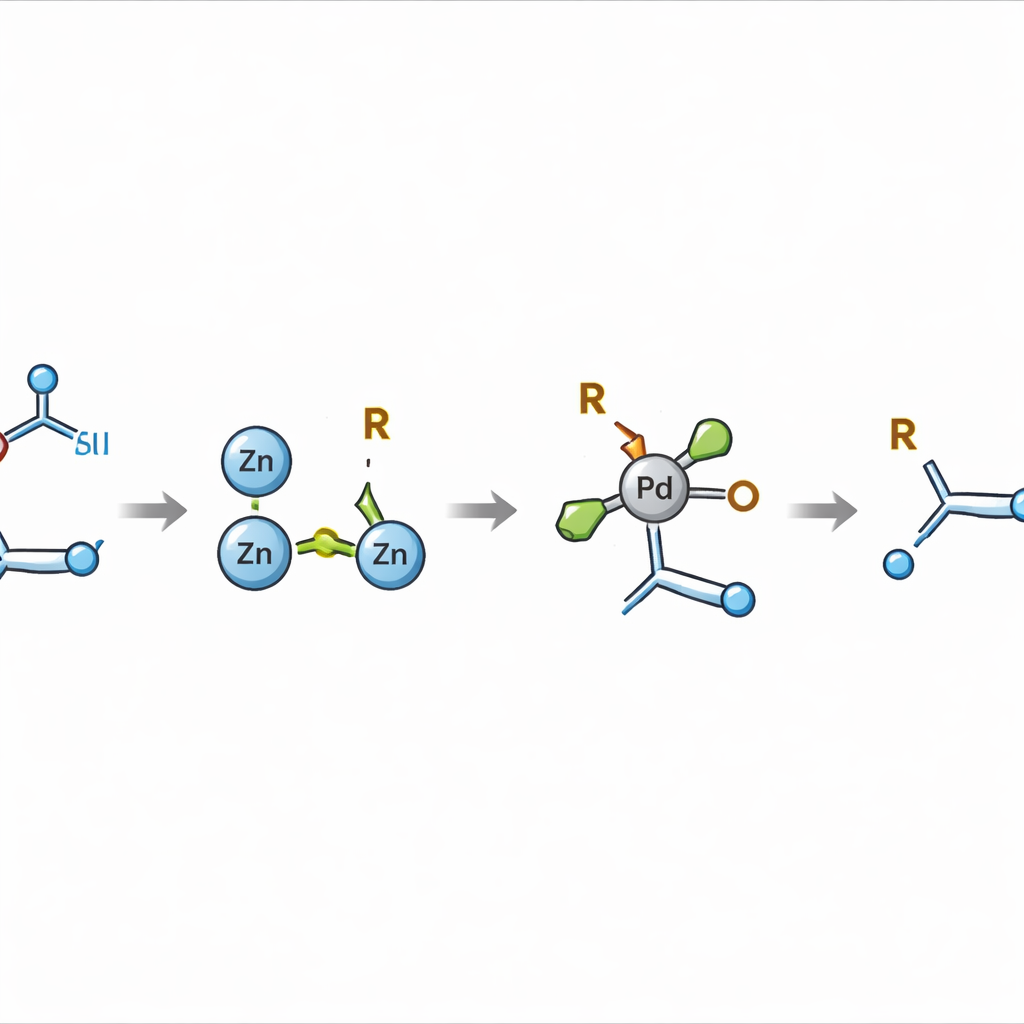
Schwierige molekulare Ziele erreichen
Weil beide Schritte – die Umwandlung des Alkens in ein Thianthreniumsalz und die Kupplung mit dem Alkyl‑Zink‑Partner – hochselektiv sind, funktioniert die Methode an vielen anspruchsvollen Strukturen. Sie kann einfache Rohstoff‑Alkene, interne und cyclische Doppelbindungen und sogar tri‑substituierte Alkene modifizieren, die bekanntlich schwer zu verändern sind. Empfindliche Gruppen wie Aldehyde, Ketone und terminale Alkine bleiben unberührt, wodurch der Ansatz für die späte Diversifizierung komplexer Moleküle geeignet ist, einschließlich Terpenen und arzneimittelähnlichen Verbindungen. Die Reaktion akzeptiert zudem eine breite Palette primärer und sekundärer Alkylfragmente, einschließlich gespannten Ringen und Heterocyclen, und erweitert damit deutlich die Auswahl an Formen, die Chemiker an ein gegebenes Alken anfügen können.
Eine neue Logik zum Aufbau von Kohlenstoffgerüsten
Über die unmittelbare synthetische Erleichterung hinaus führt diese Arbeit ein neues Gestaltungsprinzip für das Schmieden von Kohlenstoff–Kohlenstoff‑Bindungen ein. Anstatt Routen um instabile Radikale herumzuplanen, können Chemiker in Zukunft an einen »polaren« Weg denken, der Carbonsäuren in stabile, metallgebundene Partner verwandelt und diese dann mit speziell aktivierten Alkenen koppelt. Diese auf Polarität basierende Strategie bietet eine neue Perspektive, Zielmoleküle auf dem Papier zu zerlegen und anschließend im Labor zusammenzusetzen. Für Nicht‑Spezialisten lautet die Quintessenz: Die Studie liefert ein mächtiges neues Werkzeug, um Kohlenstofffragmente an eines der häufigsten Motive der organischen Chemie anzubringen und ebnet damit den Weg für schnellere Entdeckung und Optimierung von Materialien, Agrochemikalien und Arzneistoffen.
Zitation: Roy, T.K., Tamborini, F.M., Petzold, R. et al. Decarboxylative alkylation of alkenes. Nature 653, 104–109 (2026). https://doi.org/10.1038/s41586-026-10463-1
Schlüsselwörter: Alken‑Funktionalisierung, decarboxylative Kupplung, Palladiumkatalyse, organometallische Chemie, Säuren (Carboxylsäuren)