Clear Sky Science · it
Alchilazione decarbossilativa degli alcheni
Un nuovo modo per modificare molecole di uso quotidiano
Molti dei prodotti di cui ci serviamo — dalla plastica e i detergenti ai farmaci e ai fitofarmaci — sono costruiti a partire da unità chimiche semplici chiamate alcheni. I chimici desidererebbero un modo semplice per "innestare" nuovi pezzi di carbonio su queste unità nelle fasi finali del processo produttivo, così da poter perfezionare un farmaco o un materiale senza ricostruirlo da zero. Questo articolo presenta un metodo nuovo e ampiamente utile per collegare blocchi alchilici a una vasta gamma di alcheni, aprendo scorciatoie verso molecole che prima erano lente, ardue o impossibili da ottenere.
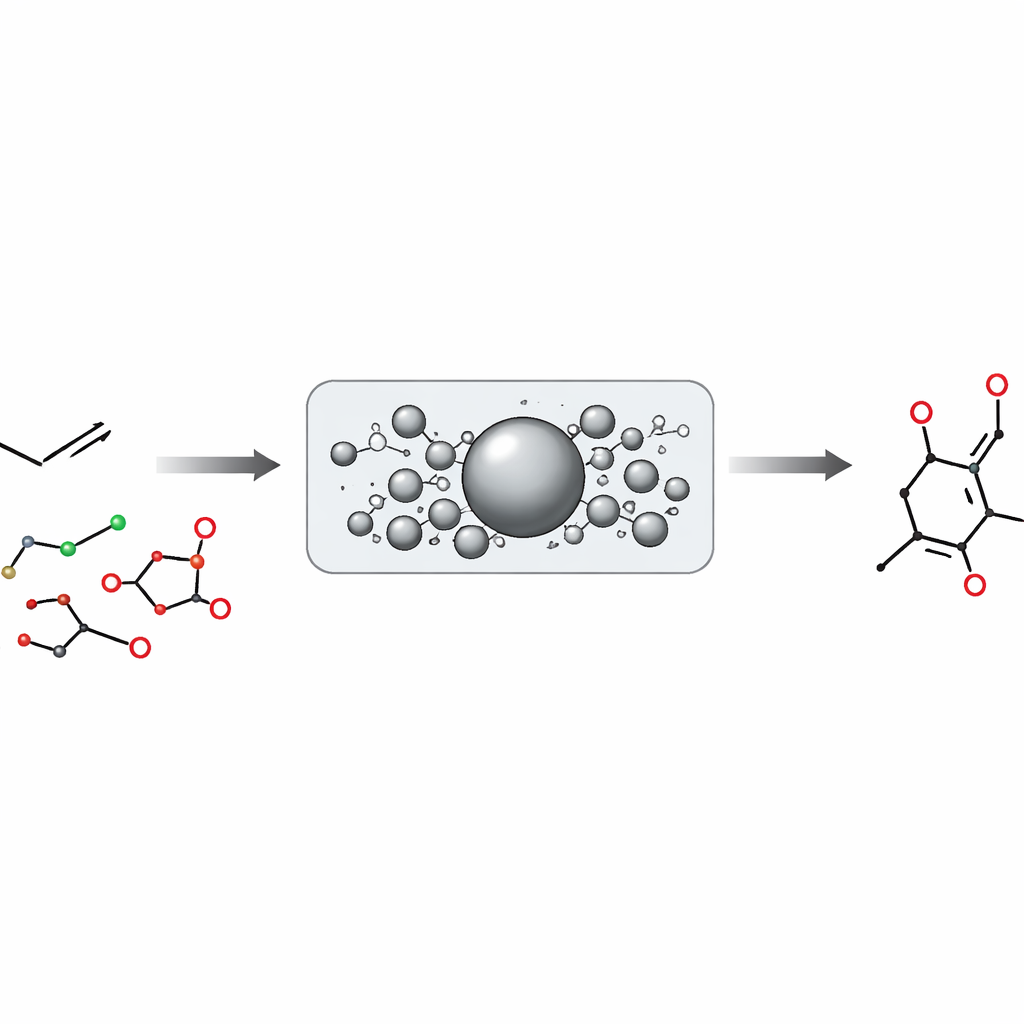
Perché cambiare gli alcheni è stato così difficile
Gli alcheni sono doppi legami carbonio–carbonio che si comportano come piccoli calamita per altri gruppi chimici. Quando incontrano partner reattivi, di solito aggiungono nuovi atomi attraverso il doppio legame, cambiandone completamente la natura invece di limitarsi a sostituire un pezzo con un altro. Al contrario, gli anelli aromatici nei coloranti e nei farmaci possono subire agevolmente sostituzioni, in cui un idrogeno è rimpiazzato da un nuovo gruppo. Poiché gli alcheni non possiedono una reazione generale equivalente di "sostituzione", i chimici devono spesso ricorrere a percorsi più lunghi e in più fasi che costruiscono il doppio legame solo dopo che il resto della molecola è stato assemblato.
Trasformare ingredienti semplici in connettori versatili
Gli autori affrontano questo problema abbinando due ingredienti estremamente comuni: alcheni e acidi carbossilici. Gli acidi carbossilici sono abbondanti, stabili e strutturalmente diversi; si trovano nei prodotti naturali, nei farmaci e nei prodotti chimici di massa. Il gruppo converte questi acidi in speciali "esteri redox‑attivi", che possono perdere anidride carbonica e rivelare un frammento carbonioso nascosto pronto per essere attaccato altrove. Allo stesso tempo, trasformano alcheni ordinari in partner "elettrofili" usando un reagente a base di tiantrene, permettendo a quegli alcheni di comportarsi come se uno degli idrogeni del doppio legame fosse una maniglia per la sostituzione anziché per una semplice addizione.
Da radicali fugaci a partner metallici miti
I precedenti tentativi di combinare questi due tipi di componenti si basavano per lo più su specie radicaliche altamente reattive — frammenti di breve durata difficili da guidare e inclini a produrre prodotti laterali anziché legami puliti e selettivi. L'innovazione chiave qui è deviare il processo dall'accoppiamento radicalico diretto e invece creare un partner organometallico più controllato: un composto alchil‑zinco. Scegliendo con cura il solvente e usando il metallo zinco, gli autori dimostrano che gli esteri redox‑attivi possono essere convertiti in intermedi alchil‑zinco relativamente persistenti. Queste specie sopravvivono abbastanza a lungo da essere convogliate, sotto catalisi al palladio, in un'unione precisa con l'alchene attivato, formando un nuovo legame tra un atomo di carbonio del doppio legame e un carbonio proveniente dall'acido.
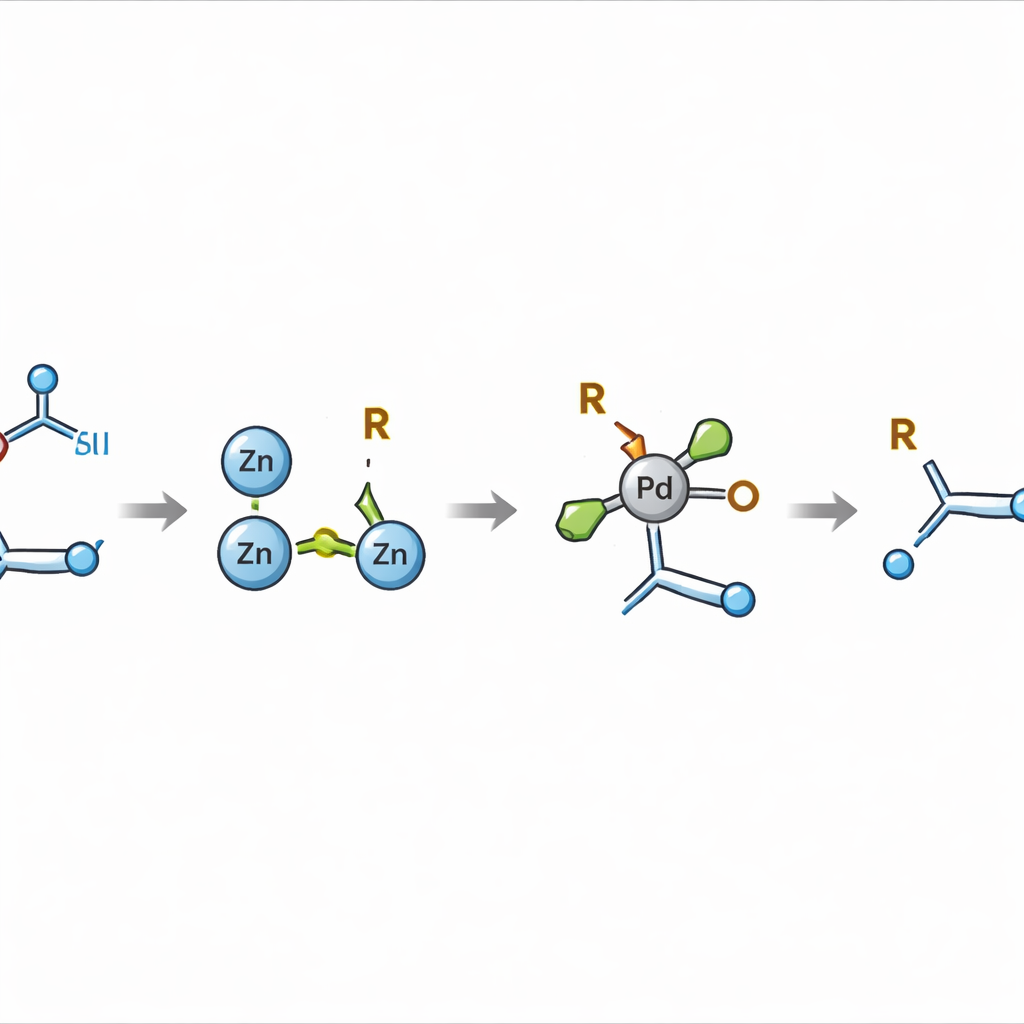
Raggiungere bersagli molecolari difficili
Poiché entrambi i passaggi — la conversione dell'alchene in un sale di tiantrenio e l'accoppiamento con il partner alchil‑zinco — sono altamente selettivi, il metodo funziona su molte strutture sfidanti. Può modificare alcheni di materia prima semplice, doppi legami interni e ciclici e persino alcheni tri‑sostituiti che sono notoriamente difficili da alterare. Gruppi sensibili come aldeidi, chetoni e alchini terminali possono rimanere intatti, rendendo l'approccio adatto alla diversificazione in stadio avanzato di molecole complesse, inclusi terpeni e composti di tipo farmaceutico. La reazione accetta anche un'ampia gamma di frammenti alchilici primari e secondari, inclusi anelli sotto tensione ed eterocicli, ampliando notevolmente il ventaglio di forme che i chimici possono innestare su un dato alchene.
Una nuova logica per costruire scheletri carboniosi
Oltre alla pratica comodità sintetica immediata, questo lavoro introduce un nuovo principio progettuale per formare legami carbonio–carbonio. Invece di pianificare percorsi attorno a radicali instabili, i chimici possono pensare in termini di una via "polare" che trasforma gli acidi carbossilici in partner stabili legati a un metallo, per poi accoppiarli con alcheni specialmente attivati. Questa strategia basata sulla polarità offre un nuovo modo di disconnettere le molecole target sulla carta e poi assemblarle in laboratorio. Per i non specialisti, la conclusione è che lo studio fornisce un potente nuovo strumento per attaccare frammenti carboniosi a uno dei motivi più comuni nella chimica organica, aprendo la strada a scoperte e ottimizzazioni più rapide di materiali, agrochimici e farmaci.
Citazione: Roy, T.K., Tamborini, F.M., Petzold, R. et al. Decarboxylative alkylation of alkenes. Nature 653, 104–109 (2026). https://doi.org/10.1038/s41586-026-10463-1
Parole chiave: funzionalizzazione degli alcheni, accoppiamento decarbossilativo, catalisi al palladio, chimica organometallica, acidi carbossilici