Clear Sky Science · fr
Alkylation décarboxylative des alcènes
Une nouvelle façon d'ajuster des molécules du quotidien
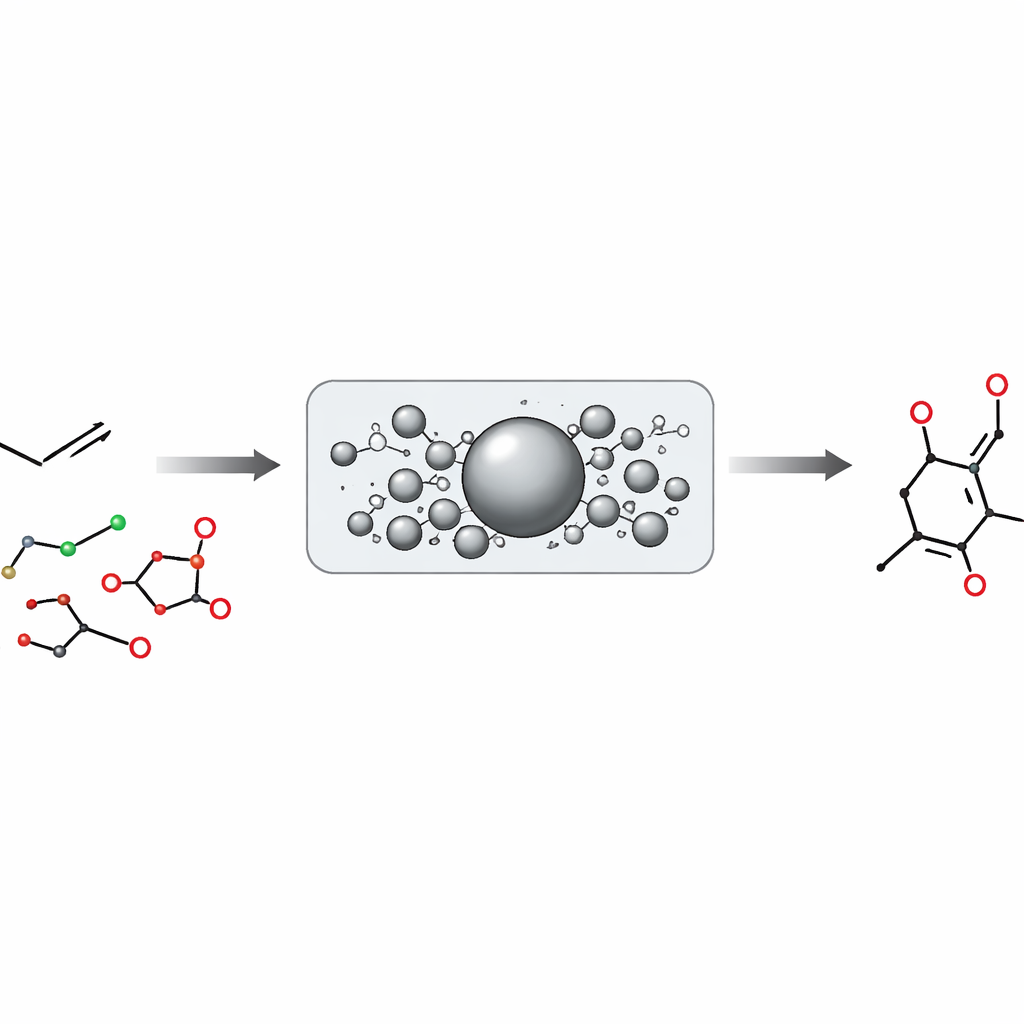
Beaucoup des produits sur lesquels nous comptons — des plastiques et savons aux médicaments et insecticides — sont construits à partir d'unités chimiques simples appelées alcènes. Les chimistes aimeraient disposer d'un moyen facile d'« emboîter » de nouveaux fragments carbonés sur ces unités en fin de procédé, pour affiner un médicament ou un matériau sans tout reconstruire depuis le début. Cet article présente une méthode nouvelle et largement applicable pour fixer des blocs alkyles sur une grande variété d'alcènes, ouvrant des raccourcis vers des molécules auparavant lentes, délicates ou impossibles à obtenir.
Pourquoi il a été si difficile de modifier les alcènes
Les alcènes sont des liaisons carbone–carbone doubles qui se comportent comme de petits aimants pour d'autres groupes chimiques. Lorsqu'ils rencontrent des partenaires réactifs, ils ont tendance à ajouter de nouveaux atomes de part et d'autre de la double liaison, changeant complètement sa nature plutôt que de simplement remplacer une pièce par une autre. En revanche, les cycles aromatiques présents dans les colorants et les produits pharmaceutiques peuvent subir facilement des substitutions où un hydrogène est remplacé par un nouveau groupe. Parce que les alcènes manquent d'une réaction générale équivalente de « remplacement », les chimistes doivent souvent recourir à des voies plus longues en plusieurs étapes qui construisent la double liaison seulement après avoir assemblé le reste de la molécule.
Transformer des ingrédients simples en connecteurs polyvalents
Les auteurs s'attaquent à ce problème en associant deux ingrédients extrêmement courants : les alcènes et les acides carboxyliques. Les acides carboxyliques sont abondants, stables et structurellement divers ; on les trouve dans des produits naturels, des médicaments et des produits de base. L'équipe convertit ces acides en « esters redox‑actifs » spéciaux, qui peuvent perdre du dioxyde de carbone et révéler un fragment carboné caché prêt à être transféré ailleurs. Parallèlement, ils transforment des alcènes ordinaires en partenaires « électrophiles » à l'aide d'un réactif à base de thianthrène, permettant à ces alcènes de se comporter comme si l'un de leurs hydrogènes de la double liaison constituait une poignée pour une substitution plutôt qu'une addition simple.
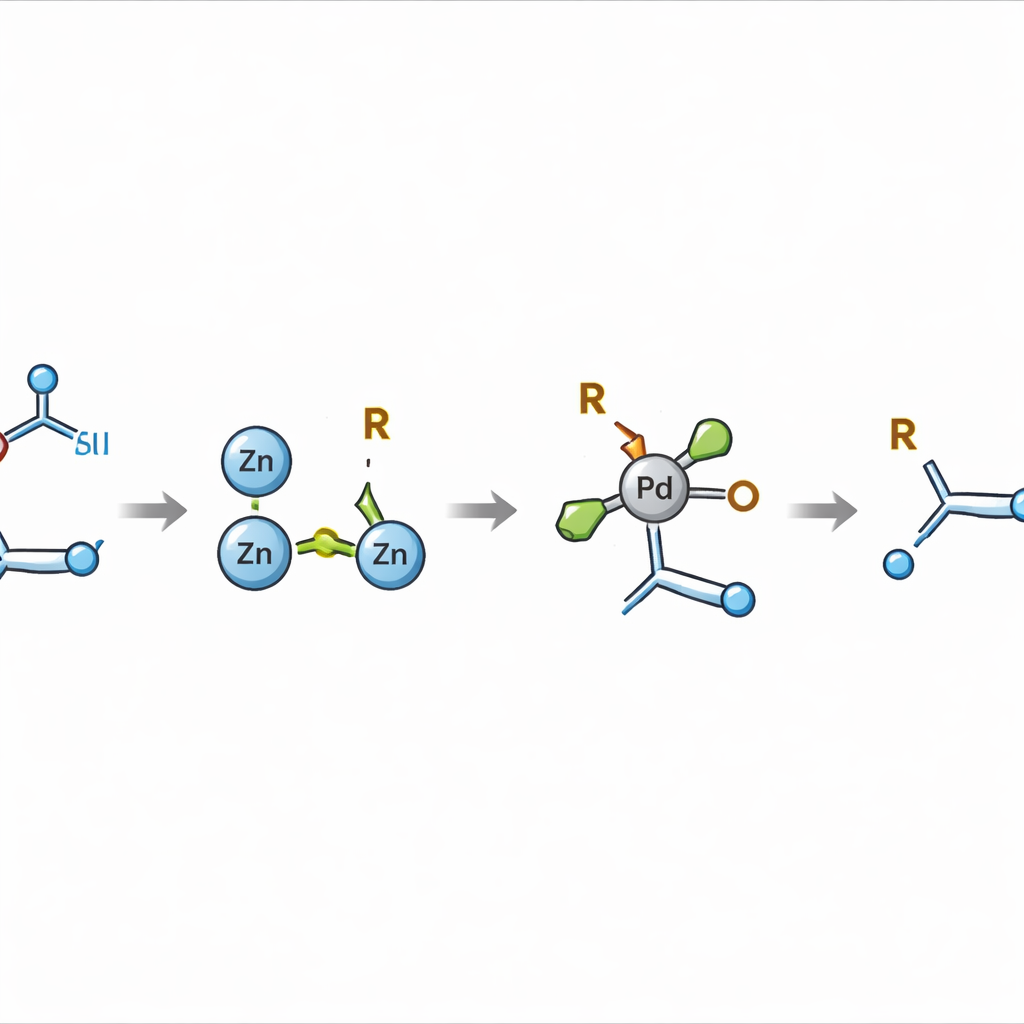
Des radicaux fugitifs à des partenaires métalliques dociles
Les tentatives antérieures pour combiner ces deux types de composants reposaient principalement sur des espèces radicalaires très réactives — des fragments de courte durée difficiles à contrôler et susceptibles de former des produits secondaires plutôt que des liaisons propres et sélectives. L'innovation clé ici est d'écarter l'accouplement radicalaire direct pour créer à la place un partenaire organométallique plus contrôlé : un composé alkyle–zinc. En choisissant soigneusement le solvant et en utilisant du zinc métal, les auteurs montrent que les esters redox‑actifs peuvent être convertis en intermédiaires alkyle–zinc relativement persistants. Ces espèces survivent suffisamment longtemps pour être dirigées, sous catalyse palladium, vers une union précise avec l'alcène activé, forgeant une nouvelle liaison entre un carbone de la double liaison et un carbone provenant de l'acide.
Atteindre des cibles moléculaires difficiles
Parce que les deux étapes — la conversion de l'alcène en sel de thianthrenium et le couplage avec le partenaire alkyle–zinc — sont hautement sélectives, la méthode fonctionne sur de nombreuses structures exigeantes. Elle peut modifier des alcènes de base issus de matières premières, des liaisons doubles internes et cycliques, et même des alcènes tri‑substitués notoirement difficiles à altérer. Des groupes sensibles tels que les aldéhydes, les cétones et les alcynes terminaux peuvent rester intacts, ce qui rend l'approche adaptée à la diversification en fin d'étape de molécules complexes, y compris des terpènes et des composés de type médicament. La réaction accepte aussi une large gamme de fragments alkyles primaires et secondaires, y compris des cycles contraints et des hétérocycles, élargissant considérablement le choix de formes que les chimistes peuvent greffer sur un alcène donné.
Une nouvelle logique pour construire des charpentes carbonées
Au‑delà de la commodité synthétique immédiate, ce travail introduit un principe de conception inédit pour la formation de liaisons carbone–carbone. Plutôt que de planifier des voies autour de radicaux instables, les chimistes peuvent penser en termes d'une voie « polaire » qui transforme des acides carboxyliques en partenaires métalliques stables, puis les couple à des alcènes spécialement activés. Cette stratégie fondée sur la polarité offre une nouvelle manière de déconnecter des molécules cibles sur le papier, puis de les assembler en laboratoire. Pour les non‑spécialistes, l'essentiel est que l'étude fournit un nouvel outil puissant pour fixer des fragments carbonés sur l'un des motifs les plus courants en chimie organique, ouvrant la voie à une découverte et une optimisation plus rapides de matériaux, d'agrochimiques et de médicaments.
Citation: Roy, T.K., Tamborini, F.M., Petzold, R. et al. Decarboxylative alkylation of alkenes. Nature 653, 104–109 (2026). https://doi.org/10.1038/s41586-026-10463-1
Mots-clés: fonctionnalisation des alcènes, couplage décarboxylatif, catalyse au palladium, chimie organométallique, acides carboxyliques