Clear Sky Science · pl
Dekarboksylacyjna alkilacja alkenów
Nowy sposób modyfikowania codziennych cząsteczek
Wiele produktów, na których polegamy — od tworzyw sztucznych i mydeł po leki i środki ochrony roślin — powstaje z prostych jednostek chemicznych zwanych alkenami. Chemicy chętnie przyjęliby prostą metodę „wtykania” nowych fragmentów węglowych w te jednostki na późnym etapie procesu produkcyjnego, co pozwoliłoby dopracować lek lub materiał bez konieczności budowania go od zera. Artykuł przedstawia nową, szeroko użyteczną metodę szybkiego przyłączania fragmentów alkilowych do rozmaitych alkenów, otwierając skróty do cząsteczek, których wcześniej synteza była powolna, skomplikowana lub niemożliwa.
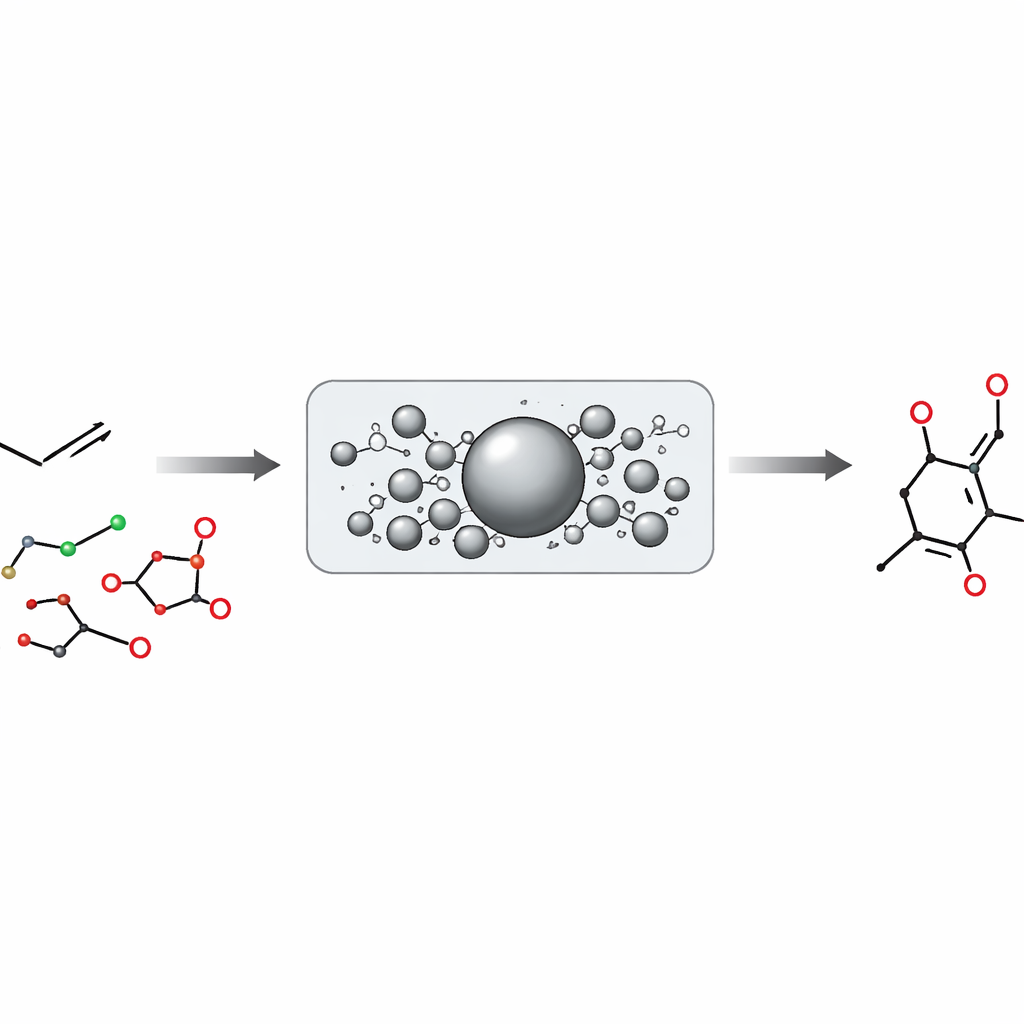
Dlaczego zmienianie alkenów było takie trudne
Alkeny to podwójne wiązania węgiel–węgiel, które działają jak małe magnesy dla innych grup chemicznych. Gdy spotykają reagenty reaktywne, zwykle dodają nowe atomy przez wiązanie się po obu stronach podwójnego wiązania, całkowicie zmieniając jego charakter, zamiast po prostu wymienić jeden fragment na inny. W przeciwieństwie do tego pierścienie aromatyczne w barwnikach i lekach łatwo przechodzą reakcje substytucji, w których jeden atom wodoru jest zastępowany nową grupą. Ponieważ alkeny nie mają równoważnej, ogólnej reakcji „wstawienia”, chemicy często muszą sięgać po dłuższe, wieloetapowe ścieżki, które tworzą podwójne wiązanie dopiero po zmontowaniu reszty cząsteczki.
Przekształcanie prostych składników w wszechstronne łączniki
Autorzy rozwiązują ten problem, łącząc dwa niezwykle powszechne składniki: alkeny i kwasy karboksylowe. Kwasy karboksylowe są dostępne, trwałe i różnorodne strukturalnie; występują w produktach naturalnych, lekach i chemikaliach przemysłowych. Zespół przekształca te kwasy w specjalne „estry redoksaktywne”, które mogą utracić dwutlenek węgla i odsłonić ukryty fragment węglowy gotowy do przyłączenia gdzie indziej. Jednocześnie przekształcają zwykłe alkeny w partnerów „elektrofilowych” za pomocą reagentu opartego na tiantrenium, co pozwala tym alkenom zachowywać się tak, jakby jeden z ich atomów wodoru przy podwójnym wiązaniu był uchwytem do substytucji zamiast prostej addycji.
Od przemijających rodników do poskromionych partnerów metalicznych
Wcześniejsze próby łączenia tych dwóch typów komponentów opierały się głównie na wysoce reaktywnych rodnikach — krótkotrwałych fragmentach, które trudno skierować i mają skłonność do tworzenia produktów ubocznych zamiast czystych, selektywnych wiązań. Kluczową innowacją jest tu skierowanie procesu z dala od bezpośredniego sprzęgania rodnikowego i zamiast tego wytworzenie bardziej kontrolowanego partnera organometalicznego: związku alkilowo‑cynkowego. Poprzez staranny wybór rozpuszczalnika i użycie metalu cynku autorzy pokazują, że estry redoksaktywne można przekształcić w stosunkowo trwałe intermediates alkilowo‑cynkowe. Gatunki te przetrwają wystarczająco długo, by poddane katalizie palladowej zostać sprowadzone do precyzyjnego połączenia z aktywowanym alkenem, tworząc nowe wiązanie między atomem węgla w podwójnym wiązaniu a atomem węgla pochodzącym z kwasu.
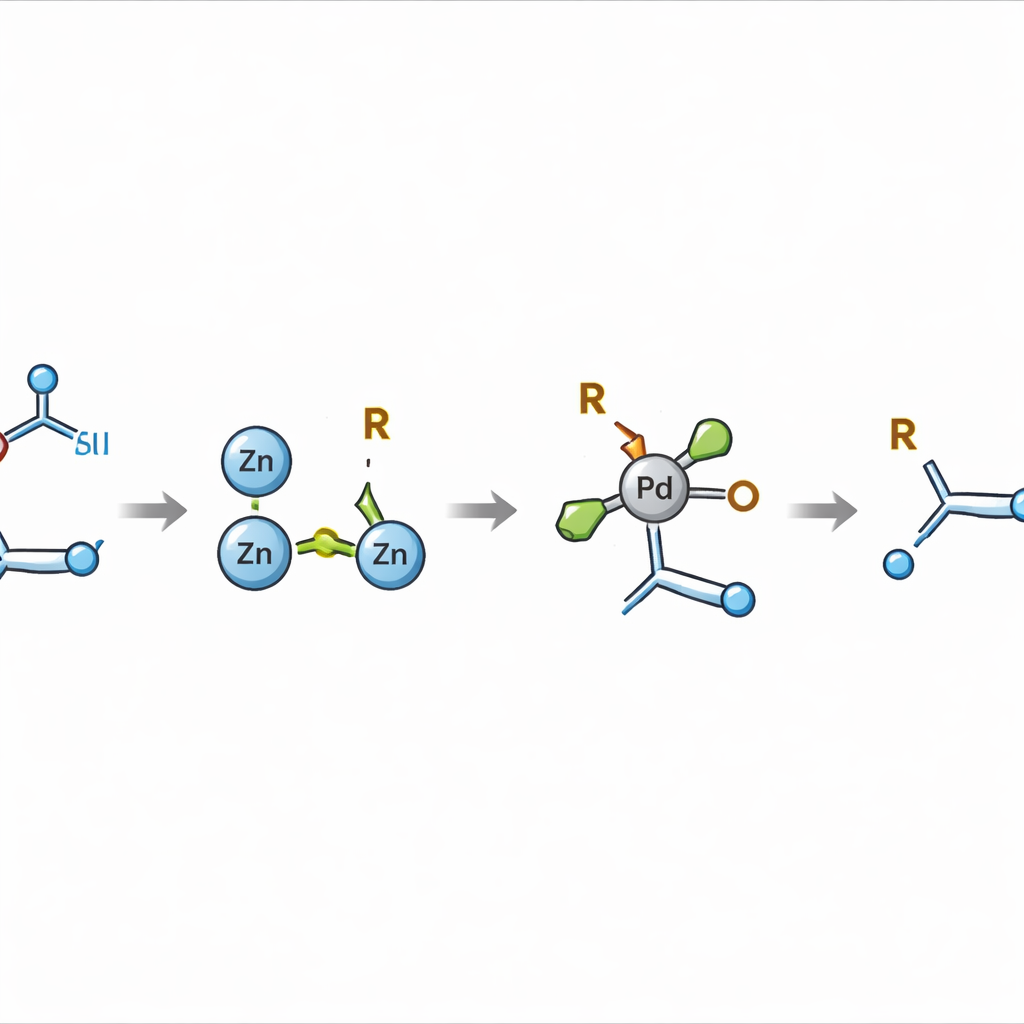
Sięgając po trudne cele molekularne
Ponieważ oba kroki — przekształcenie alkenu w sól tiantrenową i sprzęganie z partnerem alkilowo‑cynkowym — są wysoce selektywne, metoda działa na wielu wymagających strukturach. Może modyfikować proste alkeny wykorzystywane jako surowce, wiązania wewnętrzne i cykliczne, a nawet trójsubsytuowane alkeny, które są znane jako szczególnie trudne do zmiany. Wrażliwe grupy, takie jak aldehydy, ketony i terminalne alkiny, mogą pozostać nienaruszone, co czyni podejście odpowiednim do dywersyfikacji na późnym etapie złożonych cząsteczek, w tym terpenów i związków o charakterze lekowym. Reakcja akceptuje także szerokie spektrum fragmentów alkilowych pierwotnych i wtórnych, w tym pierścienie spięte i heterocykle, znacząco poszerzając gamę kształtów, które chemicy mogą wpinąć w dany alken.
Nowa logika budowania szkieletów węglowych
Ponad bezpośrednią wygodą syntetyczną, praca ta wprowadza odświeżającą zasadę projektowania wiązań węgiel–węgiel. Zamiast planować ścieżki wokół niestabilnych rodników, chemicy mogą myśleć w kategoriach „polarnej” drogi, która zamienia kwasy karboksylowe w stabilne, metalowo‑związane partner y, a następnie sprzęga je ze specjalnie aktywowanymi alkenami. Strategia oparta na polarności dostarcza nowego sposobu rozcinania docelowych cząsteczek na papierze, a następnie ich składania w laboratorium. Dla osób niebędących specjalistami najważniejszy wniosek jest taki, że badanie dostarcza potężne nowe narzędzie do przyłączania fragmentów węglowych do jednego z najpowszechniejszych motywów w chemii organicznej, torując drogę do szybszego odkrywania i optymalizacji materiałów, agrochemikaliów i leków.
Cytowanie: Roy, T.K., Tamborini, F.M., Petzold, R. et al. Decarboxylative alkylation of alkenes. Nature 653, 104–109 (2026). https://doi.org/10.1038/s41586-026-10463-1
Słowa kluczowe: functionalizacja alkenów, sprzęganie dekarboksylacyjne, kataliza palladowa, chemia organometaliczna, kwasy karboksylowe