Clear Sky Science · pt
Base estrutural da hidratação vetorial de CO₂ acoplada ao potencial de membrana pelo complexo DAB2 em quimiolitotrófos
Como micróbios ajudam a aprisionar carbono
Escondidos nos oceanos e em sedimentos ricos em enxofre há micróbios que vivem inteiramente de substâncias inorgânicas e dióxido de carbono. Este estudo revela como um desses grupos de bactérias usa uma minúscula máquina molecular, chamada complexo DAB2, para extrair CO₂ do ambiente e convertê-lo em uma forma que a célula pode utilizar. Entender essa bomba natural de carbono é importante para a ciência climática básica e pode, no futuro, inspirar novas maneiras de captar CO₂ do ambiente.
Uma bomba de carbono microscópica
Muitos microrganismos constroem seus corpos a partir de carbono inorgânico dissolvido, uma mistura de CO₂ e moléculas relacionadas na água. Eles dependem de uma enzima lenta, a RuBisCO, para incorporar CO₂ a compostos orgânicos — uma reação central no ciclo global do carbono. Como a RuBisCO é lenta e facilmente perturbada, muitos micróbios evoluíram mecanismos de concentração de CO₂ que estocam carbono utilizável bem onde a RuBisCO atua. Embora esses sistemas sejam bem conhecidos em cianobactérias fotossintéticas, os quimiolitotrófos — bactérias que obtêm energia oxidando substâncias inorgânicas como enxofre — permanecem menos compreendidos. Trabalhos anteriores apontaram para uma família de complexos de membrana, coletivamente chamados de DACs, que ajudam essas bactérias a crescer quando o carbono escasseia. Um desses sistemas, o DAB2 da bactéria Halothiobacillus neapolitanus, pode resgatar E. coli privadas de carbono, sugerindo que ele acumula ativamente carbono inorgânico dentro das células.
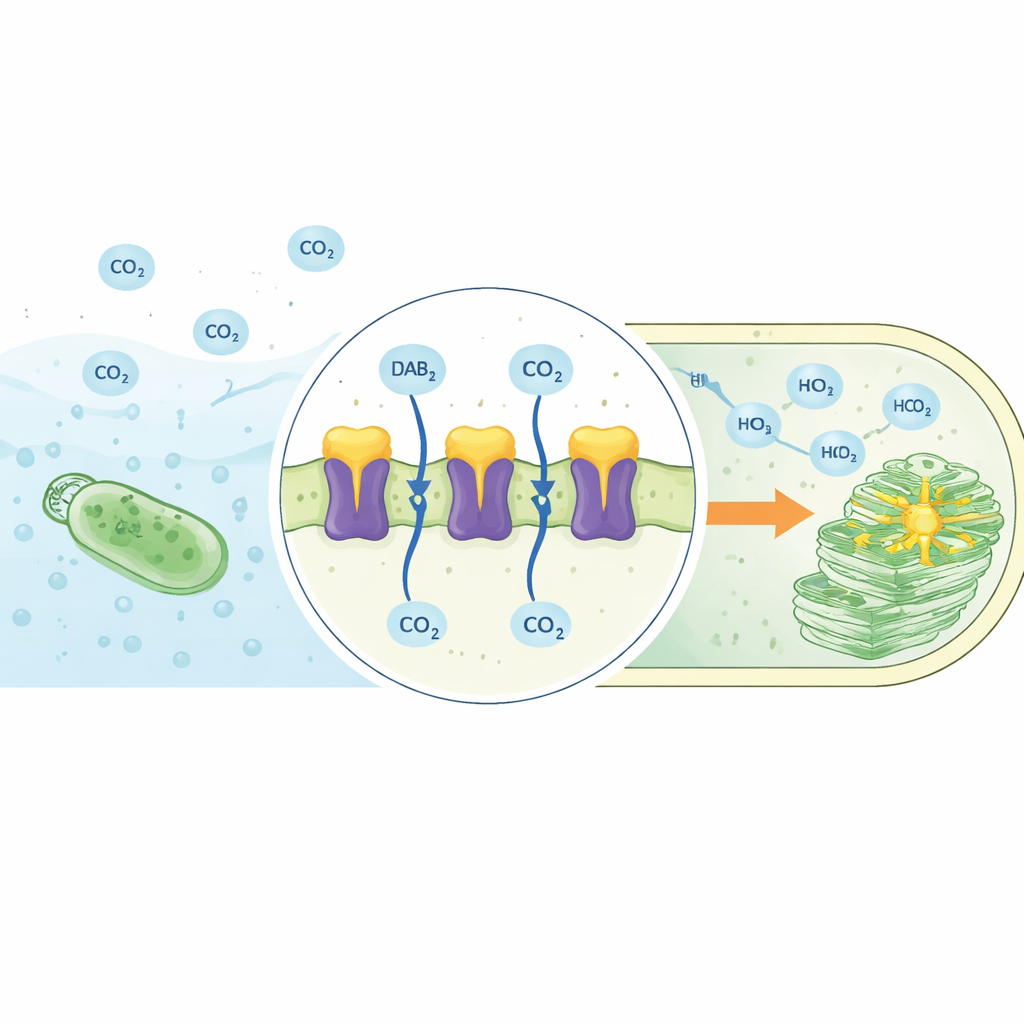
O complexo DAB2 revelado em 3D
Os autores utilizaram microscopia eletrônica crio de alta resolução para determinar a estrutura do complexo DAB2 inserido em um ambiente semelhante à membrana. O DAB2 revelou-se uma máquina de duas partes: uma proteína solúvel superior (DabA2) que se posiciona do lado interno da membrana, e uma proteína transmembrana inferior (DabB2) que forma um canal através da camada lipídica. DabA2 se assemelha a anidrases carbônicas conhecidas, enzimas que normalmente aceleram a interconversão entre CO₂ e bicarbonato, mas sua arquitetura está fortemente modificada. Ela contém dois domínios catalíticos relacionados e um “dedo” transmembrana único que se estende para dentro de DabB2. DabB2, por sua vez, lembra fortemente subunidades condutoras de prótons do Complexo I respiratório, um ator central na conversão de energia celular. Essa combinação sugere que o DAB2 conecta um centro de processamento de carbono a uma fonte de energia movida por prótons.
Uma câmara de reação oculta com túneis com comportas
Uma inspeção mais detalhada de DabA2 revelou um único íon de zinco no centro de um bolso profundamente enterrado, onde CO₂ e bicarbonato se ligam. Ao contrário das anidrases carbônicas tradicionais, esse sítio ativo carece de um aminoácido chave que normalmente estabiliza o efêmero estado de transição da reação. O sítio é acessível somente por túneis estreitos e sinuosos, revestidos em sua maior parte por resíduos hidrofóbicos. Usando tanto análise estrutural quanto espectroscopia infravermelha, os pesquisadores mostraram que o bolso pode ligar múltiplas moléculas de CO₂ fortemente, mas não as converte rapidamente em bicarbonato por si só. A geometria apertada dos túneis cria estrangulamentos que provavelmente precisam abrir e fechar de forma controlada, funcionando como comportas que regulam quando o CO₂ pode entrar e quando o bicarbonato pode sair.
Energia de prótons e tráfego unidirecional
A estrutura de DabB2 e uma série de mutações direcionadas indicam que ele forma uma via para prótons — íons de hidrogênio carregados positivamente — através da membrana. Resíduos carregados e polares-chave alinham-se para formar uma rota contínua para transferência de prótons, lembrando os “fios de água” que transportam prótons em complexos respiratórios. A extensão helicoidal incomum de DabA2 encaixa-se em DabB2 justamente onde se esperaria uma segunda meia-conduta, aparentemente ajudando a formar a saída para prótons. Quando os autores alteraram resíduos específicos ao longo dessa rota, o complexo deixou de suportar o crescimento de E. coli privadas de carbono, embora as proteínas ainda fossem produzidas. Testes adicionais mostraram que o DAB2 não depende de gradientes de sódio, distinguindo-o de complexos relacionados em alguns patógenos; em vez disso, parece ser impulsionado puramente pela força prótonmotriz da membrana.
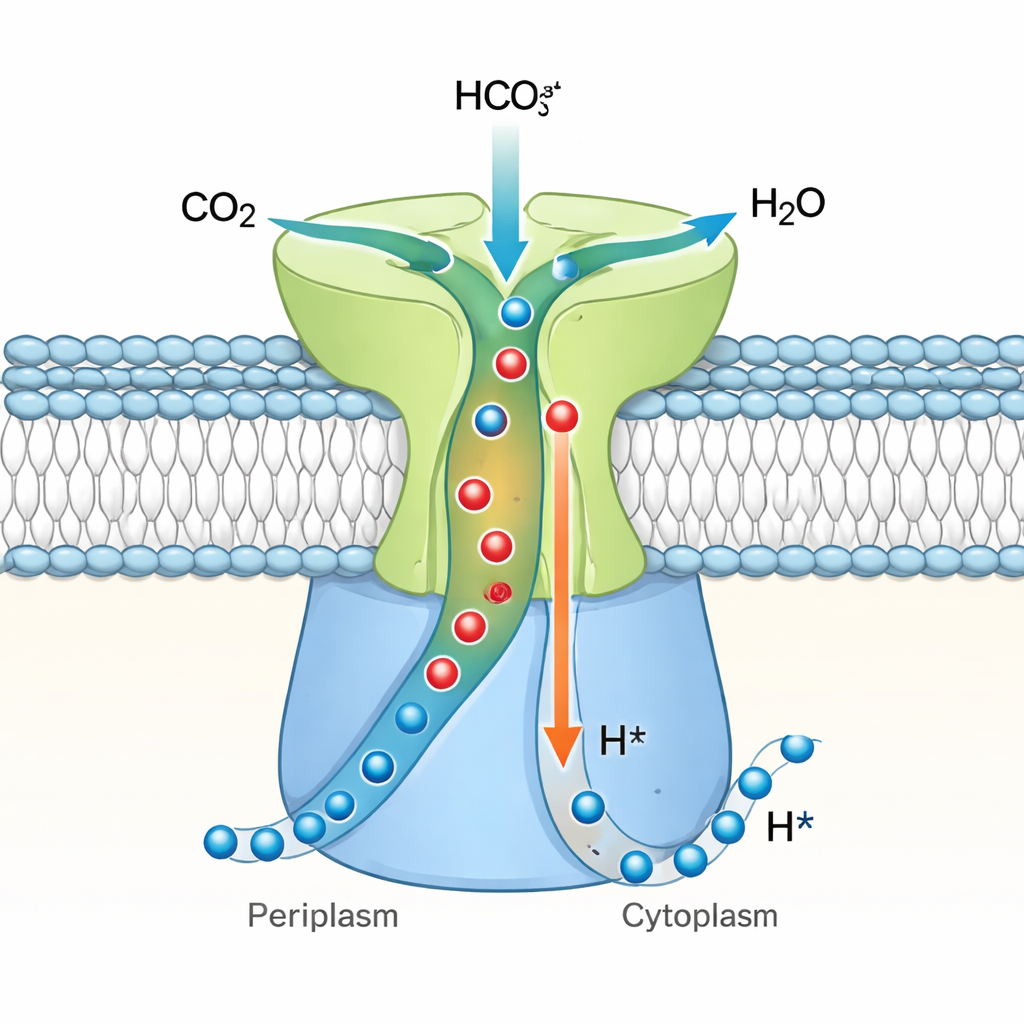
Uma válvula unidirecional para o carbono celular
Reunindo esses achados, os autores propõem que o DAB2 é uma anidrase carbônica vetorial — um hidratador de CO₂ unidirecional fortemente acoplado ao fluxo de prótons. Em seu modelo, CO₂ e água podem escorregar para o sítio ativo enterrado quando o sistema está em um estado de repouso “fechado”, mas a geometria dos túneis e o impedimento estérico impedem que o bicarbonato retorne, bloqueando a reação reversa. Quando existe um gradiente de prótons através da membrana, prótons movem-se através de DabB2 e desencadeiam deslocamentos sutis na estrutura do DAB2, provavelmente transmitidos pelo “dedo” de DabA2. Esses deslocamentos abrem os túneis e reorganizam o sítio ativo de modo que o CO₂ seja convertido eficientemente em bicarbonato e liberado para o interior da célula, enquanto os prótons são transportados através da membrana. Esse projeto permite que bactérias quimiolitotróficas vinculem a captação de carbono diretamente ao seu estado energético, garantindo que a captura de CO₂ ocorra somente quando há força prótonmotriz suficiente para acioná-la. O trabalho estabelece o DAB2 como um protótipo de uma família difundida de máquinas de conversão de carbono movidas por prótons e amplia nossa compreensão de como micróbios projetam suas próprias bombas microscópicas de carbono.
Citação: Lo, Y.K., Seletskiy, M., Bohn, S. et al. Structural basis of membrane potential coupled vectorial CO₂ hydration by the DAB2 complex in chemolithoautotrophs. Nat Commun 17, 4071 (2026). https://doi.org/10.1038/s41467-026-72558-7
Palavras-chave: captação de dióxido de carbono, quimiolitotrófos, anhidrase carbônica, força prótonmotriz, estrutura de proteína de membrana