Clear Sky Science · pl
Strukturalne podstawy potencjałem błonowym sprzężonej wektorowej hydratacji CO₂ przez kompleks DAB2 u chemolitotrofoautotrofów
Jak mikroby pomagają zamykać węgiel
W ukryciu oceanów i w siarkowych osadach żyją mikroby, które utrzymują się wyłącznie z nieorganicznych chemikaliów i dwutlenku węgla. W tym badaniu odkryto, jak jedna z takich grup bakterii używa maleńkiej molekularnej maszyny, zwanej kompleksem DAB2, by wyciągać CO₂ ze środowiska i przekształcać go w formę użyteczną dla komórki. Zrozumienie tej naturalnej pompy węglowej ma znaczenie dla podstawowej nauki o klimacie i może w przyszłości zainspirować nowe metody wychwytywania CO₂ z otoczenia.
Microskopijna pompa węglowa
Wiele mikroorganizmów buduje swoje ciała z rozpuszczonego w wodzie węgla nieorganicznego — mieszaniny CO₂ i blisko spokrewnionych cząsteczek. Polegają przy tym na powolnym enzymie RuBisCO, który przyłącza CO₂ do związków organicznych, reakcji kluczowej dla globalnego cyklu węgla. Ponieważ RuBisCO jest wolny i łatwo ulega zakłóceniom, wiele mikroorganizmów wykształciło mechanizmy koncentracji CO₂, które magazynują użyteczny węgiel tam, gdzie działa RuBisCO. Choć systemy te są dobrze znane u fotosyntetycznych cyjanobakterii, chemolitotrofoautotrofy — bakterie pozyskujące energię przez utlenianie substancji nieorganicznych, jak siarka — pozostawały zagadką. Wcześniejsze badania wskazywały na rodzinę kompleksów błonowych, łącznie nazywanych DAC, które pomagają tym bakteriom rosnąć przy ograniczonym węglu. Jeden z takich systemów, DAB2 z bakterii Halothiobacillus neapolitanus, potrafi uratować rośnięcie E. coli pozbawionego węgla, co sugeruje, że aktywnie kumuluje węgiel nieorganiczny wewnątrz komórek.
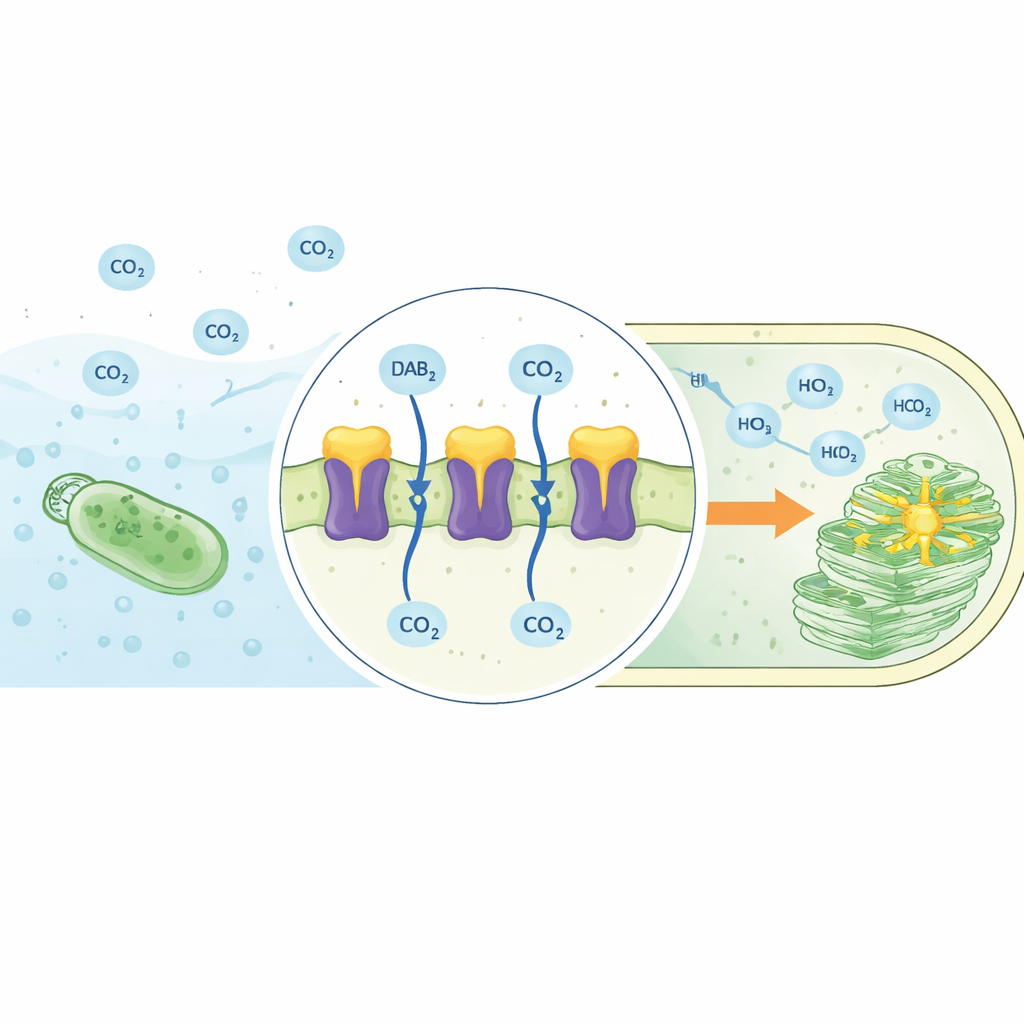
Kompleks DAB2 ujawniony w 3D
Autorzy użyli wysokorozdzielczej kriogenicznej mikroskopii elektronowej, by określić strukturę kompleksu DAB2 osadzonego w środowisku przypominającym błonę. DAB2 okazał się maszyną złożoną z dwóch części: górnej, rozpuszczalnej podjednostki (DabA2) leżącej po wewnętrznej stronie błony, oraz dolnej, przezbłonowej podjednostki (DabB2) tworzącej kanał przez warstwę lipidową. DabA2 przypomina znane anhydrazy węglanowe, enzymy, które zwykle przyspieszają przekształcanie CO₂ i wodorowęglanu, lecz jego architektura jest silnie zmodyfikowana. Zawiera dwa pokrewne domeny katalityczne i unikalny przezbłonowy „palec”, który sięga w dół do DabB2. DabB2 z kolei wygląda uderzająco podobnie do podjednostek przewodzących protony z kompleksu oddechowego I, centralnego elementu konwersji energii w komórce. To zestawienie sugeruje, że DAB2 łączy centrum przetwarzające węgiel ze źródłem napędu napędzanym protonami.
Ukryta komora reakcyjna z zaporowymi tunelami
Bardziej szczegółowa analiza DabA2 ujawniła pojedynczy jon cynku w centrum głęboko pogrzebanego kieszonkowego miejsca, gdzie wiążą się CO₂ i wodorowęglan. W przeciwieństwie do podręcznikowych anhydraz, to miejsce aktywne nie ma kluczowego aminokwasu, który zwykle stabilizuje ulotny stan przejściowy reakcji. Do tego miejsca prowadzą jedynie wąskie, kręte tunele wysłane przeważnie resztami o właściwościach odpychających wodę. Wykorzystując zarówno analizę strukturalną, jak i spektroskopię w podczerwieni, badacze wykazali, że kieszeń może silnie wiązać wiele cząsteczek CO₂, ale sama w sobie nie przekształca ich szybko w wodorowęglan. Ścisła geometria tuneli tworzy wąskie gardła, które prawdopodobnie muszą otwierać się i zamykać w kontrolowany sposób, działając jak zawory regulujące, kiedy CO₂ może wejść, a wodorowęglan wyjść.
Siła protonów i ruch jednokierunkowy
Struktura DabB2 i seria ukierunkowanych mutacji wskazują, że tworzy on ścieżkę dla protonów — naładowanych dodatnio jonów wodoru — przez błonę. Kluczowe naładowane i polarne reszty ustawiają się tak, by tworzyć ciągłą drogę transportu protonów, przypominającą „druty wodne”, które przenoszą protony w kompleksach oddechowych. Nietypowe przedłużenie helisy z DabA2 wchodzi w szczelinę DabB2 dokładnie tam, gdzie oczekiwałby się drugi półkanał, najwyraźniej pomagając utworzyć wypływ dla protonów. Gdy autorzy zaburzyli konkretne reszty wzdłuż tej trasy, kompleks nie był już w stanie wspierać wzrostu E. coli pozbawionego węgla, choć białka wciąż były wytwarzane. Dodatkowe testy wykazały, że DAB2 nie zależy od gradientów sodu, co odróżnia go od pokrewnych kompleksów w niektórych patogenach; zamiast tego wydaje się być napędzany wyłącznie siłą protonomotoryczną błony.
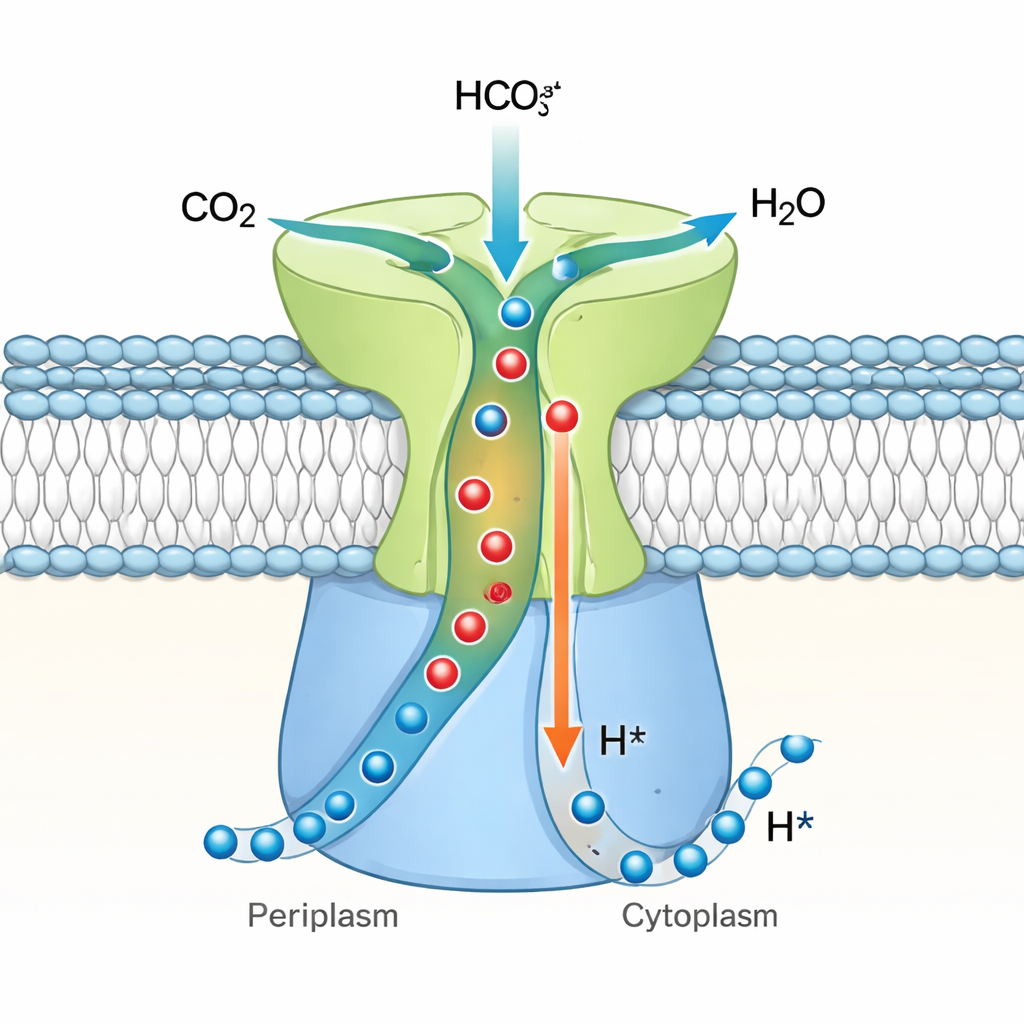
Jednokierunkowy zawór dla węgla komórkowego
Łącząc te obserwacje, autorzy proponują, że DAB2 jest wektorową anhydrazą węglanową — jednokierunkową hydratazą CO₂ ściśle sprzężoną z przepływem protonów. W ich modelu CO₂ i woda mogą wślizgiwać się do pogrzebanego miejsca aktywnego, gdy system znajduje się w „zamkniętym” stanie spoczynkowym, ale geometria tuneli i przeszkody steryczne uniemożliwiają wodorowęglanowi powrót, blokując reakcję odwrotną. Gdy istnieje gradient protonowy przez błonę, protony przemieszczają się przez DabB2 i wywołują subtelne przesunięcia w strukturze DAB2, prawdopodobnie przekazywane przez „palec” DabA2. Te przesunięcia otwierają tunele i reorganizują miejsce aktywne tak, że CO₂ jest efektywnie przekształcany w wodorowęglan i uwalniany do wnętrza komórki, podczas gdy protony są przenoszone przez błonę. Taki mechanizm pozwala bakteriom chemolitotrofoautotroficznym wiązać pobór węgla bezpośrednio ze stanem energetycznym, zapewniając, że wychwyt CO₂ zachodzi tylko wtedy, gdy jest wystarczająca siła protonomotoryczna, by go napędzać. Praca ustala DAB2 jako prototyp szeroko rozpowszechnionej, napędzanej protonami rodziny maszyn przekształcających węgiel i poszerza nasze rozumienie, jak mikroby projektują swoje mikroskopijne pompy węglowe.
Cytowanie: Lo, Y.K., Seletskiy, M., Bohn, S. et al. Structural basis of membrane potential coupled vectorial CO₂ hydration by the DAB2 complex in chemolithoautotrophs. Nat Commun 17, 4071 (2026). https://doi.org/10.1038/s41467-026-72558-7
Słowa kluczowe: pobieranie dwutlenku węgla, chemolitotrofoautotrofy, anhydraza węglanowa, siła protonomotoryczna, struktura białka błonowego