Clear Sky Science · de
Strukturelle Grundlage der membranpotenzialgekoppelten vektoriellen CO₂-Hydratisierung durch den DAB2-Komplex in Chemolithoautotrophen
Wie Mikroben dabei helfen, Kohlenstoff zu binden
Versteckt in Ozeanen und schwefelreichen Sedimenten gibt es Mikroben, die vollständig von anorganischen Chemikalien und Kohlendioxid leben. Diese Studie enthüllt, wie eine solche Bakteriengruppe eine winzige molekulare Maschine, den DAB2-Komplex, einsetzt, um CO₂ aus ihrer Umgebung zu entziehen und in eine für die Zelle nutzbare Form umzuwandeln. Das Verständnis dieser natürlichen Kohlenstoffpumpe ist wichtig für die Grundlagen der Klimawissenschaft und könnte langfristig neue Ansätze zur Umgehung von CO₂ aus der Umwelt inspirieren.
Eine mikroskopische Kohlenstoffpumpe
Viele Mikroorganismen bauen ihren Körper aus gelöstem anorganischem Kohlenstoff, einem Gemisch aus CO₂ und eng verwandten Molekülen im Wasser. Sie sind auf ein träges Enzym, RuBisCO, angewiesen, das CO₂ an organische Verbindungen bindet — eine Reaktion, die im Zentrum des globalen Kohlenstoffkreislaufs steht. Da RuBisCO langsam und leicht störbar ist, haben viele Mikroben CO₂-konzentrierende Mechanismen entwickelt, die verwertbaren Kohlenstoff genau dort speichern, wo RuBisCO arbeitet. Während diese Systeme bei photosynthetischen Cyanobakterien gut untersucht sind, blieben Chemolithoautotrophe — Bakterien, die Energie durch Oxidation anorganischer Substanzen wie Schwefel gewinnen — rätselhaft. Frühere Arbeiten deuteten auf eine Familie von Membrankomplexen hin, die kollektiv als DACs bezeichnet werden und diesen Bakterien helfen, bei Kohlenstoffknappheit zu wachsen. Ein solches System, DAB2 aus dem Bakterium Halothiobacillus neapolitanus, kann kohlenstoffgestresstes E. coli retten, was darauf hindeutet, dass es aktiv anorganischen Kohlenstoff innerhalb der Zellen anreichert.
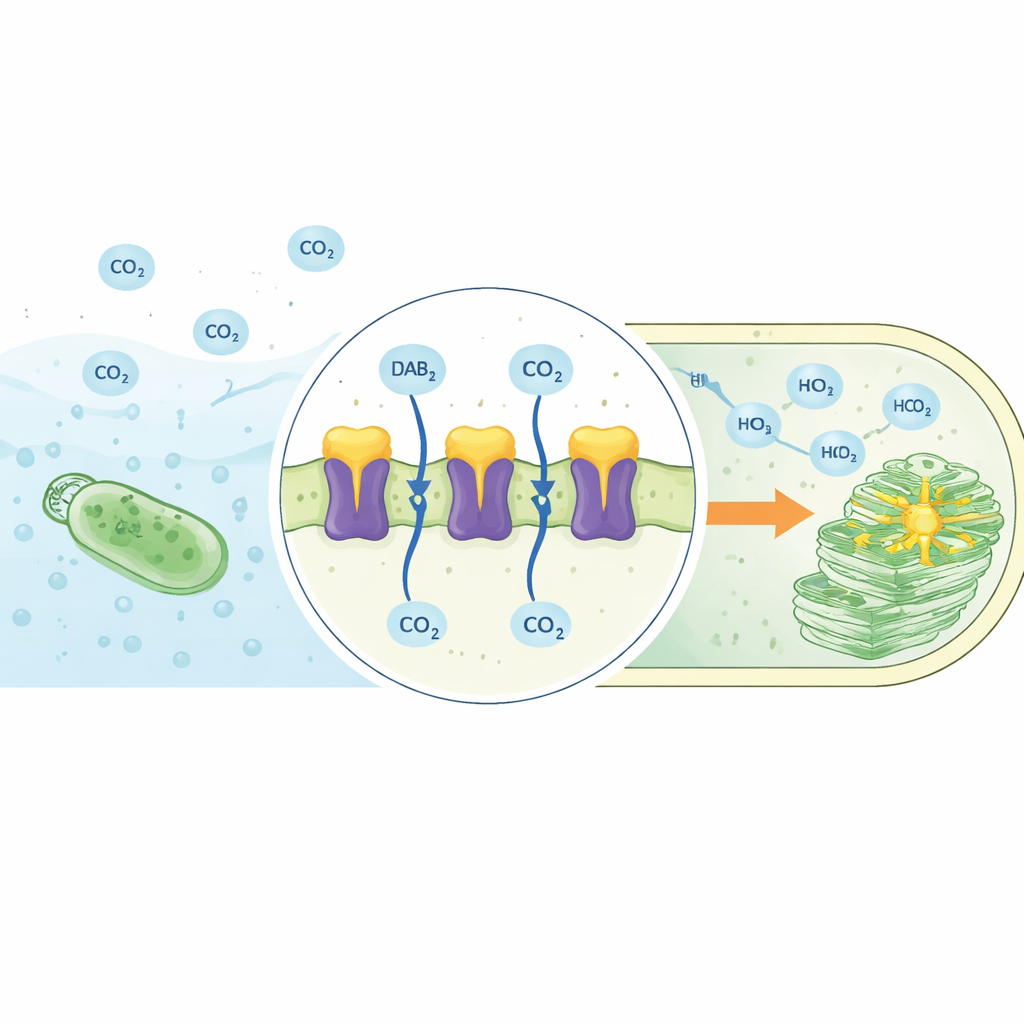
Der DAB2-Komplex in 3D enthüllt
Die Autoren nutzten hochauflösende kryogene Elektronenmikroskopie, um die Struktur des DAB2-Komplexes in einer membranähnlichen Umgebung zu bestimmen. DAB2 erwies sich als zweigliedrige Maschine: ein oberer, löslicher Proteinanteil (DabA2), der auf der Innenseite der Membran sitzt, und ein unterer, membranüberspannender Anteil (DabB2), der einen Kanal durch die Lipidschicht bildet. DabA2 ähnelt bekannten Carboanhydrasen, Enzymen, die normalerweise die Umwandlung von CO₂ und Bicarbonat beschleunigen, doch seine Architektur ist stark verändert. Es enthält zwei verwandte katalytische Domänen und einen einzigartigen transmembranen „Finger“, der in DabB2 hineinreicht. DabB2 wiederum ähnelt auffallend Protonen-leitenden Untereinheiten des respiratorischen Komplex I, einem zentralen Akteur der zellulären Energieumwandlung. Diese Kombination legt nahe, dass DAB2 ein Kohlenstoffverarbeitungszentrum mit einer protongetriebenen Energiequelle verbindet.
Eine verborgene Reaktionskammer mit verschließbaren Tunneln
Eine genauere Untersuchung von DabA2 zeigte ein einzelnes Zinkion im Zentrum einer tief eingebetteten Tasche, in der CO₂ und Bicarbonat binden. Im Gegensatz zu klassischen Carboanhydrasen fehlt dieser aktiven Stelle eine entscheidende Aminosäure, die normalerweise den flüchtigen Übergangszustand der Reaktion stabilisiert. Die Stelle ist nur durch enge, gewundene Tunnel erreichbar, die überwiegend mit wasserabweisenden Resten ausgekleidet sind. Mithilfe sowohl struktureller Analysen als auch Infrarotspektroskopie zeigten die Forscher, dass die Tasche mehrere CO₂-Moleküle stark binden kann, diese aber nicht von sich aus schnell zu Bicarbonat umwandelt. Die enge Geometrie der Tunnel schafft Engpässe, die sich kontrolliert öffnen und schließen müssen und als Tore wirken, die regeln, wann CO₂ eintreten und wann Bicarbonat austreten kann.
Protonenenergie und Einbahnverkehr
Die Struktur von DabB2 und eine Reihe gezielter Mutationen deuten darauf hin, dass es einen Weg für Protonen — positiv geladene Wasserstoffionen — quer durch die Membran bildet. Wichtige geladene und polare Reste reihen sich aus, um eine kontinuierliche Route für den Protonentransfer zu bilden, erinnernd an die „Wasserdrähte“, die Protonen in respiratorischen Komplexen transportieren. Die ungewöhnliche helikale Ausstülpung von DabA2 steckt genau dort in DabB2, wo man die zweite Halbkanal erwartet hätte, und hilft offenbar, den Ausgang für Protonen zu bilden. Wenn die Autoren bestimmte Reste entlang dieser Route störten, konnte der Komplex das Wachstum kohlenstoffgestressten E. coli nicht mehr unterstützen, obwohl die Proteine weiterhin produziert wurden. Weitere Tests zeigten, dass DAB2 nicht auf Natriumgradienten angewiesen ist, wodurch es sich von verwandten Komplexen einiger Krankheitserreger unterscheidet; stattdessen scheint es ausschließlich durch die protonmotorische Kraft der Membran angetrieben zu werden.
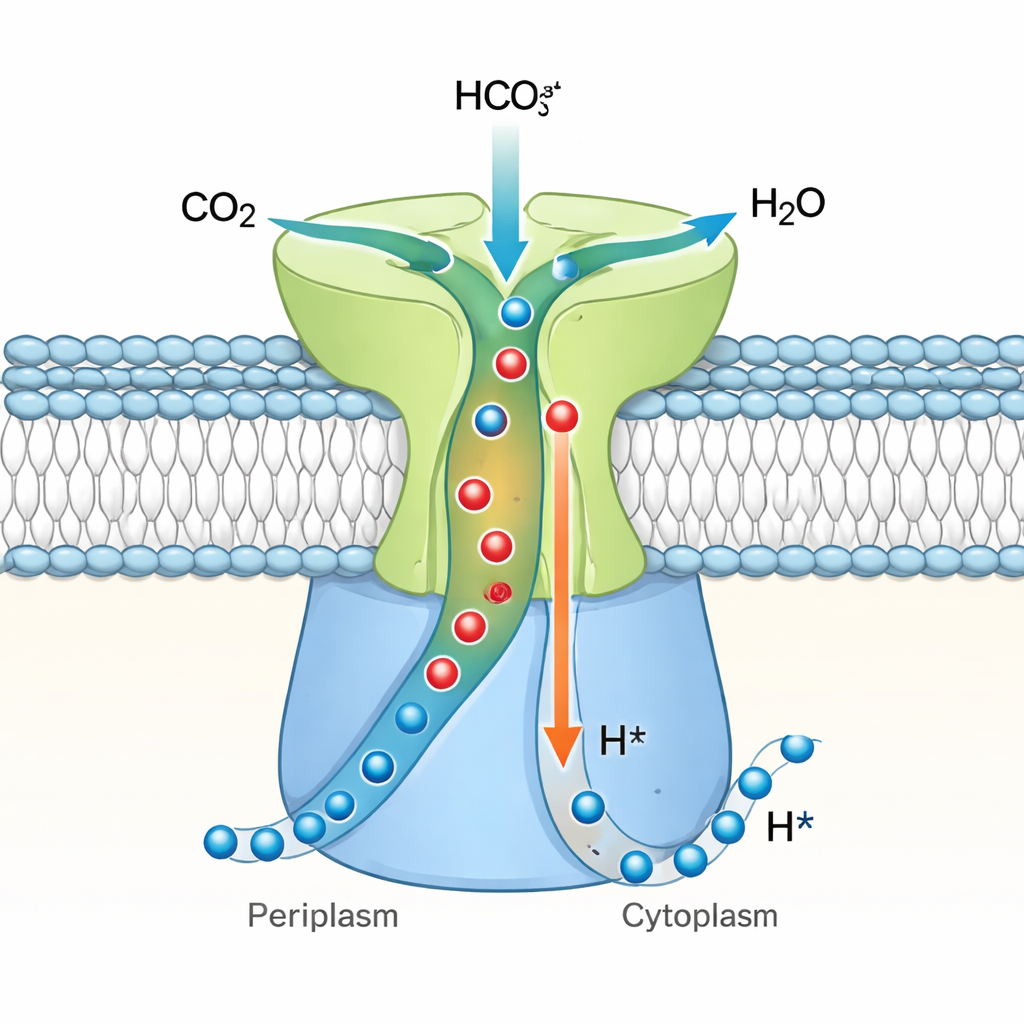
Ein Rückschlagventil für zellulären Kohlenstoff
Zusammengefasst schlagen die Autoren vor, dass DAB2 eine vektorielle Carboanhydrase ist — ein einseitig wirkender CO₂-Hydrator, der eng mit dem Protonenfluss gekoppelt ist. In ihrem Modell können CO₂ und Wasser in die verborgene aktive Stelle eindringen, wenn das System im „geschlossenen“ Ruhezustand ist, aber die Geometrie der Tunnel und sterische Hinderung verhindern, dass Bicarbonat zurückkehrt und damit die Rückreaktion blockiert. Besteht ein Protonengradient über die Membran, bewegen sich Protonen durch DabB2 und lösen subtile Verschiebungen in der DAB2-Struktur aus, wahrscheinlich vermittelt durch den DabA2‑„Finger“. Diese Verschiebungen öffnen die Tunnel und reorganisieren die aktive Stelle so, dass CO₂ effizient zu Bicarbonat umgewandelt und ins Zellinnere freigesetzt wird, während Protonen über die Membran transportiert werden. Dieses Design erlaubt es chemolithoautotrophen Bakterien, die Kohlenstoffaufnahme direkt an ihren Energiestatus zu koppeln und sicherzustellen, dass die CO₂-Aufnahme nur dann erfolgt, wenn ausreichend Protonenenergie vorhanden ist, um sie anzutreiben. Die Arbeit etabliert DAB2 als Prototyp einer verbreiteten, protongetriebenen Familie von Kohlenstoff-umwandelnden Maschinen und erweitert unser Bild davon, wie Mikroben ihre eigenen mikroskopischen Kohlenstoffpumpen bauen.
Zitation: Lo, Y.K., Seletskiy, M., Bohn, S. et al. Structural basis of membrane potential coupled vectorial CO₂ hydration by the DAB2 complex in chemolithoautotrophs. Nat Commun 17, 4071 (2026). https://doi.org/10.1038/s41467-026-72558-7
Schlüsselwörter: Kohlenstoffdioxidaufnahme, Chemolithoautotrophe, Carboanhydrase, Protonmotorische Kraft, Membranproteinstruktur