Clear Sky Science · fr
Base structurelle de l’hydratation vectorielle du CO₂ couplée au potentiel de membrane par le complexe DAB2 chez les chimiolithoautotrophes
Comment les microbes contribuent à séquestrer le carbone
Cachés dans les océans et dans des sédiments riches en soufre se trouvent des microbes qui vivent entièrement de substances inorganiques et de dioxyde de carbone. Cette étude révèle comment un groupe de ces bactéries utilise une petite machine moléculaire, appelée complexe DAB2, pour extraire le CO₂ de son environnement et le convertir en une forme utilisable par la cellule. Comprendre cette pompe naturelle à carbone est important pour la science climatique fondamentale et pourrait, à terme, inspirer de nouvelles méthodes de capture du CO₂ dans l’environnement.
Une pompe à carbone microscopique
De nombreux micro-organismes construisent leur matière à partir du carbone inorganique dissous, un mélange de CO₂ et de molécules proches en solution. Ils dépendent d’une enzyme lente, la RuBisCO, pour fixer le CO₂ sur des composés organiques, une réaction au cœur du cycle global du carbone. Parce que la RuBisCO est lente et facilement perturbée, de nombreux microbes ont évolué des mécanismes de concentration du CO₂ qui stockent le carbone utilisable là où la RuBisCO agit. Si ces systèmes sont bien connus chez les cyanobactéries photosynthétiques, les chimiolithoautotrophes — des bactéries qui tirent de l’énergie de l’oxydation de substances inorganiques comme le soufre — demeuraient énigmatiques. Des travaux antérieurs ont pointé une famille de complexes membranaires, appelés collectivement DAC, qui aident ces bactéries à se développer quand le carbone est rare. L’un de ces systèmes, DAB2 de la bactérie Halothiobacillus neapolitanus, peut sauver des E. coli en manque de carbone, ce qui suggère qu’il accumule activement du carbone inorganique à l’intérieur des cellules.
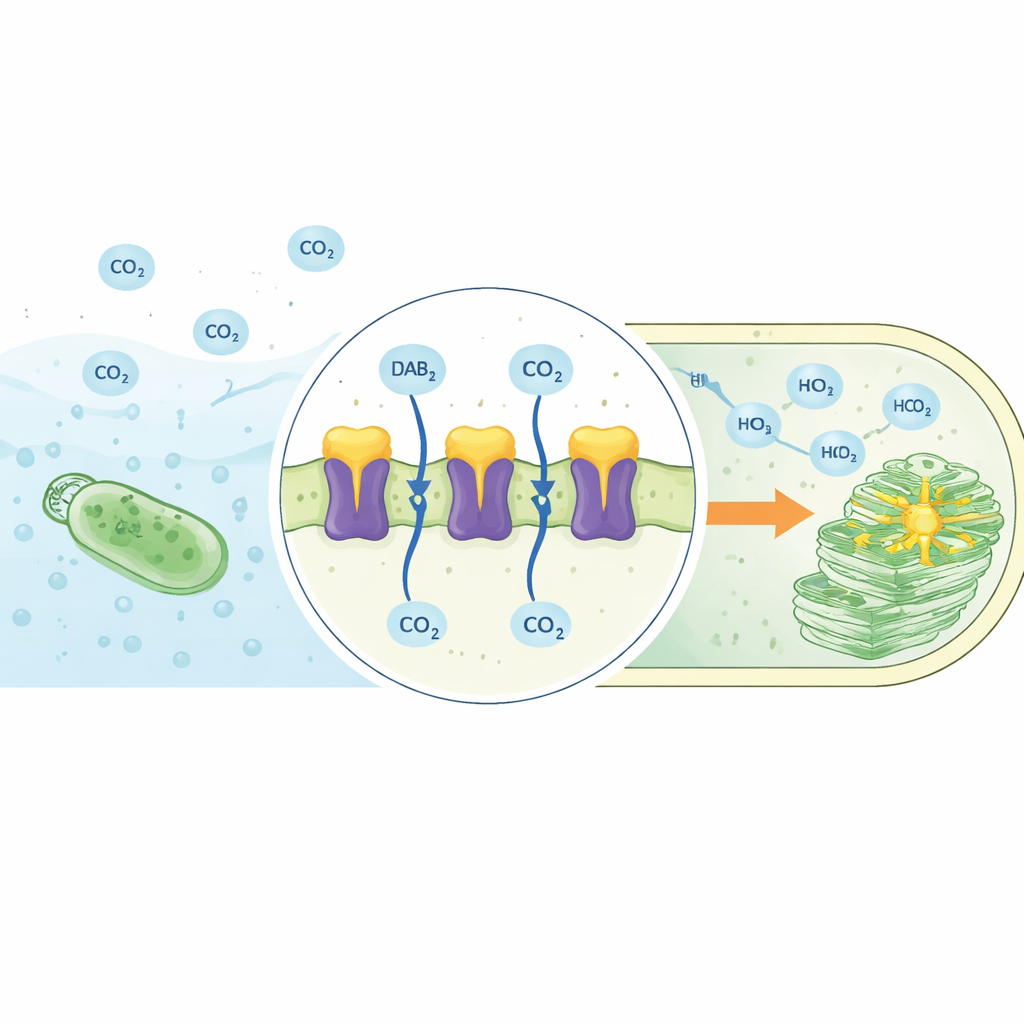
Le complexe DAB2 révélé en 3D
Les auteurs ont utilisé la cryo-microscopie électronique à haute résolution pour déterminer la structure du complexe DAB2 intégré dans un environnement similaire à une membrane. DAB2 s’est avéré être une machine en deux parties : une protéine soluble supérieure (DabA2) située du côté interne de la membrane, et une protéine transmembranaire inférieure (DabB2) qui forme un canal à travers la couche lipidique. DabA2 ressemble à des anhydrazes carboniques connues, des enzymes qui accélèrent normalement l’interconversion du CO₂ et du bicarbonate, mais son architecture est fortement modifiée. Elle contient deux domaines catalytiques apparentés et un « doigt » transmembranaire unique qui s’enfonce dans DabB2. DabB2, pour sa part, ressemble étonnamment aux sous-unités conductrices de protons du Complexe I respiratoire, un acteur central de la conversion d’énergie cellulaire. Cette combinaison suggère que DAB2 relie un centre de traitement du carbone à une source d’énergie entraînée par les protons.
Une chambre de réaction cachée avec des tunnels à portails
Une inspection plus fine de DabA2 a révélé un ion zinc unique au centre d’une poche profondément enfouie, où se lient le CO₂ et le bicarbonate. Contrairement aux anhydrases carboniques classiques, ce site actif manque d’un acide aminé clé qui stabilise normalement l’état de transition fugitif de la réaction. Le site n’est accessible que par des tunnels étroits et sinueux bordés principalement de résidus hydrophobes. Grâce à l’analyse structurale et à la spectroscopie infrarouge, les chercheurs ont montré que la poche peut lier plusieurs molécules de CO₂ avec forte affinité mais n’effectue pas, par elle-même, une conversion rapide en bicarbonate. La géométrie serrée des tunnels crée des goulots d’étranglement qui doivent probablement s’ouvrir et se fermer de manière contrôlée, agissant comme des portails qui régulent l’entrée du CO₂ et la sortie du bicarbonate.
Puissance protonique et trafic unidirectionnel
La structure de DabB2 et une série de mutations ciblées indiquent qu’il forme une voie pour les protons — des ions hydrogène chargés positivement — à travers la membrane. Des résidus chargés et polaires clés s’alignent pour former un trajet continu pour le transfert protonique, rappelant les « fils d’eau » qui transportent les protons dans les complexes respiratoires. L’extension hélicoïdale inhabituelle de DabA2 s’insère dans DabB2 exactement là où l’on attendrait une seconde demi-voie, contribuant apparemment à former la sortie pour les protons. Lorsque les auteurs ont perturbé des résidus spécifiques le long de ce trajet, le complexe n’a plus pu soutenir la croissance d’E. coli privés de carbone, même si les protéines étaient toujours produites. Des tests supplémentaires ont montré que DAB2 ne dépend pas de gradients de sodium, ce qui le distingue de complexes apparentés chez certains agents pathogènes ; il semble au contraire être entraîné uniquement par la force protonmotrice de la membrane.
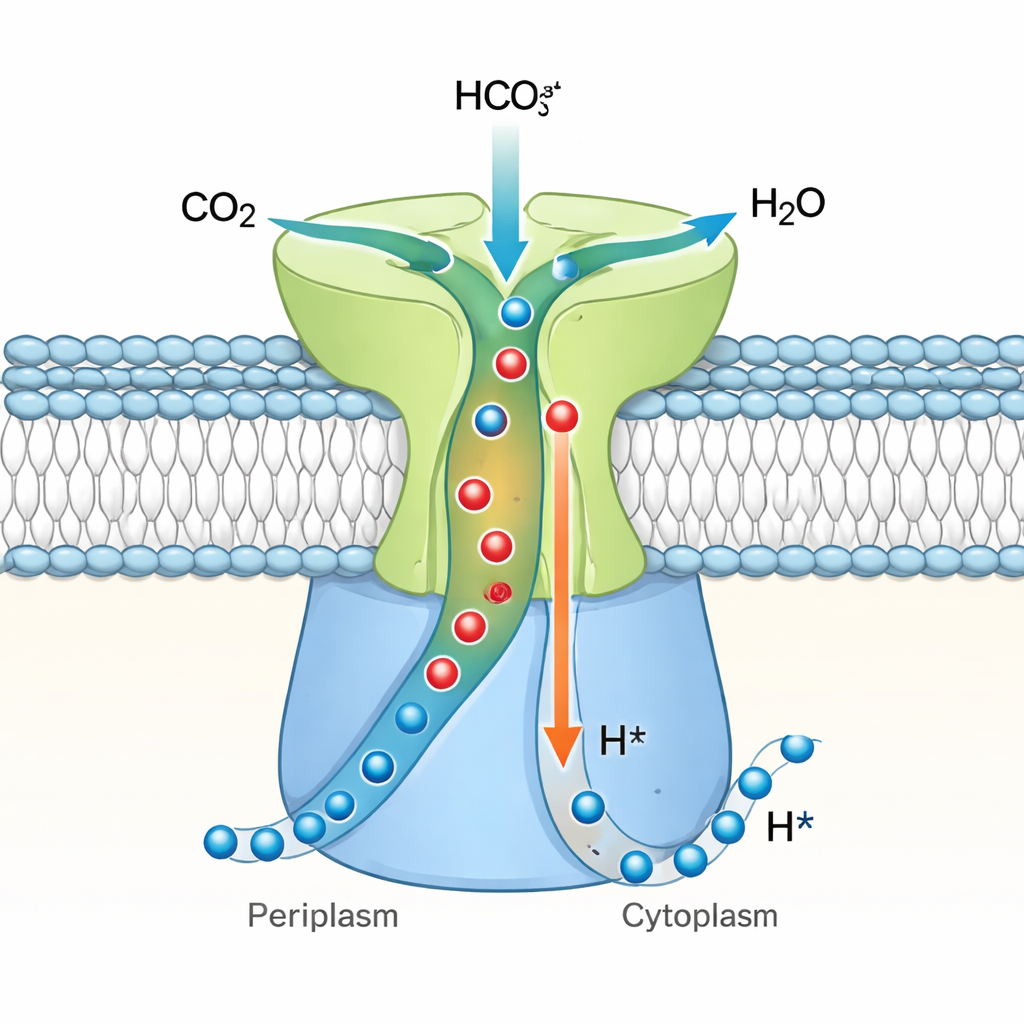
Une valve unidirectionnelle pour le carbone cellulaire
En regroupant ces résultats, les auteurs proposent que DAB2 soit une anhydrase carbonique vectorielle — un hydratant du CO₂ à sens unique étroitement couplé au flux de protons. Selon leur modèle, le CO₂ et l’eau peuvent glisser dans le site actif enfoui lorsque le système est dans un état de repos « fermé », mais la géométrie des tunnels et l’encombrement stérique empêchent le bicarbonate de revenir, bloquant la réaction inverse. Lorsqu’un gradient de protons existe à travers la membrane, les protons circulent via DabB2 et déclenchent de subtiles modifications de la structure de DAB2, probablement transmises par le « doigt » de DabA2. Ces modifications ouvrent les tunnels et réorganisent le site actif de sorte que le CO₂ est efficacement converti en bicarbonate et relâché dans l’intérieur cellulaire, tandis que les protons sont transportés de l’autre côté de la membrane. Ce dispositif permet aux bactéries chimiolithoautotrophes de lier directement la capture du carbone à leur état énergétique, garantissant que la captation du CO₂ n’a lieu que lorsqu’il y a suffisamment de puissance protonique pour l’alimenter. Ce travail établit DAB2 comme un prototype d’une famille répandue de machines de conversion du carbone entraînées par les protons et élargit notre compréhension de la manière dont les microbes conçoivent leurs propres pompes microscopiques à carbone.
Citation: Lo, Y.K., Seletskiy, M., Bohn, S. et al. Structural basis of membrane potential coupled vectorial CO₂ hydration by the DAB2 complex in chemolithoautotrophs. Nat Commun 17, 4071 (2026). https://doi.org/10.1038/s41467-026-72558-7
Mots-clés: absorption du dioxyde de carbone, chimiolithoautotrophes, anhydrase carbonique, force protonmotrice, structure des protéines membranaires