Clear Sky Science · it
Base strutturale dell’idratazione vettoriale del CO₂ accoppiata al potenziale di membrana dal complesso DAB2 nei chemolitotrofi
Come i microbi contribuiscono a sequestrare il carbonio
Nascosti negli oceani e nei sedimenti ricchi di zolfo ci sono microbi che vivono interamente di sostanze inorganiche e di anidride carbonica. Questo studio svela come un gruppo di batteri utilizzi una minuscola macchina molecolare, chiamata complesso DAB2, per estrarre CO₂ dall’ambiente e convertirlo in una forma utilizzabile dalla cellula. Comprendere questa pompa naturale di carbonio è importante per la scienza climatica di base e potrebbe infine ispirare nuovi modi per catturare il CO₂ dall’ambiente.
Una pompa microscopica del carbonio
Molti microrganismi costruiscono i loro tessuti a partire dal carbonio inorganico disciolto, una miscela di CO₂ e molecole correlate in acqua. Si affidano a un enzima lento, la RuBisCO, per fissare il CO₂ su composti organici, una reazione al centro del ciclo globale del carbonio. Poiché la RuBisCO è lenta e facilmente compromessa, molti microbi hanno evoluto meccanismi di concentrazione del CO₂ che accumulano carbonio utilizzabile proprio nel luogo in cui opera la RuBisCO. Pur essendo ben noti nei cianobatteri fotosintetici, i chemolitotrofi — batteri che ricavano energia ossidando sostanze inorganiche come lo zolfo — sono rimasti in parte misteriosi. Lavori precedenti avevano indicato una famiglia di complessi di membrana, collettivamente chiamati DAC, che aiutano questi batteri a crescere quando il carbonio scarseggia. Un sistema in particolare, DAB2 dal batterio Halothiobacillus neapolitanus, è in grado di salvare ceppi di E. coli affamati di carbonio, suggerendo che accumuli attivamente carbonio inorganico all’interno delle cellule.
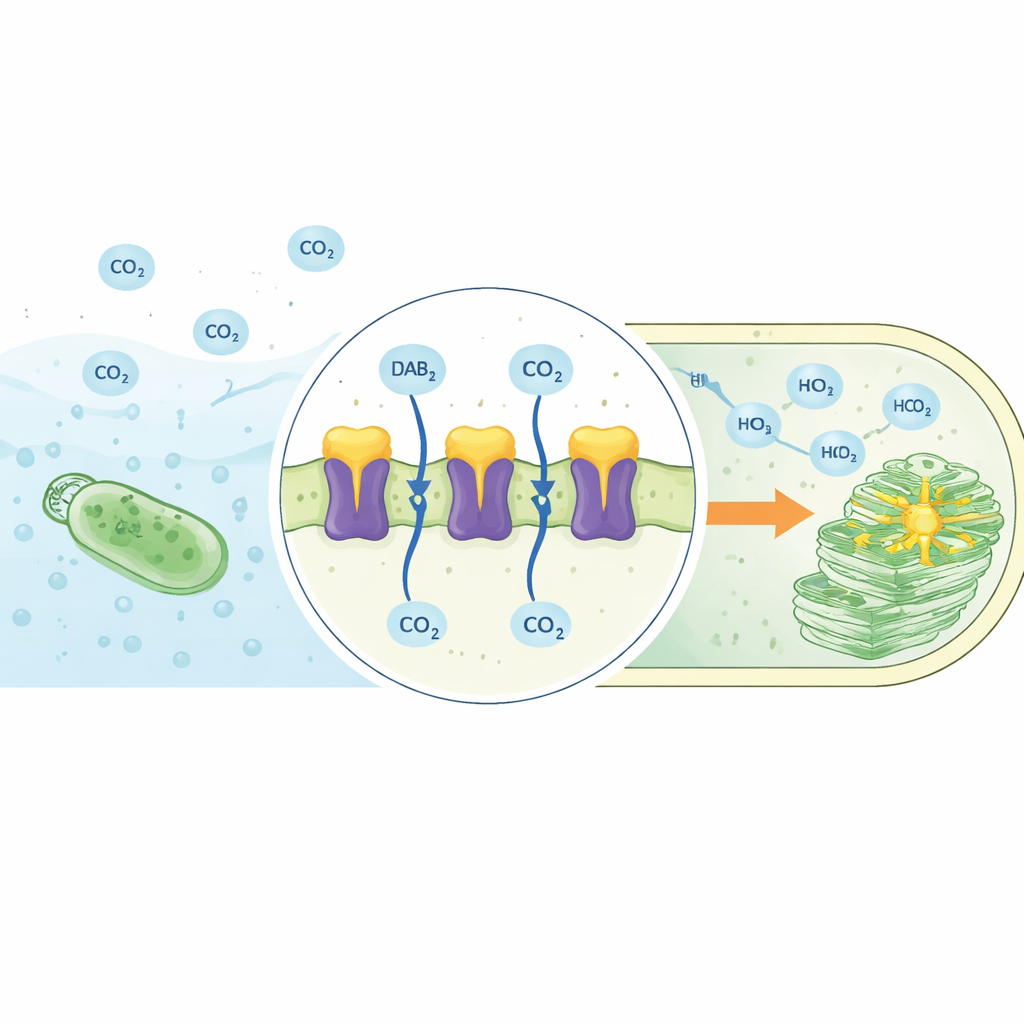
Il complesso DAB2 rivelato in 3D
Gli autori hanno usato la microscopia crioelettronica ad alta risoluzione per determinare la struttura del complesso DAB2 inserito in un ambiente simile alla membrana. DAB2 si è rivelato una macchina in due parti: una proteina solubile superiore (DabA2) che si trova sul lato interno della membrana, e una proteina inferiore che attraversa la membrana (DabB2) che forma un canale attraverso lo strato lipidico. DabA2 somiglia ad anidrasi carboniche note, enzimi che normalmente accelerano l’interconversione tra CO₂ e bicarbonato, ma la sua architettura è fortemente modificata. Contiene due domini catalitici correlati e un “dito” transmembrana unico che si estende verso il basso dentro DabB2. DabB2, a sua volta, assomiglia sorprendentemente alle subunità che conducono protoni del Complesso I respiratorio, un attore centrale nella conversione di energia cellulare. Questa combinazione suggerisce che DAB2 colleghi un centro di elaborazione del carbonio a una fonte di energia guidata da protoni.
Una camera di reazione nascosta con gallerie a sportello
Un’ispezione più ravvicinata di DabA2 ha rivelato un singolo ione zinco al centro di una tasca profondamente sepolta, dove si legano CO₂ e bicarbonato. Diversamente dalle anidrasi carboniche dei manuali, questo sito attivo è privo di un amminoacido chiave che normalmente stabilizza lo stato di transizione fugace della reazione. Il sito è accessibile solo attraverso tunnel stretti e tortuosi rivestiti principalmente da residui idrofobici. Usando sia l’analisi strutturale sia la spettroscopia infrarossa, i ricercatori hanno dimostrato che la tasca può legare più molecole di CO₂ con alta affinità ma non le converte rapidamente in bicarbonato da sola. La geometria stretta dei tunnel crea strozzature che probabilmente devono aprirsi e chiudersi in modo controllato, agendo come sportelli che regolano quando il CO₂ può entrare e quando il bicarbonato può uscire.
Energia dei protoni e traffico a senso unico
La struttura di DabB2 e una serie di mutazioni mirate indicano che esso forma un percorso per i protoni — ioni idrogeno carichi positivamente — attraverso la membrana. Residui carichi e polari chiave si allineano per formare una rotta continua per il trasferimento di protoni, ricordando i “fili d’acqua” che trasportano protoni nei complessi respiratori. L’estensione elicoidale insolita da DabA2 si inserisce in DabB2 proprio dove ci si aspetterebbe una seconda mezza-canale, contribuendo apparentemente a formare l’uscita per i protoni. Quando gli autori hanno disturbato residui specifici lungo questo percorso, il complesso non è più stato in grado di sostenere la crescita di E. coli affamati di carbonio, nonostante le proteine fossero ancora prodotte. Test aggiuntivi hanno mostrato che DAB2 non si affida a gradienti di sodio, distinguendolo dai complessi correlati in alcuni patogeni; invece, sembra essere guidato esclusivamente dalla forza protomotrice della membrana.
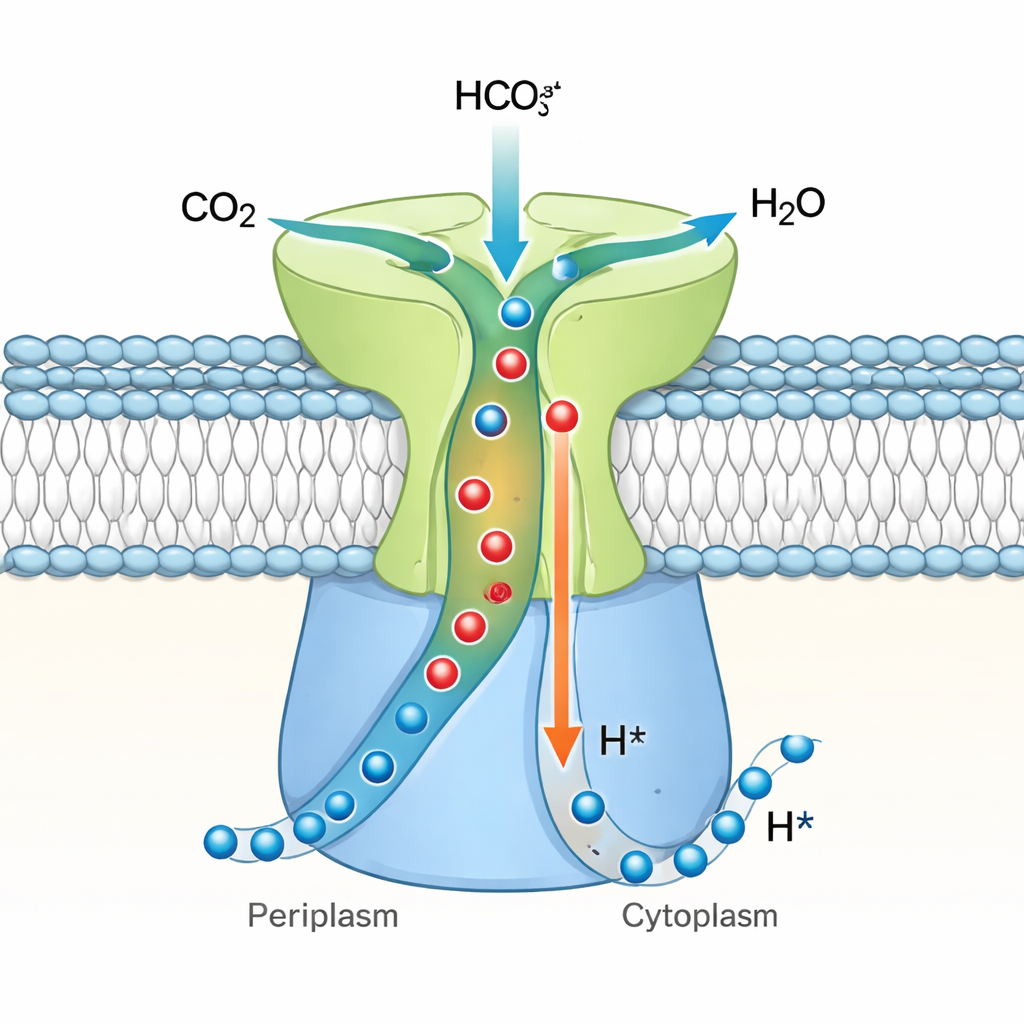
Una valvola a senso unico per il carbonio cellulare
Raccogliendo insieme questi risultati, gli autori propongono che DAB2 sia un’anidrasi carbonica vettoriale — un idratatore unidirezionale del CO₂ strettamente accoppiato al flusso di protoni. Nel loro modello, CO₂ e acqua possono insinuarsi nel sito attivo sepolto quando il sistema è in uno stato di riposo “chiuso”, ma la geometria dei tunnel e l’ingombro sterico impediscono al bicarbonato di rientrare, bloccando la reazione inversa. Quando esiste un gradiente di protoni attraverso la membrana, i protoni si muovono attraverso DabB2 e provocano sottili cambiamenti nella struttura di DAB2, probabilmente trasmessi dal “dito” di DabA2. Questi spostamenti aprono i tunnel e riorganizzano il sito attivo in modo che il CO₂ venga convertito efficacemente in bicarbonato e rilasciato nell’interno della cellula, mentre i protoni vengono trasportati attraverso la membrana. Questo design permette ai batteri chemolitotrofi di legare l’assorbimento di carbonio direttamente al loro stato energetico, assicurando che la cattura di CO₂ proceda solo quando c’è sufficiente energia protomotrice per alimentarla. Il lavoro stabilisce DAB2 come un prototipo di una famiglia diffusa di macchine di conversione del carbonio guidate dai protoni e amplia la nostra comprensione di come i microbi progettano le proprie pompe microscopiche del carbonio.
Citazione: Lo, Y.K., Seletskiy, M., Bohn, S. et al. Structural basis of membrane potential coupled vectorial CO₂ hydration by the DAB2 complex in chemolithoautotrophs. Nat Commun 17, 4071 (2026). https://doi.org/10.1038/s41467-026-72558-7
Parole chiave: assorbimento di anidride carbonica, chemolitotrofi, anidrasi carbonica, forza protomotrice, struttura delle proteine di membrana