Clear Sky Science · pt
Dissecação molecular e funcional usando CaMPARI-seq revela a organização neuronal para dissociar comportamentos dependentes de fluxo óptico
Como o cérebro distingue curva de natação em linha reta
Quando animais se movem, todo o mundo visual parece deslizar diante de seus olhos. Dessa cena em constante mudança, o cérebro precisa responder a uma pergunta simples, mas vital: estamos girando ou nos movendo em linha reta? Este artigo usa pequenos peixes-zebra e uma nova técnica molecular de "realce" para revelar como células cerebrais específicas separam esses dois tipos de movimento para controlar movimentos oculares ou a natação do corpo inteiro.
Ver o movimento como uma paisagem em fluxo
Quando um animal nada ou anda, padrões de luz varrem os olhos — um fenômeno chamado fluxo óptico. O fluxo rotacional, como quando um animal gira a cabeça, deve principalmente desencadear movimentos oculares que estabilizam o olhar. O fluxo translacional, como quando o animal nada para frente, deve em vez disso ativar o corpo para manter o movimento com a água ou o solo ao redor. Em muitos vertebrados, incluindo peixes-zebra, uma região do mesencéfalo chamada pré-tecto desempenha papel central em interpretar esses padrões de movimento e rotear sinais para centros motores. Trabalhos anteriores mapearam muitos neurônios pré-tectais que respondem ao fluxo óptico, mas não estava claro quais tipos celulares precisos, definidos por sua expressão gênica e conexões, eram responsáveis por diferentes comportamentos dirigidos pelo movimento.
Iluminar neurônios ativos e ler seus genes
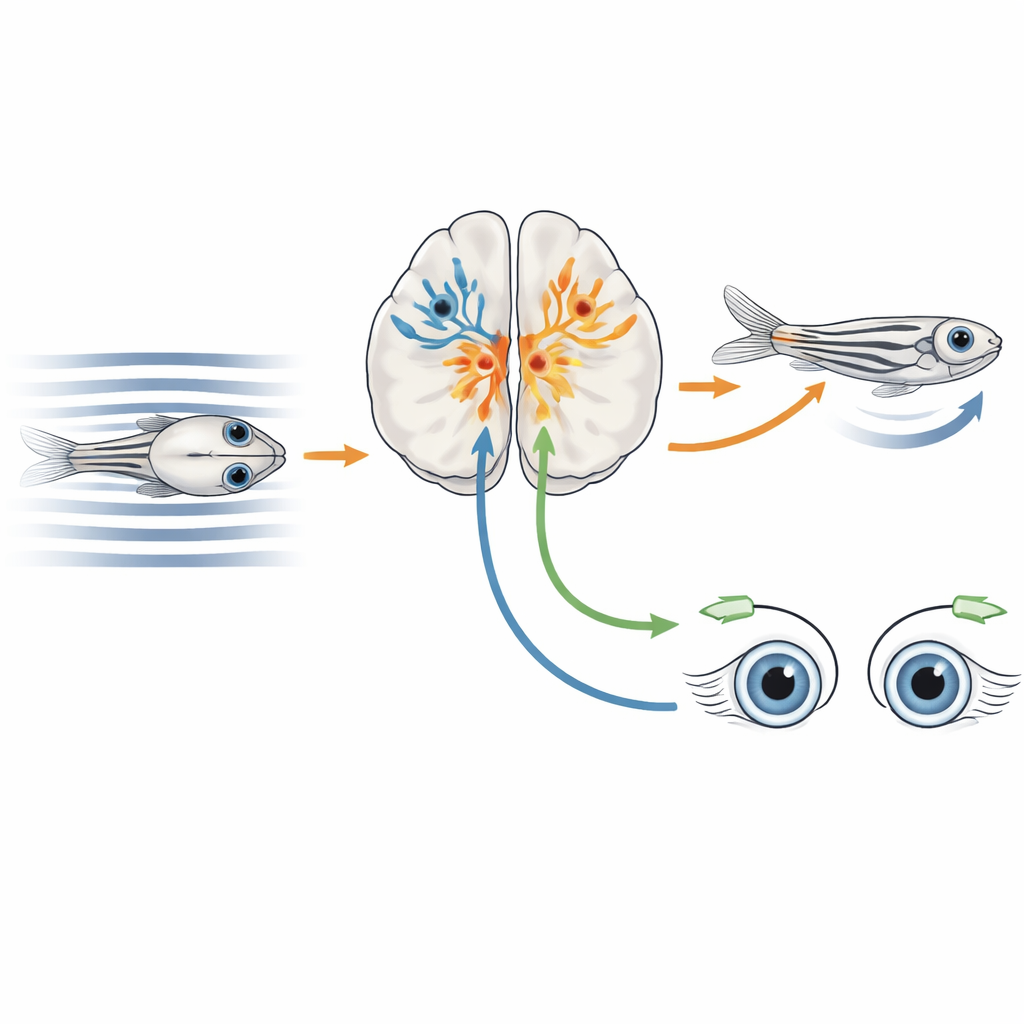
Os pesquisadores desenvolveram uma abordagem híbrida que chamam de CaMPARI-seq, combinando marcação óptica de neurônios ativos com perfilagem de expressão gênica em célula única. Eles engenheiraram larvas de peixe-zebra para que a maioria dos neurônios produzisse uma proteína fluorescente especial, CaMPARI2, direcionada ao núcleo celular. Quando neurônios estão ativos e iluminados com luz ultravioleta, essa proteína muda permanentemente do verde para o vermelho. A equipe expôs os peixes a padrões listrados em movimento que geram uma variedade de condições de fluxo óptico binocular, enquanto iluminava o pré-tecto com ultravioleta. Neurônios ativos e responsivos ao movimento ficaram vermelhos, foram depois isolados um a um, e suas sequências de RNA foram lidas para determinar quais genes cada célula expressava.
Construindo um atlas celular dos neurônios de fluxo óptico
Ao agrupar milhares de células marcadas com base em seus padrões de expressão gênica, os autores identificaram um grande grupo pré-tectal marcado pelo gene tcf7l2, cujas células em sua maioria também apresentavam genes típicos de neurônios inibitórios. Usando peixes geneticamente modificados em que células tcf7l2-positivas conduziam um indicador de cálcio, verificaram que essa população ampla incluía quase todos os tipos de resposta ao fluxo óptico descritos anteriormente, desde neurônios sintonizados para movimento visto por apenas um olho até outros que respondiam somente quando ambos os olhos detectavam movimento coerente para frente ou para trás. A divisão adicional do grupo tcf7l2 revelou sete subtipos molecularmente distintos, cada um com sua combinação de genes marcadores e uma posição espacial amplamente não sobreposta dentro do pré-tecto, sugerindo um mosaico de circuitos inibitórios especializados ao redor do núcleo de processamento do movimento.
Dois subtipos-chave com funções muito diferentes
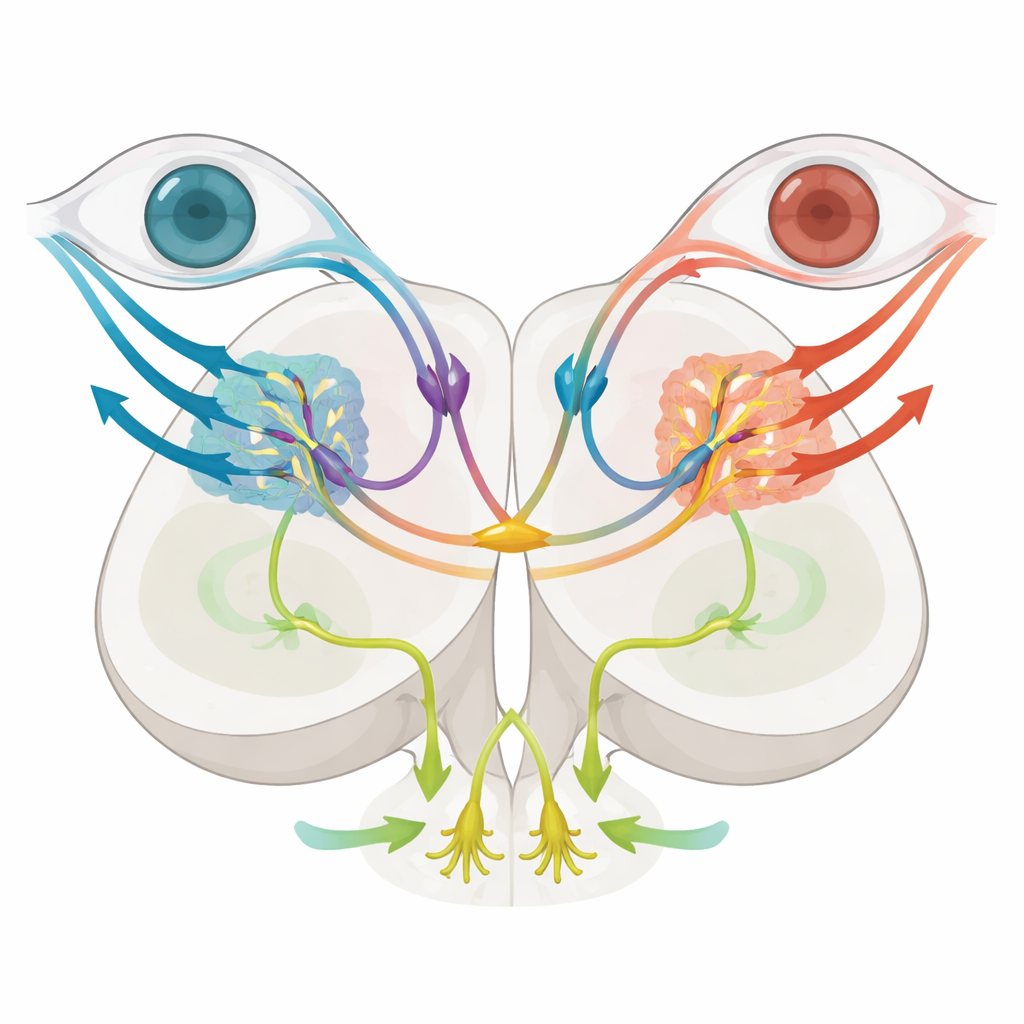
Entre esses subtipos, dois se destacaram. Células que expressam o gene mafaa localizavam-se numa região lateral migrada que se sobrepõe a fibras retinianas sensíveis à direção que chegam. Imagens e traçagens anatômicas mostraram que esses neurônios fazem conexões locais e respondem fortemente quando listras se movem numa direção particular em apenas um olho, compatível com um papel em codificar movimento simples, específico de um olho, que pode suportar o giro ocular. Em contraste, neurônios que expressam nkx1.2lb ocupavam uma zona mais medial e enviavam projeções longas e cruzadas através de um comissura dorsal para o lado oposto, formando uma ponte entre circuitos pré-tectais esquerdo e direito. Essas células nkx1.2lb-positivas também eram em sua maioria inibitórias e, em conjunto, cobriam uma ampla variedade de tipos de resposta ao fluxo óptico, incluindo padrões monoculares e binoculares, sugerindo que ajudam a comparar sinais dos dois olhos.
Desembaralhando respostas oculares e corporais
Para testar a função, a equipe eliminou seletivamente neurônios pré-tectais nkx1.2lb-positivos usando uma enzima genética de "suicídio" que se torna tóxica apenas nessas células quando os peixes recebem uma droga inócua. Após a ablação, as larvas ainda mostraram movimentos de acompanhamento ocular normais quando o mundo girava ao redor delas, indicando que o fluxo óptico rotacional e a resposta optocinética permaneceram intactos. No entanto, quando o padrão do solo se moveu para imitar a natação para frente, a resposta optomotora foi severamente enfraquecida: os peixes percorreram distâncias menores e suas batidas de cauda ficaram menos coordenadas, mostrando computação perturbada da direção de nado. Imagens cerebrais revelaram que células sintonizadas especificamente para fluxo óptico translacional foram reduzidas, enquanto detectores monoculares básicos de movimento foram em grande parte preservados. Juntos, esses experimentos sugerem que os neurônios comissurais nkx1.2lb são essenciais para integrar sinais de ambos os olhos para estimar o movimento em linha reta e dirigir a natação para frente, mas não são necessários para estabilizar o olhar durante a rotação.
Por que isso importa para entender a detecção de movimento
Para um não-especialista, a mensagem-chave é que o cérebro separa "estou girando?" de "estou me movendo para frente?" atribuindo essas questões a conjuntos diferentes de células, mesmo dentro de um peixe minúsculo. Os autores mostram que uma ponte inibitória específica entre os lados esquerdo e direito do pré-tecto é crucial para reconhecer movimento translacional e direcionar o corpo, enquanto outros circuitos conseguem lidar com o movimento rotacional e os movimentos oculares sem essa ponte. O método CaMPARI-seq — usar luz para marcar células ativas e então ler sua identidade molecular — oferece uma maneira poderosa de ligar o que os neurônios fazem, como são construídos e quais comportamentos controlam. Insights desse sistema compacto de peixe-zebra podem ajudar a esclarecer como cérebros de vertebrados maiores, incluindo o nosso, mantêm a visão estável e a navegação precisa em um mundo em movimento.
Citação: Matsuda, K., Wang, CH., Kakinuma, H. et al. Molecular and functional dissection using CaMPARI-seq reveals the neuronal organization for dissociating optic flow-dependent behaviors. Nat Commun 17, 3411 (2026). https://doi.org/10.1038/s41467-026-71371-6
Palavras-chave: fluxo óptico, peixe-zebra, pré-tecto, sequenciamento de RNA de célula única, processamento de movimento visual