Clear Sky Science · de
Molekulare und funktionelle Aufschlüsselung mit CaMPARI-seq enthüllt die neuronale Organisation zur Trennung optic-flow‑abhängiger Verhaltensweisen
Wie das Gehirn Kurvenfahrt von geradem Schwimmen unterscheidet
Wenn Tiere sich bewegen, scheint die gesamte visuelle Welt an ihren Augen vorbeizuströmen. Aus dieser ständig wechselnden Szene muss das Gehirn eine einfache, aber lebenswichtige Frage beantworten: Drehen wir gerade oder bewegen wir uns geradeaus? Diese Studie nutzt winzige Zebrafische und eine neue molekulare „Leuchtmarker“-Technik, um zu zeigen, wie bestimmte Gehirnzellen diese beiden Bewegungsarten trennen, um entweder Augenbewegungen oder Ganzkörperschwimmen zu steuern.
Bewegung als fließende Landschaft sehen
Wenn ein Tier schwimmt oder läuft, fegen Lichtmuster über die Augen — ein Phänomen, das als optischer Fluss bezeichnet wird. Rotationaler Fluss, etwa wenn ein Tier den Kopf dreht, sollte vor allem Augenbewegungen antreiben, die den Blick stabilisieren. Translationaler Fluss, wie beim Vorwärtsschwimmen, sollte stattdessen den Körper anleiten, mit dem umgebenden Wasser oder Boden mitzuhalten. In vielen Wirbeltieren, einschließlich Zebrafischen, spielt eine Mittelhirnregion, das Prätectum, eine zentrale Rolle bei der Interpretation dieser Bewegungssignale und der Weiterleitung an motorische Zentren. Frühere Arbeiten hatten viele prätectale Neuronen kartiert, die auf optischen Fluss reagieren, doch blieb unklar, welche genauen Zelltypen — definiert durch Genexpression und Verschaltungen — für welche bewegungsgetriebenen Verhaltensweisen verantwortlich sind.
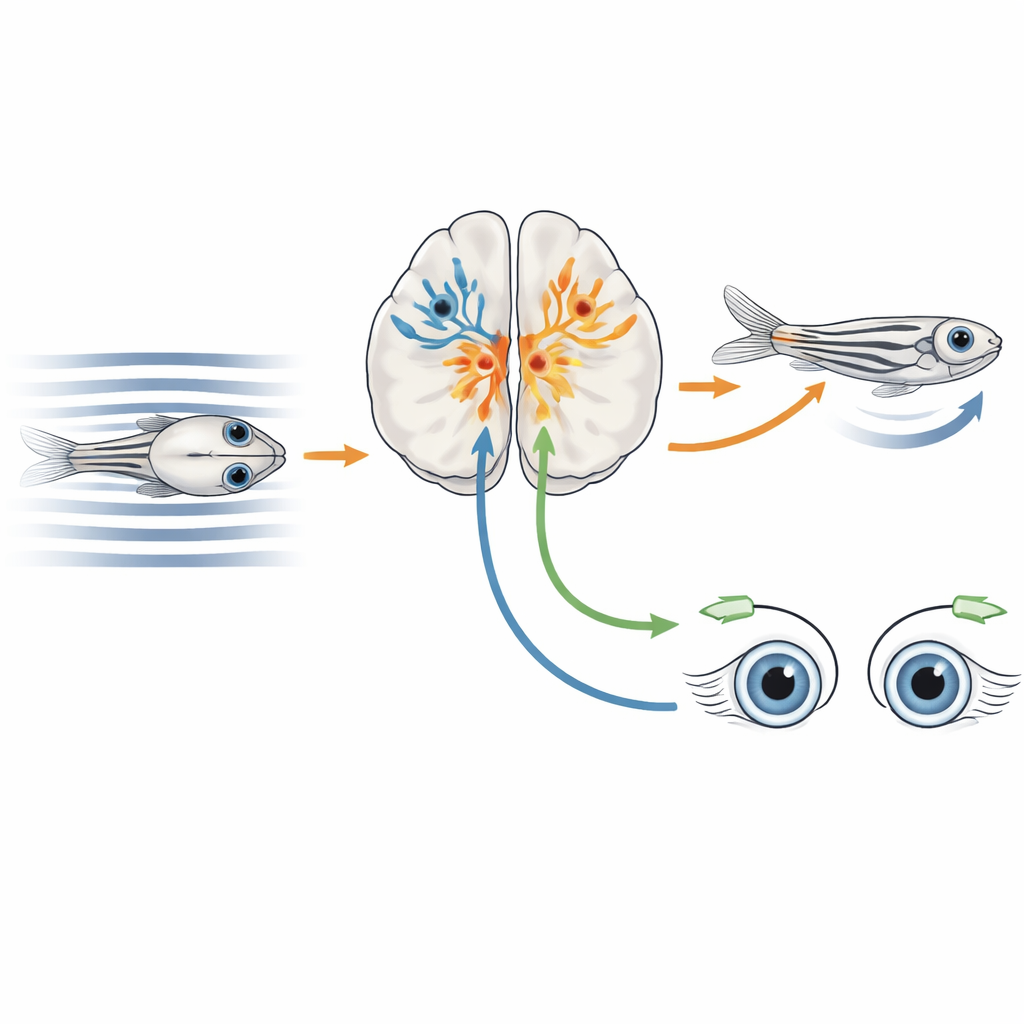
Aktive Neuronen anleuchten und ihre Gene lesen
Die Forschenden entwickelten einen hybriden Ansatz, den sie CaMPARI-seq nennen, und kombinierten optisches Markieren aktiver Neuronen mit Einzelzell-Genexpressionsprofilierung. Sie erzeugten Zebrafischlarven so, dass die meisten Neuronen ein spezielles fluoreszierendes Protein, CaMPARI2, im Zellkern produzierten. Wenn Neuronen aktiv sind und mit ultraviolettem Licht bestrahlt werden, wechselt dieses Protein dauerhaft von Grün zu Rot. Das Team setzte die Fische bewegten Streifenmustern aus, die verschiedene binokulare optische Flussbedingungen erzeugen, während sie Ultraviolettlicht auf das Prätectum strahlten. Aktive, bewegungsreaktive Neuronen wurden rot, wurden später einzeln isoliert und ihre RNA-Sequenzen gelesen, um zu bestimmen, welche Gene jede Zelle exprimierte.
Aufbau eines zellulären Atlas der Optic‑Flow‑Neuronen
Durch das Clustern von Tausenden markierter Zellen anhand ihrer Genexpressionsmuster identifizierten die Autor:innen eine bedeutende prätectale Gruppe, gekennzeichnet durch das Gen tcf7l2, deren Zellen größtenteils auch Gene trugen, die für inhibitorische Neuronen typisch sind. Mithilfe genetisch veränderter Fische, in denen tcf7l2-positive Zellen einen Calciumindikator trieben, bestätigten sie, dass diese breite Population nahezu alle zuvor beschriebenen Optic‑Flow‑Antworttypen umfasste — von Neuronen, die auf Bewegung eines einzelnen Auges abgestimmt sind, bis hin zu solchen, die nur reagieren, wenn beide Augen kohärente Vorwärts- oder Rückwärtsbewegung wahrnehmen. Eine weitere Unterteilung der tcf7l2‑Gruppe ergab sieben molekular eindeutig unterscheidbare Subtypen, jeder mit einer eigenen Kombination von Markergenen und einer weitgehend nicht überlappenden räumlichen Lage im Prätectum, was auf ein Mosaik spezialisierter inhibitorischer Schaltkreise rund um das Bewegungsverarbeitungszentrum hindeutet.
Zwei Schlüssel‑Subtypen mit sehr unterschiedlichen Aufgaben
Unter diesen Subtypen stachen zwei hervor. Zellen, die das Gen mafaa exprimieren, lagen in einer lateral migrierten Region, die mit einlaufenden richtungsselektiven retinalen Fasern überlappt. Bildgebung und anatomische Rückverfolgung zeigten, dass diese Neuronen lokale Verbindungen herstellen und stark reagieren, wenn Streifen in einer bestimmten Richtung nur in einem Auge bewegt werden — passend zu einer Rolle bei der Kodierung einfacher, augenspezifischer Bewegung, die Augenbewegungen unterstützen kann. Im Gegensatz dazu besetzten Neuronen, die nkx1.2lb exprimieren, eine medialere Zone und schickten lange, gekreuzte Projektionen durch eine dorsale Hirnkommissur zur Gegenseite und bildeten so eine Brücke zwischen linken und rechten prätectalen Schaltkreisen. Diese nkx1.2lb‑positiven Zellen waren ebenfalls überwiegend inhibitorisch und deckten zusammen eine breite Vielfalt von Optic‑Flow‑Antworttypen ab, einschließlich mono- und binokularer Muster, was darauf hindeutet, dass sie bei der Gegenüberstellung der Signale beider Augen helfen.
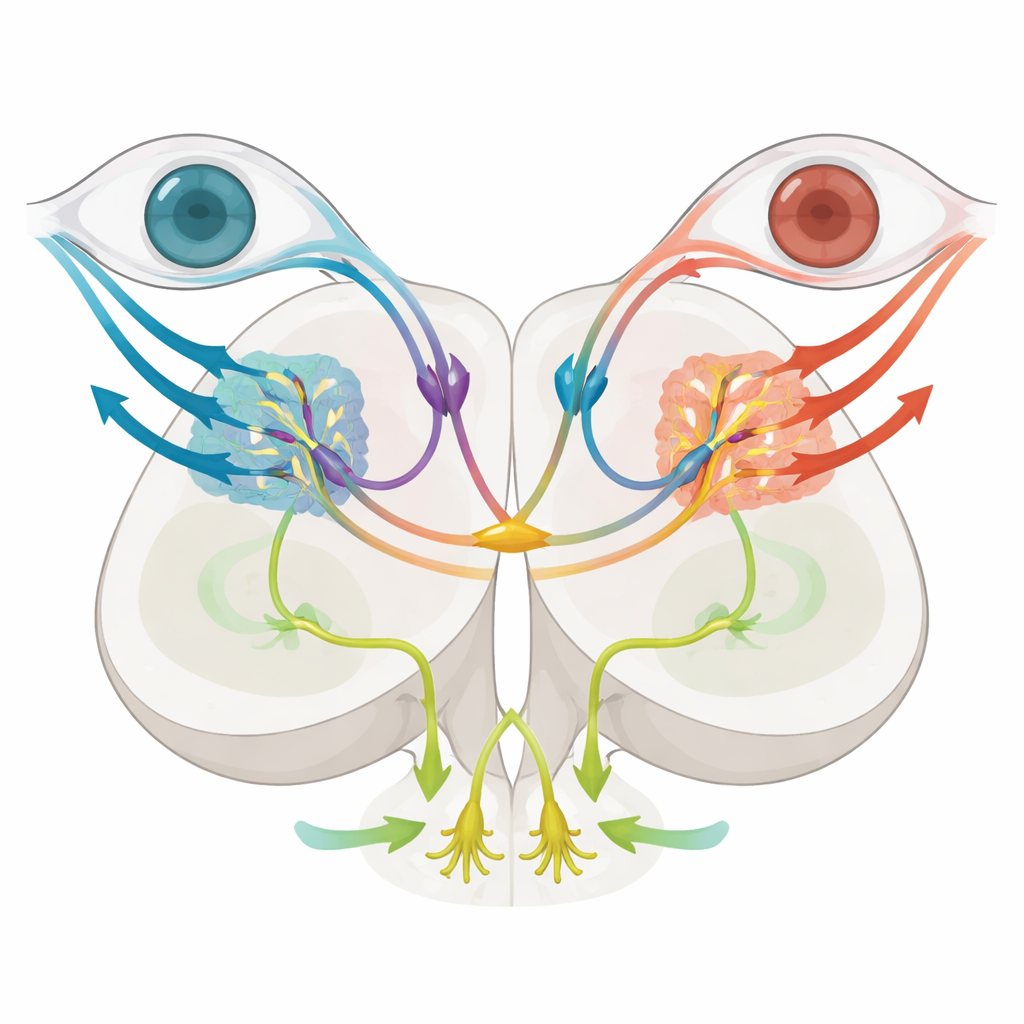
Augen‑ und Körperreaktionen entwirren
Um die Funktion zu prüfen, entfernte das Team selektiv nkx1.2lb‑positive prätectale Neuronen mithilfe eines genetischen „Suizid“-Enzyms, das nur in diesen Zellen toxisch wird, wenn den Fischen ein harmloses Mittel verabreicht wird. Nach der Ablation zeigten Larven weiterhin normale Augenverfolgungsbewegungen, wenn sich die Welt um sie drehte, was darauf hindeutet, dass rotationaler optischer Fluss und die daraus resultierende optokinetische Reaktion intakt blieben. Bewegte sich jedoch das Bodenmuster, um Vorwärtsschwimmen zu simulieren, war die optomotorische Reaktion stark abgeschwächt: Die Fische legten kürzere Strecken zurück und ihre Schwanzschläge wurden weniger koordiniert, was eine gestörte Berechnung der Schwimmrichtung zeigt. Hirnbildgebung offenbarte, dass speziell auf translationalen optischen Fluss eingestellte Zellen reduziert waren, während grundlegende monokulare Bewegungsdetektoren weitgehend erhalten blieben. Zusammengenommen deuten diese Experimente darauf hin, dass die kommissuralen nkx1.2lb‑Neuronen wesentlich sind, um Signale beider Augen zu integrieren, geradeaus gerichtete Bewegung zu schätzen und Vorwärtsschwimmen zu steuern, jedoch nicht nötig sind, um den Blick bei Drehungen zu stabilisieren.
Warum das für das Verständnis der Bewegungssinnes wichtig ist
Für Nichtfachleute lautet die Kernbotschaft: Das Gehirn trennt „Drehe ich?“ von „Bewege ich mich vorwärts?“ indem es diese Fragen verschiedenen Zellgruppen zuweist, sogar innerhalb eines winzigen Fisches. Die Autor:innen zeigen, dass eine spezifische inhibitorische Brücke zwischen linker und rechter Seite des Prätectums entscheidend ist, um translationale Bewegung zu erkennen und den Körper zu steuern, während andere Schaltkreise die Rotation und Augenbewegungen ohne diese Brücke bewältigen können. Ihre CaMPARI‑seq‑Methode — Licht zum Markieren aktiver Zellen nutzen und anschließend deren molekulare Identität lesen — bietet einen leistungsfähigen Weg, um zu verknüpfen, was Neurone tun, wie sie gebaut sind und welche Verhaltensweisen sie steuern. Erkenntnisse aus diesem kompakten Zebrafischsystem könnten helfen zu klären, wie größere Wirbeltiergehirne, einschließlich unseres eigenen, das Sehen stabil und die Navigation in einer bewegten Welt genau halten.
Zitation: Matsuda, K., Wang, CH., Kakinuma, H. et al. Molecular and functional dissection using CaMPARI-seq reveals the neuronal organization for dissociating optic flow-dependent behaviors. Nat Commun 17, 3411 (2026). https://doi.org/10.1038/s41467-026-71371-6
Schlüsselwörter: optischer Fluss, Zebrafisch, Prätectum, Einzelzell-RNA-Sequenzierung, visuelle Bewegungsverarbeitung