Clear Sky Science · fr
Dissection moléculaire et fonctionnelle avec CaMPARI-seq révèle l’organisation neuronale dissociant les comportements dépendants du flux optique
Comment le cerveau distingue tourner de nager tout droit
Quand les animaux se déplacent, tout le paysage visuel semble défiler devant leurs yeux. À partir de cette scène en perpétuel déplacement, le cerveau doit résoudre une question simple mais vitale : sommes‑nous en train de tourner, ou avançons‑nous tout droit ? Cet article utilise de petits poissons zèbres et une nouvelle technique moléculaire de « surlignage » pour révéler comment des cellules cérébrales spécifiques séparent ces deux types de mouvement afin de contrôler soit les mouvements oculaires, soit la nage globale du corps.
Voir le mouvement comme un paysage qui s’écoule
Lorsqu’un animal nage ou marche, des motifs lumineux balayent la rétine : c’est le flux optique. Le flux rotationnel, comme lors d’une rotation de la tête, doit principalement déclencher des mouvements oculaires qui stabilisent le regard. Le flux translationnel, comme lors d’une avancée, doit en revanche piloter le corps pour rester en phase avec l’eau ou le sol environnant. Chez de nombreux vertébrés, y compris le poisson zèbre, une région mésencéphalique appelée le prétectum joue un rôle central dans l’interprétation de ces motifs de mouvement et le routage des signaux vers les centres moteurs. Des travaux antérieurs avaient cartographié de nombreux neurones prétectaux répondant au flux optique, mais il restait flou quels types cellulaires précis, définis par leur expression génique et leur câblage, sous‑tendaient les différents comportements guidés par le mouvement.
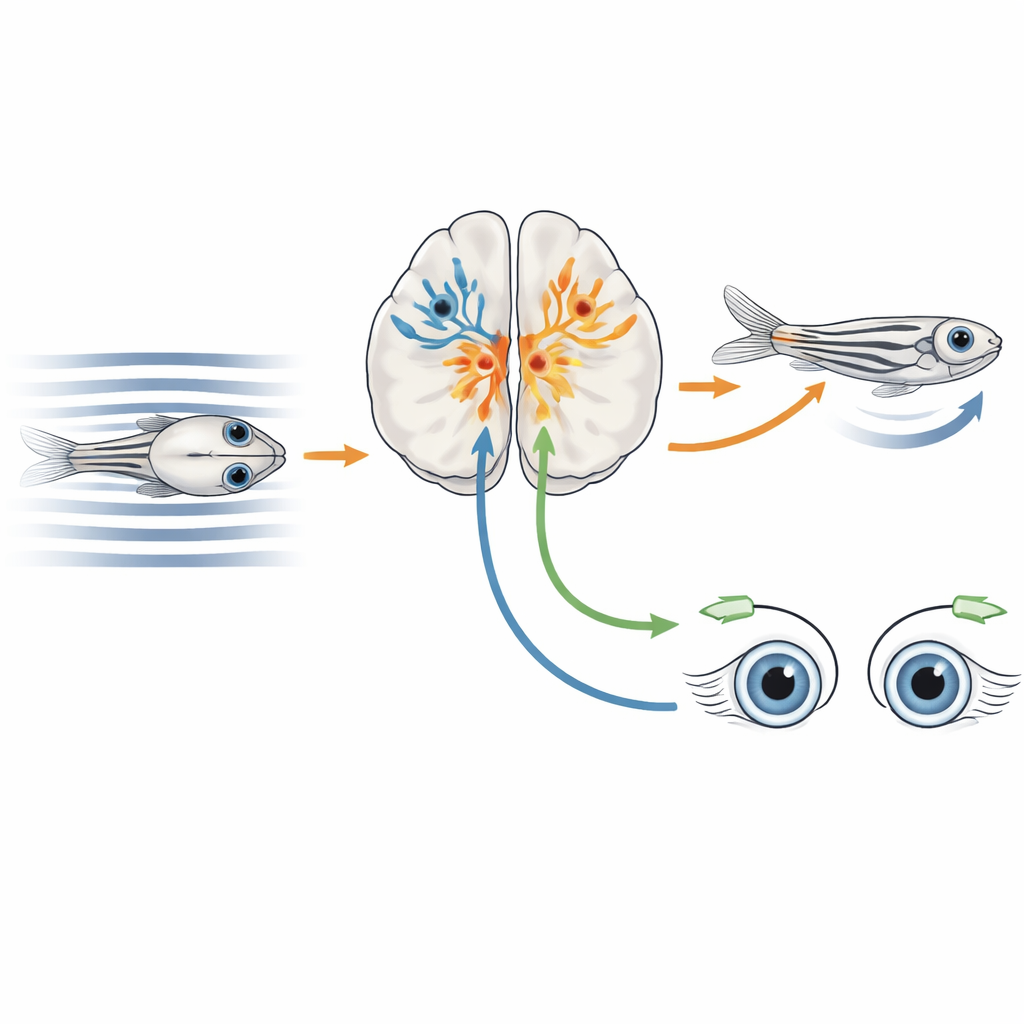
Illuminer les neurones actifs et lire leurs gènes
Les chercheurs ont développé une approche hybride qu’ils appellent CaMPARI‑seq, combinant le marquage optique des neurones actifs et le profilage de l’expression génique au niveau unicellulaire. Ils ont modifié génétiquement des larves de poisson zèbre pour que la plupart des neurones produisent une protéine fluorescente spéciale, CaMPARI2, ciblée dans le noyau cellulaire. Lorsque les neurones sont actifs et exposés à la lumière ultraviolette, cette protéine bascule de façon permanente du vert au rouge. L’équipe a exposé les poissons à des motifs de bandes mobiles créant diverses conditions de flux optique binoculaire, tout en illuminant le prétectum en ultraviolet. Les neurones actifs, sensibles au mouvement, viraient au rouge, étaient ensuite isolés un par un, et leurs séquences d’ARN furent lues pour déterminer quels gènes chaque cellule exprimait.
Construire une atlas cellulaire des neurones sensibles au flux optique
En regroupant des milliers de cellules marquées selon leurs profils d’expression génique, les auteurs ont identifié un groupe prétectal majeur marqué par le gène tcf7l2, dont la plupart des cellules exprimaient aussi des gènes typiques de neurones inhibiteurs. En utilisant des poissons génétiquement modifiés où les cellules tcf7l2‑positives déclenchent un indicateur calcique, ils ont vérifié que cette large population comprenait presque tous les types de réponses au flux optique décrits précédemment, des neurones accordés au mouvement perçu par un seul œil à d’autres ne répondant que lorsque les deux yeux détectent un mouvement avant ou arrière cohérent. Une subdivision plus fine du groupe tcf7l2 a révélé sept sous‑types moléculairement distincts, chacun avec sa combinaison de gènes marqueurs et une position spatiale en grande partie non chevauchante dans le prétectum, suggérant un patchwork de circuits inhibiteurs spécialisés organisés autour du noyau de traitement du mouvement.
Deux sous‑types clés avec des fonctions très différentes
Parmi ces sous‑types, deux se sont distingués. Les cellules exprimant le gène mafaa se situaient dans une région migrée latérale qui chevauche les fibres rétiniennes directionnellement sélectives entrantes. L’imagerie et le traçage anatomique ont montré que ces neurones établissent des connexions locales et répondent fortement quand des bandes se déplacent dans une direction particulière au niveau d’un seul œil, ce qui correspond à un rôle d’encodage de mouvements simples et spécifiques à un œil pouvant soutenir la rotation oculaire. En revanche, les neurones exprimant nkx1.2lb occupaient une zone plus médiale et envoyaient de longues projections croisées via une commissure dorsale vers le côté opposé, formant un pont entre les circuits prétectaux gauche et droit. Ces cellules nkx1.2lb‑positives étaient également majoritairement inhibitrices et couvraient ensemble une large variété de types de réponses au flux optique, incluant des motifs monoculaires et binoculaires, suggérant qu’elles participent à la comparaison des signaux des deux yeux.
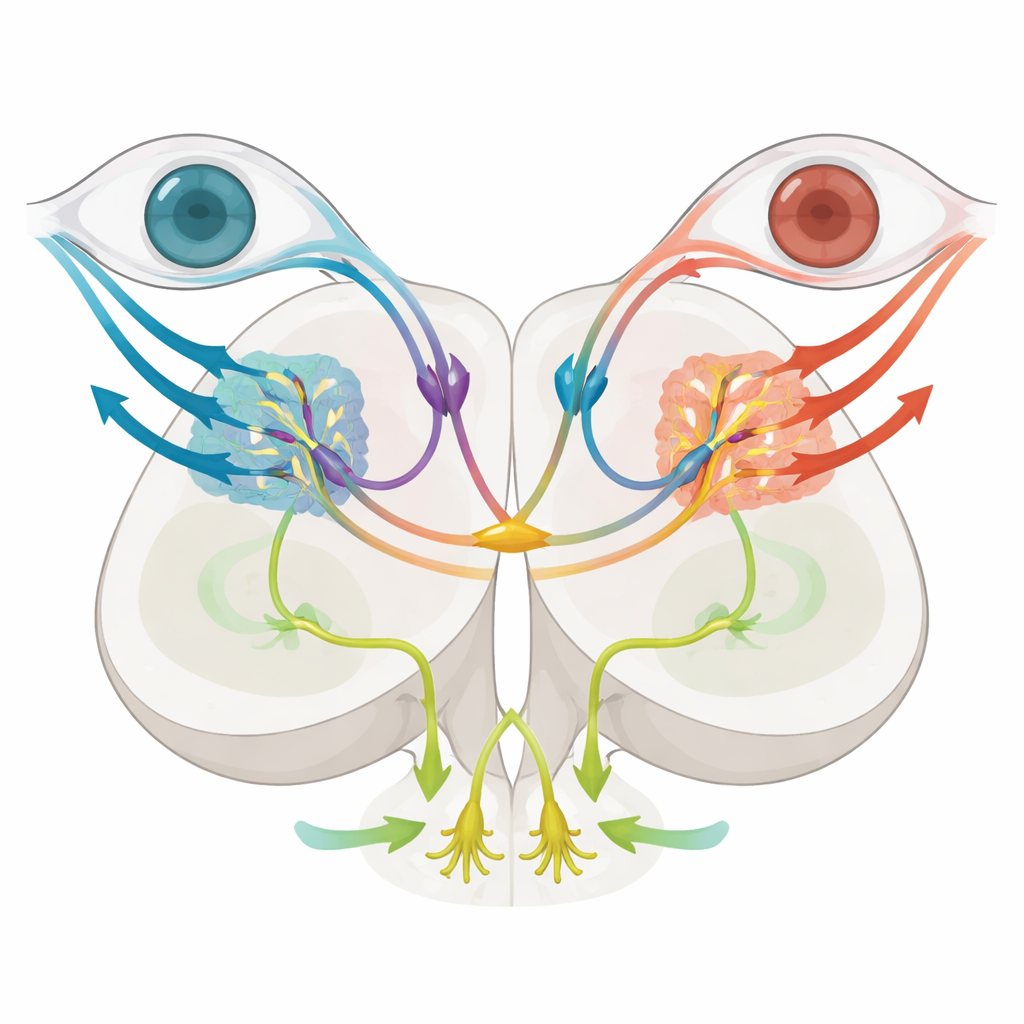
Démêler les réponses oculaires et corporelles
Pour tester la fonction, l’équipe a éliminé sélectivement les neurones prétectaux nkx1.2lb‑positifs à l’aide d’une enzyme génétique « suicide » qui devient toxique uniquement dans ces cellules lorsque les poissons reçoivent un médicament inoffensif. Après ablation, les larves présentaient encore des mouvements de poursuite oculaire normaux lorsque le monde tournait autour d’elles, indiquant que le flux optique rotationnel et la réponse optocinétique restaient intacts. Toutefois, quand le motif du sol se déplaçait pour imiter une nage vers l’avant, la réponse optomotrice était fortement amoindrie : les poissons parcouraient des distances plus courtes et leurs battements de queue étaient moins coordonnés, montrant une altération du calcul de la direction de nage. L’imagerie cérébrale a révélé une diminution des cellules spécifiquement accordées au flux translationnel, tandis que les détecteurs de mouvement monoculaires de base étaient largement préservés. Ensemble, ces expériences suggèrent que les neurones commissuraux nkx1.2lb sont essentiels pour intégrer les signaux des deux yeux afin d’estimer le mouvement vers l’avant et de piloter la nage, mais ne sont pas requis pour stabiliser le regard lors d’une rotation.
Pourquoi c’est important pour comprendre la détection du mouvement
Pour un non‑spécialiste, le message clé est que le cerveau sépare « est‑ce que je tourne ? » de « est‑ce que j’avance tout droit ? » en confiant ces questions à des ensembles distincts de cellules, même chez un tout petit poisson. Les auteurs montrent qu’un pont inhibiteur spécifique entre les côtés gauche et droit du prétectum est crucial pour reconnaître le mouvement translationnel et orienter le corps, tandis que d’autres circuits peuvent gérer le mouvement rotationnel et les mouvements oculaires sans ce pont. Leur méthode CaMPARI‑seq — utiliser la lumière pour marquer les cellules actives puis lire leur identité moléculaire — offre un moyen puissant de relier ce que font les neurones, comment ils sont construits et quels comportements ils contrôlent. Les enseignements tirés de ce système compact chez le poisson zèbre pourraient aider à éclairer comment des cerveaux de vertébrés plus grands, y compris le nôtre, maintiennent la stabilité visuelle et la précision de la navigation dans un monde en mouvement.
Citation: Matsuda, K., Wang, CH., Kakinuma, H. et al. Molecular and functional dissection using CaMPARI-seq reveals the neuronal organization for dissociating optic flow-dependent behaviors. Nat Commun 17, 3411 (2026). https://doi.org/10.1038/s41467-026-71371-6
Mots-clés: flux optique, poisson zèbre, prétectum, séquençage ARN unicellulaire, traitement du mouvement visuel