Clear Sky Science · es
Disección molecular y funcional mediante CaMPARI-seq revela la organización neuronal para disociar comportamientos dependientes del flujo óptico
Cómo el cerebro distingue girar de nadar en línea recta
Cuando los animales se mueven, el mundo visual entero parece deslizarse ante sus ojos. A partir de esta escena en constante cambio, el cerebro debe resolver una pregunta simple pero vital: ¿estamos girando o avanzando en línea recta? Este artículo utiliza diminutos peces cebra y una nueva técnica molecular de “resaltado” para revelar cómo células cerebrales específicas separan estos dos tipos de movimiento para controlar ya sea los movimientos oculares o la natación de todo el cuerpo.
Ver el movimiento como un paisaje que fluye
Cuando un animal nada o camina, patrones de luz barren los ojos, un fenómeno llamado flujo óptico. El flujo rotacional, como cuando un animal gira la cabeza, debería impulsar principalmente movimientos oculares que estabilicen la mirada. El flujo translacional, como cuando el animal avanza, debería en cambio impulsar el cuerpo para mantener el movimiento con respecto al agua o al suelo circundante. En muchos vertebrados, incluido el pez cebra, una región del mesencéfalo llamada pretecto desempeña un papel central en interpretar estos patrones de movimiento y en encaminar señales hacia centros motores. Trabajos previos habían cartografiado muchas neuronas pretectales que responden al flujo óptico, pero seguía sin quedar claro qué tipos celulares precisos, definidos por su expresión génica y su conectividad, eran responsables de los distintos comportamientos impulsados por el movimiento.
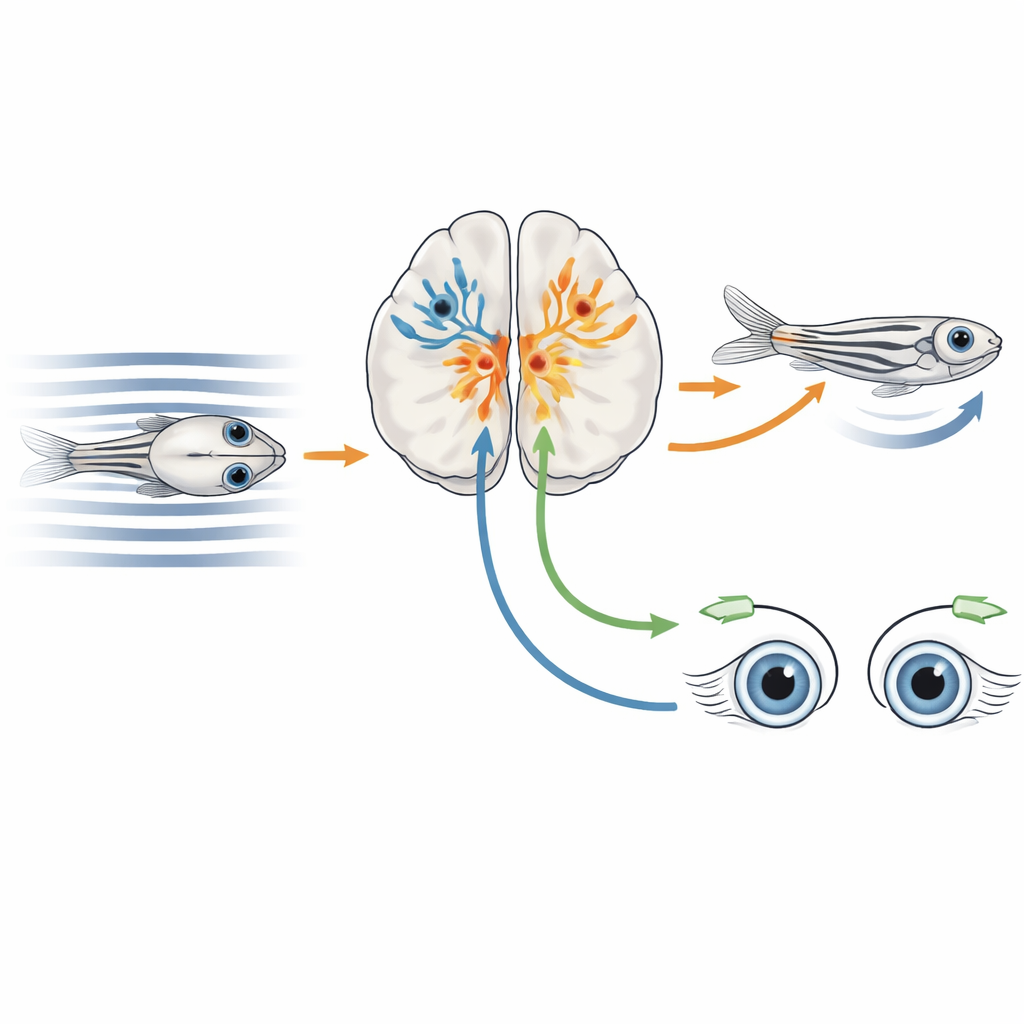
Iluminar neuronas activas y leer sus genes
Los investigadores desarrollaron un enfoque híbrido que llaman CaMPARI-seq, combinando el marcado óptico de neuronas activas con el perfilado de expresión génica a nivel de célula individual. Ingeniería genética en larvas de pez cebra hizo que la mayoría de las neuronas produjeran una proteína fluorescente especial, CaMPARI2, dirigida al núcleo celular. Cuando las neuronas están activas y se iluminan con luz ultravioleta, esta proteína cambia de forma permanente de verde a rojo. El equipo expuso a los peces a patrones de franjas en movimiento que generan una gama de condiciones de flujo óptico binocular, mientras iluminaban el pretecto con ultravioleta. Las neuronas activas y sensibles al movimiento se volvieron rojas, se aislaron posteriormente una por una y se leyó su ARN para determinar qué genes expresaba cada célula.
Construyendo un atlas celular de neuronas del flujo óptico
Mediante el agrupamiento de miles de células etiquetadas según sus patrones de expresión génica, los autores identificaron un grupo pretectal mayor marcado por el gen tcf7l2, la mayoría de cuyas células también portaban genes típicos de neuronas inhibitorias. Usando peces genéticamente modificados en los que las células positivas para tcf7l2 activaban un indicador de calcio, verificaron que esta población amplia incluía casi todos los tipos de respuesta al flujo óptico descritos anteriormente, desde neuronas afinadas al movimiento visto por un solo ojo hasta otras que respondían solo cuando ambos ojos percibían un movimiento coherente hacia delante o hacia atrás. Dividir más el grupo tcf7l2 reveló siete subtipos molecularmente distintos, cada uno con su propia combinación de genes marcadores y una posición espacial en gran medida no solapada dentro del pretecto, lo que sugiere un mosaico de circuitos inhibitorios especializados alrededor del centro de procesamiento del movimiento.
Dos subtipos clave con funciones muy diferentes
Entre estos subtipos, dos destacaron. Las células que expresan el gen mafaa se ubicaban en una región lateral migrada que se solapa con fibras retinianas selectivas a la dirección entrantes. Imagenología y trazado anatómico mostraron que estas neuronas establecen conexiones locales y responden con fuerza cuando las franjas se mueven en una dirección particular en un solo ojo, lo que coincide con un papel en codificar movimiento simple y específico de un ojo que puede apoyar el giro ocular. En contraste, las neuronas que expresan nkx1.2lb ocupaban una zona más medial y enviaban largas proyecciones cruzadas a través de una comisura dorsal cerebral hacia el lado opuesto, formando un puente entre los circuitos pretectales izquierdo y derecho. Estas células positivas para nkx1.2lb también eran mayoritariamente inhibitorias, y en conjunto abarcaban una amplia variedad de tipos de respuesta al flujo óptico, incluyendo patrones monoculares y binoculares, lo que sugiere que ayudan a comparar señales de ambos ojos.
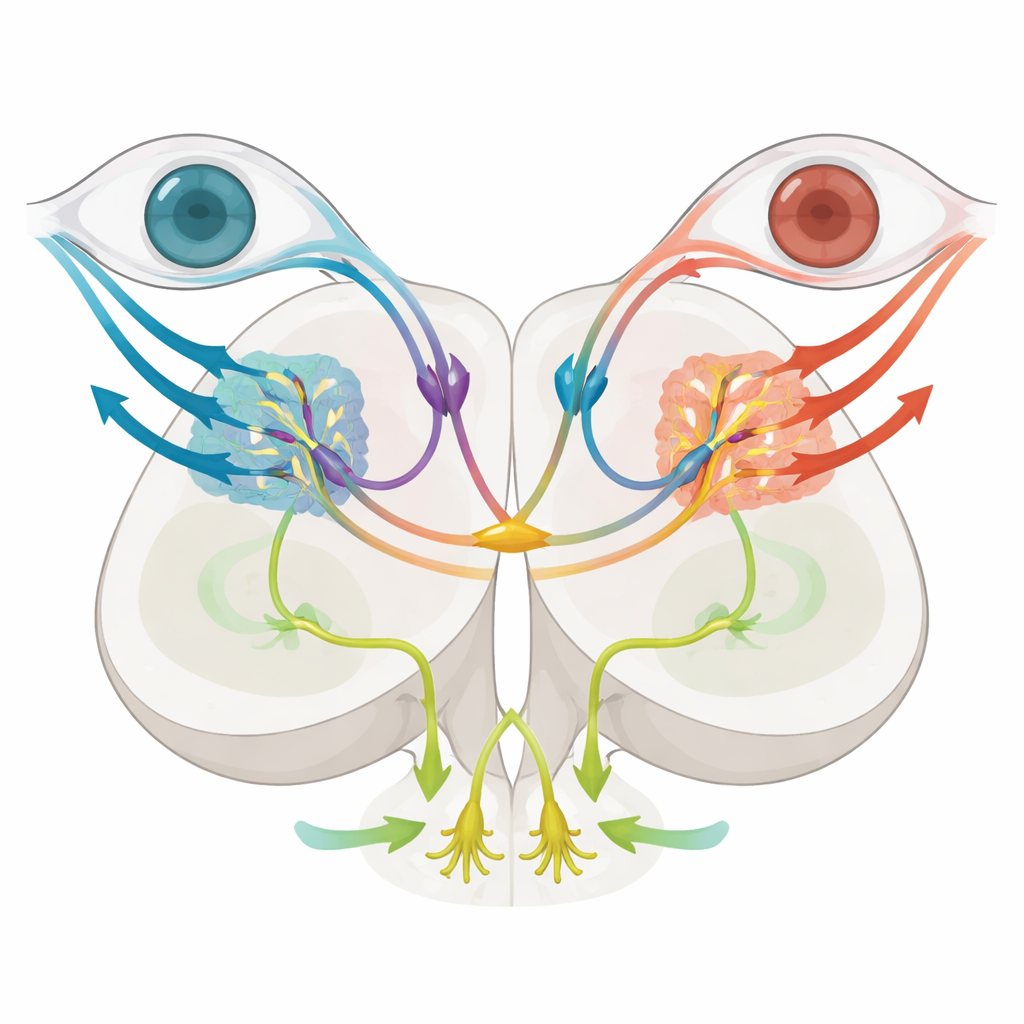
Desenredando las respuestas oculares y corporales
Para probar la función, el equipo eliminó selectivamente las neuronas pretectales positivas para nkx1.2lb usando una enzima genética de “suicidio” que se vuelve tóxica solo en esas células cuando a los peces se les administra un fármaco inocuo. Tras la ablación, las larvas todavía mostraron movimientos de seguimiento ocular normales cuando el mundo giraba a su alrededor, lo que indica que el flujo óptico rotacional y la respuesta optocinética resultante permanecieron intactos. Sin embargo, cuando el patrón del suelo se movió para imitar la natación hacia delante, la respuesta optomotriz se debilitó notablemente: los peces recorrieron distancias más cortas y sus latidos de cola se volvieron menos coordinados, mostrando una alteración en el cálculo de la dirección de nado. La imagenología cerebral reveló que las células afinadas específicamente al flujo óptico translacional se vieron reducidas, mientras que los detectores básicos de movimiento monocular se conservaron en gran medida. En conjunto, estos experimentos sugieren que las neuronas comisurales nkx1.2lb son esenciales para integrar señales de ambos ojos para estimar el movimiento hacia adelante y propulsar la natación, pero no son necesarias para estabilizar la mirada durante el giro.
Por qué esto importa para entender la detección del movimiento
Para un no especialista, el mensaje clave es que el cerebro separa “¿estoy girando?” de “¿estoy moviéndome hacia adelante?” asignando estas preguntas a distintos conjuntos de células, incluso en un pez diminuto. Los autores muestran que un puente inhibitor io específico entre los lados izquierdo y derecho del pretecto es crucial para reconocer el movimiento translacional y dirigir el cuerpo, mientras que otros circuitos pueden encargarse del movimiento rotacional y de los movimientos oculares sin este puente. Su método CaMPARI-seq —usar luz para marcar células activas y luego leer su identidad molecular— ofrece una forma potente de vincular lo que hacen las neuronas, cómo están construidas y qué conductas controlan. Las ideas provenientes de este compacto sistema de pez cebra podrían ayudar a aclarar cómo cerebros vertebrados mayores, incluido el nuestro, mantienen la visión estable y la navegación precisa en un mundo en movimiento.
Cita: Matsuda, K., Wang, CH., Kakinuma, H. et al. Molecular and functional dissection using CaMPARI-seq reveals the neuronal organization for dissociating optic flow-dependent behaviors. Nat Commun 17, 3411 (2026). https://doi.org/10.1038/s41467-026-71371-6
Palabras clave: flujo óptico, pez cebra, pretecto, secuenciación de ARN unicelular, procesamiento del movimiento visual