Clear Sky Science · pt
Mutações no KIF11 que causam deficiência intelectual prejudicam a dinâmica dos microtúbulos e a arborização dendrítica
Como pequenos motores celulares moldam o pensamento
Nossos cérebros dependem de bilhões de neurônios que precisam se conectar com precisão notável. Este estudo investiga como um único motor molecular, chamado KIF11, ajuda a esculpir a “árvore” ramificada dos prolongamentos neuronais que recebem sinais, e como alterações patológicas nesse motor podem levar à deficiência intelectual. Ao observar neurônios vivos no microscópio e sondar a mecânica do KIF11 em tubos de ensaio e em camundongos, os autores revelam como essa proteína ajusta a estrutura interna dos neurônios e, por sua vez, sua capacidade de se comunicar.
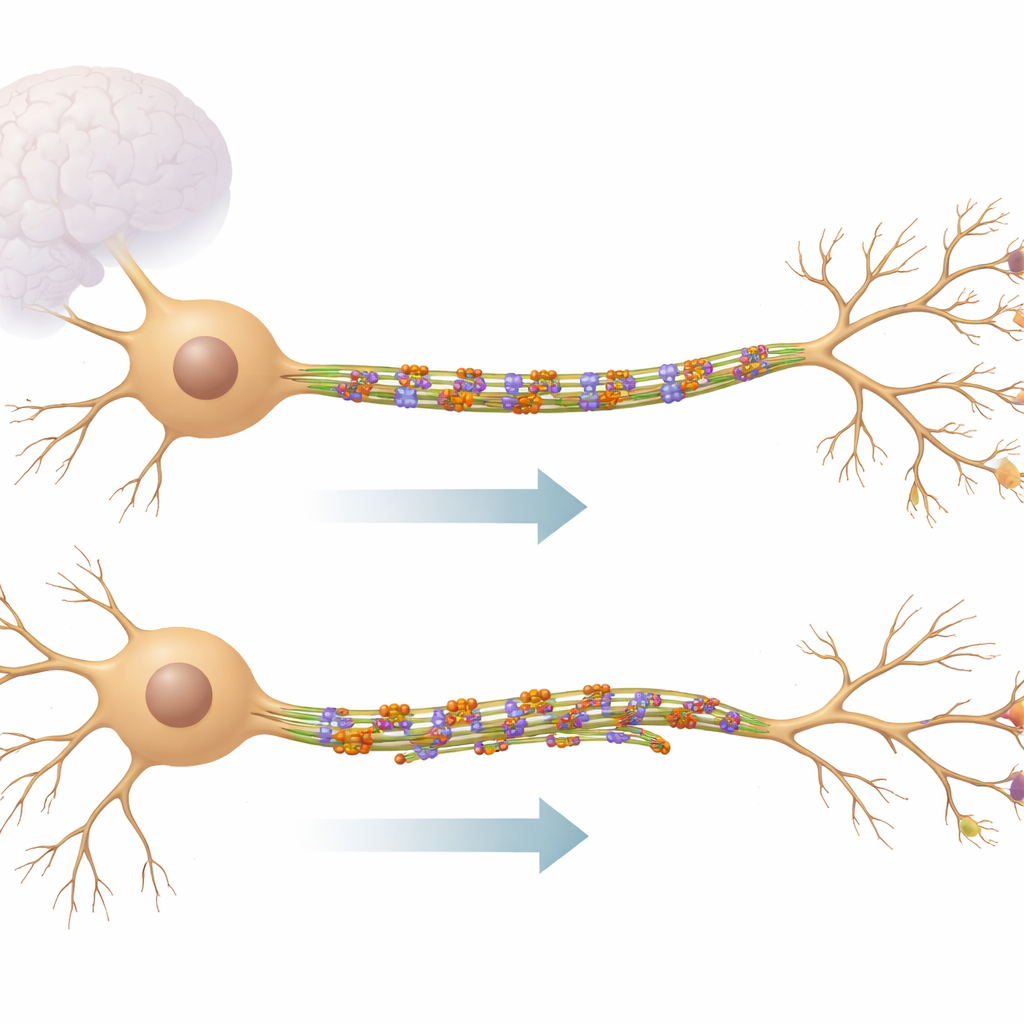
O sistema ferroviário interno do neurônio
Os neurônios enviam e recebem informações por meio de extensões longas e semelhantes a cabos. No interior desses cabos correm os microtúbulos, hastes proteicas rígidas que funcionam como trilhos para transporte de suprimentos e ajudam a definir a forma da célula. Nos principais ramos receptores, chamados dendritos, os microtúbulos correm em ambas as direções, criando uma rede mista e dinâmica. O KIF11 pertence a uma família de pequenos motores que normalmente atuam durante a divisão celular, mas este trabalho mostra que ele também permanece ativo em células cerebrais totalmente desenvolvidas. Em vez de transportar carga, o KIF11 liga microtúbulos vizinhos, atuando mais como um freio e estabilizador do que como um caminhão de entrega.
Manter o crescimento em equilíbrio
Usando imageamento ao vivo de neurônios do hipocampo de camundongo, os pesquisadores reduziram os níveis de KIF11 ou bloquearam sua atividade com drogas e acompanharam as pontas dos microtúbulos em crescimento. Eles descobriram que, quando o KIF11 foi inibido, uma classe particular de microtúbulos — aqueles com sua “extremidade menos” apontando para fora — tornou‑se mais ativa, especialmente em ramos dendríticos secundários e terciários. Isso aumentou o surgimento e o crescimento desses trilhos e incentivou a formação de novos ramos, tornando a árvore dendrítica mais complexa. Por outro lado, quando o KIF11 foi superproduzido, a dinâmica dos microtúbulos desacelerou, os dendritos ficaram menos complexos e os trilhos internos às vezes se torciam e formavam laços, sugerindo que força excessiva do KIF11 pode entortar e tensionar o esqueleto.
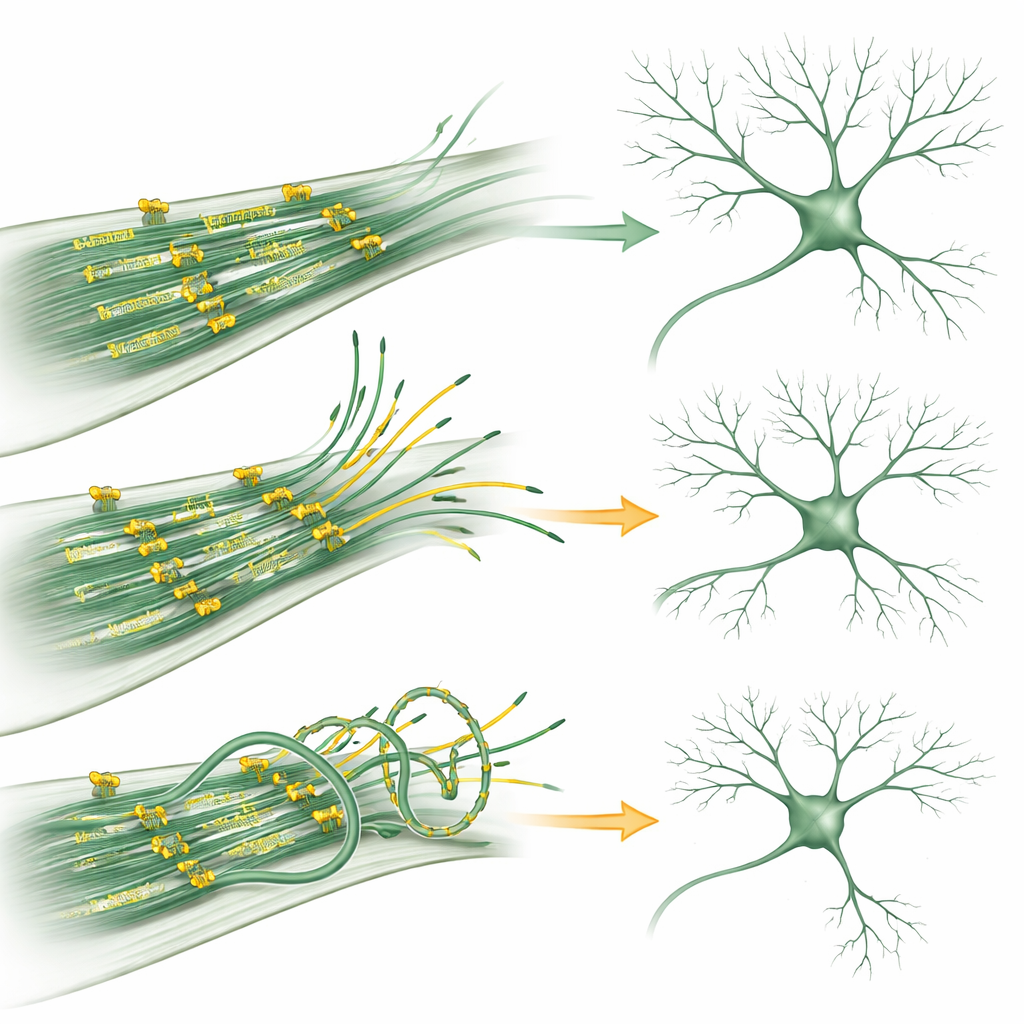
Quando um motor dá errado
Certa famílias afetadas por uma condição rara chamada MCLID — marcada por microcefalia, problemas oculares, edema de membros e deficiência intelectual — carregam mutações no gene KIF11. A equipe recriou duas dessas mutações em laboratório. Em neurônios, ambas as formas alteradas do KIF11 reduziram a dinâmica dos microtúbulos e diminuíram a ramificação dendrítica, de forma semelhante à superprodução de KIF11. Testes bioquímicos detalhados revelaram como: um mutante atrapalhou a capacidade do KIF11 de se montar em sua estrutura normal de quatro partes, enfraquecendo sua aptidão para ligar microtúbulos; o outro ainda formou o complexo correto, mas deslizou ao longo dos microtúbulos muito mais lentamente e teve afinidade reduzida pela molécula combustível ATP. Apesar dessas diferenças, ambos os mutantes continuaram a exercer forças anormais sobre os microtúbulos, desequilibrando o delicado balanço entre estabilidade e flexibilidade que os neurônios exigem.
Da forma celular aos sinais cerebrais
Os autores então perguntaram se essas mudanças estruturais importam para a comunicação entre neurônios. Ao registrar pequenos eventos elétricos espontâneos em células cultivadas, mostraram que aumentar a quantidade de KIF11 normal ou introduzir qualquer um dos mutantes reduziu significativamente a frequência com que vesículas sinápticas liberavam suas mensagens químicas, embora o tamanho de cada evento permanecesse o mesmo. Em camundongos vivos, a introdução das variantes humanas do KIF11 em neurônios em desenvolvimento do hipocampo levou a árvores dendríticas mais curtas e menos ramificadas, com a gravidade dependendo da mutação específica e do estágio de desenvolvimento. Em conjunto, essas descobertas ligam a atividade prejudicada do KIF11 tanto à arquitetura física dos neurônios quanto ao fluxo de informação através de circuitos cerebrais.
Motores controlados por luz e uma nova visão da doença
Para testar se alterar localmente a atividade do KIF11 é suficiente para remodelar neurônios, os pesquisadores projetaram uma versão sensível à luz do motor. Rápidos flashes de luz violeta desligaram o KIF11 em segmentos dendríticos escolhidos, aumentando rapidamente o crescimento dos microtúbulos e desencadeando o brotamento de novos ramos em minutos. Pulsos de luz opostos ligaram o KIF11 e reduziram o crescimento enquanto induziam dobras e laços nos feixes de microtúbulos. Esses experimentos sustentam uma imagem simples: o KIF11 age como um reostato, ou dimmer, para os trilhos internos do neurônio — atividade insuficiente permite crescimento excessivo dos ramos, enquanto atividade excessiva ou forças inadequadas os tornam rígidos ou distorcidos. Na MCLID, proteínas KIF11 mutantes parecem aplicar forças desequilibradas sobre os microtúbulos, levando a árvores dendríticas instáveis e comunicação sináptica enfraquecida, o que provavelmente contribui para dificuldades de aprendizagem e cognição.
Citação: Wingfield, J.L., Niese, L., Avchalumov, Y. et al. Intellectual disability-causing mutations in KIF11 impair microtubule dynamics and dendritic arborization. Nat Commun 17, 4125 (2026). https://doi.org/10.1038/s41467-026-70522-z
Palavras-chave: microtúbulos neuronais, ramificação dendrítica, proteínas motoras cinésinas, deficiência intelectual, transmissão sináptica